Tuberkulosis atau TB atau istilah lama dan sering dikenal di masyarakat yaitu TBC merupakan penyakit infeksi kronis nomor satu di Indonesia. Infeksi ini disebabkan oleh bakteri Mycobacterium tuberculosis yang dapat menyebabkan infeksi laten maupun infeksi aktif. Infeksi M. tuberculosis merupakan endemis di Indonesia dengan perkiraan menginfeksi sekitar dua per tiga dari populasi negara kita. (Gambar thumbnail adalah lukisan La Miseria oleh Cristóbal Rojas (1886)).
Daftar Isi
Etiologi: Mycobacterium tuberculosis
Terdapat 5 bakteri yang berkaitan dengan infeksi TB yaitu Mycobacterium tuberculosis, Mycobacterium bovis, Mycobacterium africanum, Mycobacterium microti, dan Mycobacterium cannettii. Adapun bakteri utama penyebab penyakit tuberkulosis ada bakteri Mycobacterium tuberculosis. Untuk pembahasan lebih detil mengenai bakteri ini dapat disimak di artikel dengan tautan ini.
Selain manusia, tidak ditemukan hewan yang berperan sebagai agen penularan MTB. M. bovis dapat bertahan dalam susu sapi yang terinfeksi dan melakukan penetrasi ke mukosa saluran cerna serta menginvasi jaringan limfe orofaring saat seseorang mengonsumsi susu dari sapi yang terinfeksi tersebut. Untungnya, kejadian infeksi M. bovis pada manusia sudah mengalami penurunan signifikan di negara berkembang dikarenakan proses pasteurisasi susu dan telah diberlakukannya strategi kontrol tuberkulosis yang efektif pada ternak. Infeksi terhadap organisme lain relatif jarang ditemukan.
Penularan Tuberkulosis
Tuberkulosis merupakan penyakit menular dimana bakteri berpindah dari individu dengan infeksi aktif ke individu lainnya. Kuman MTB ditularkan lewat udara yaitu melalui droplet (5 mikron) yang mengandung bakteri. Droplet ini dihasilkan ketika penderita tuberkulosis aktif batuk, bersin, bicara, atau meludah. Air liur yang mengandung bakteri berubah menjadi droplet dan apabila droplet ini dihirup orang sehat, maka bakteri akan berpindah dan menginfeksi orang tersebut.
Dalam satu droplet bisa mengandung 1-5 basil MTB dan dapat bertahan hidup di udara sampai 4 jam. Sekali batuk dapat menghasilkan 3000 droplet sedangkan sekali bersin menghasilkan 1 juta droplet. Untuk menginfeksi, dibutuhkan sekitar setidaknya 1-10 basil MTB. Pada kasus TB ekstraparu biasanya tidak infeksius kecuali penderita juga menderita TB paru.
Jadi, sebagian besar rute infeksi adalah melalui saluran pernapsan. Cara lain bisa dengan kontak langsung bakteri lewat kulit atau tertelan lewat salutan cerna.
MTB dapat hidup bertahan lama di luar tubuh inang. Bakteri ini tetap hidup selama satu tahun dalam air, 6 bulan dalam tanah, dan beberapa bulan di debu atau dahak kering. Dikarenakan kandungan lipid yang tinggi dalam dinding sel, MTB relatif tahan terhadap desinfektan.
Untuk membunuh kuman MTB diperlukan proses desinfeksi yang lebih lama. Adapun zat desinfektan yang paling efektif digunakan adalah jenis zat kimia yang mengandung klorin. Selain dengan desinfektan, MTB dapat dibunuh dengan pemanasan sampai 100°C maupun pasteurisasi. MTB juga sensitif atau terbunuh oleh sinar matahari dan radiasi ultraviolet.
Epidemiologi
Tuberkulosis merupakan masalah dunia. WHO memperkirakan 1 milyar populasi terinfeksi penyakit ini dengan sekitar 8,7 juta kasus baru dan menyebabkan 1,4 juta kematian per tahun. Sejak awal abad ke-20, kasus dan kematian akibat tuberkulosis menurun secara pesat namun dengan kemunculan HIV/AIDS dalam empat dekade terakhir, tuberkulosis kembali menjadi perhatian karena besarnya risiko kelompok ini menderita tuberkulosis.
Data Global
Pada tahun 2016 terdapat sekitar 10,4 juta kasus insiden TB atau setara dengan 120 kasus per 100.000 penduduk. Lima negara dengan insiden kasus tertinggi yaitu India, Indonesia, China, Philipina, dan Pakistan. Asia menjadi benua dengan jumlah penderita TB terbanyak diikuti dengan Afrika.

Selain jumlah kasus yang besar, beban penyakit tuberkulosis juga bertambah seiring dengan munculnya HIV dan resistensi MTB. Data di bawah adalah daftar negara yang memiliki beban penyakit TB yang besar:
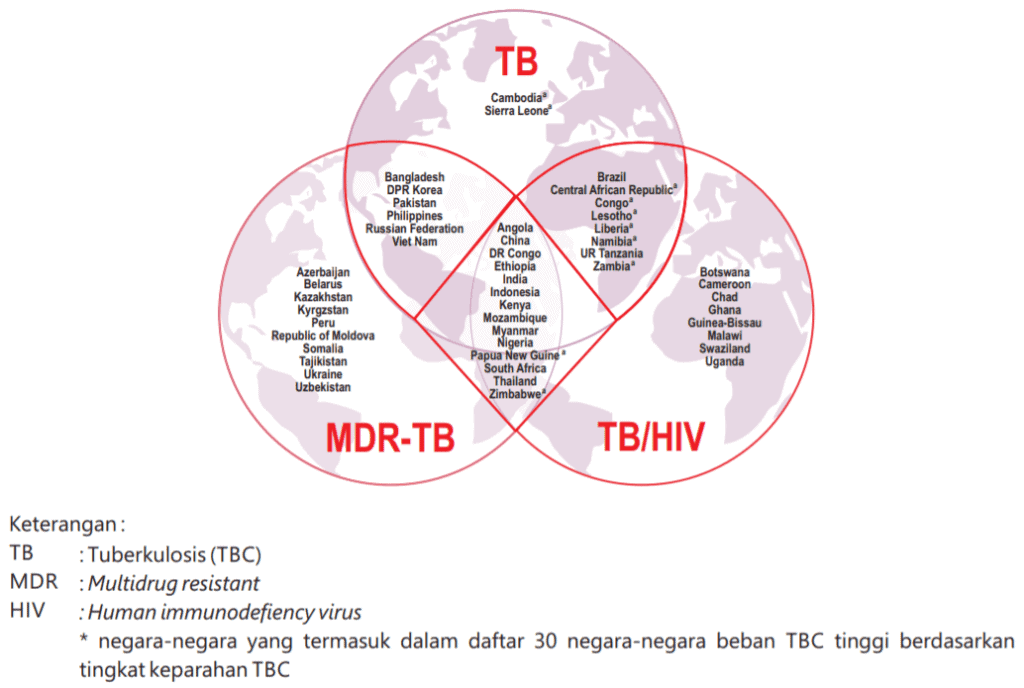
Data Tuberkulosis di Indonesia
Indonesia merupakan negara endemis tuberkulosis dengan jumlah penderita dan beban penyakit yang tinggi di dunia. Jumlah kasus baru TB di Indonesia sebanyak 420.994 kasus pada tahun 2017.
Di Indonesia, jumlah kasus baru TB pada laki-laki 1,4 kali lebih besar dibandingkan pada perempuan. Prevalensi pada laki-laki juga 3 kali lebih tinggi dibandingkan pada perempuan. Profil ini kurang lebih sama dengan negara-negara lain.
Faktor yang menyebabkannya karena laki-laki lebih terpapar pada faktor risiko TBC misalnya merokok dan kurangnya ketidakpatuhan minum obat. Dalam survei ditemukan bahwa partisipan laki penderita TB yang merokok sebanyak 68,5% dan hanya 3,7% perempuan yang merokok.
Faktor lain adalah usia, dimana prevalensi tinggi TB di Indonesia banyak yang berusia lanjut, pendidikan rendah, dana sosial ekonomi menengah ke bawah.

Faktor Risiko Penyakit Tuberkulosis
Terdapat kelompok individu yang memiliki risiko tinggi mengalami penyakit TB yaitu sebagai berikut:
- Orang dengan HIV positif dan penyakit imunokompromais lain
- Orang yang mengonsumsi obat imunosupresan dalam jangka waktu panjang.
- Perokok
- Konsumsi alkohol tinggi
- Anak usia <5 tahun dan lansia
- Memiliki kontak erat dengan orang dengan penyakit TB aktif yang infeksius.
- Berada di tempat dengan risiko tinggi terinfeksi tuberkulosis (contoh: lembaga permasyarakatan, fasilitas panti)
- Petugas kesehatan
Perjalanan Penyakit dan Patogenesis Tuberkulosis
Tuberkulosis merupakan infeksi kronik. Kuman ini tinggal di makrofag dan membelah setiap 23-32 jam sekali. Pada individu yang terinfeksi, dapat menjadi infeksi primer aktif dan infeksi laten. Infeksi laten dapat mengalami reaktivasi menjadi infeksi aktif kembali apabila terdapat perubahan kondisi misalnya apabila penderita mengalami imunodefisiensi.
Progres perjalanan infeksi ini tergantung dari proses imunitas yang dimediasi oleh sel T. Selain menyebabkan bentuk khas lesi infeksi TB, reaksi sel T ini juga bertanggung jawab dalam bentuk reaksi yang dimunculkan oleh tubuh terhadap patogen MTB.
Pada tahap permulaan, saat kuman MTB masuk, maka kuman ini akan bereaksi dengan makrofag. Berikut proses patogenesis infekti TB mulai infeksi makrofag, terjadinya reaksi imun terhadap kuman TB, dan reaksi imunitas yang menyebabkan munculnya gambaran klinis tuberkulosis.
Fase Awal Infeksi M. tuberculosis (MTB)
Yang dimaksud fase awal adalah fase di mana kuman masuk sampai munculnya reaksi imunitas awal dari tubuh. Kuman MTB masuk melalui proses fagositosis yang dimediasi oleh reseptor di fagosit seperti mannose binding lectin dan CR3.
Kuman MTB masuk ke dalam tubuh melalui rute paling umum yaitu airborne menumpang dalam aerosol. MTB merupakan patogen intraseluler yang hidup dalam sel target yaitu makrofag. Saat tiba di sistem pernapasan, MTB akan berinteraksi dengan sel makrofag melalui reseptor mannosa atau C3b. Setelah berinteraksi dengan reseptor, MTB akan masuk melalui proses fagositosis.
Setelah masuk, maka terbentuk fagosom. Di fagosom, MTB mengeluarkan faktor yang menghambat maturasi fagosom dan mencegah pembentukan fagolisosom. Dengan proses ini, alih-alih mati dibunuh oleh makrofag, MTB malah mendapat tempat untuk bereplikasi atau berkembang biak.
Cara MTB menghambat pembentukan fagolisosom diantaranya adalah dengan menghambat sinyal Ca2+ dan menghambat rekrutmen serta penyusunan protein yang memediasi fusi antara lisosom dengan fagosom. Oleh sebab itu, pada tahap awal ini yaitu dalam waktu tiga minggu pertama, MTB berproliferasi di makrofag alveolar paru.
Bersamaan dengan proses proliferasi ini kemudian terjadi bakterimia dan penyebaran bakteri ke berbagai tempat. Walaupun terjadi bakterimia, penderita pada fase ini kebanyakan tidak bergejala atau sakit ringan seperti flu.

Terjadinya Reaksi Imunitas Terhadap MTB
Setelah proliferasi, sistem imunitas mulai bereaksi. Diawali dengan dikenalinya pola molekuler patogen MTB seperti lipoprotein dan glikolipid (gambar bawah) oleh sistem innate immunity termasuk Toll-like receptor misalnya TLR2. Reaksi ini memprakarsai terjadinya respon imunitas adaptif terhadap MTB.

Respon adaptif dimulai sekitar 3 minggu setelah bakteri masuk. Proses ini terjadi saat antigen MTB masuk ke saluran getah bening dan bertemu sel APC (misal sel dendritik). APC ini kemudian mengeluarkan IL-12 yang kemudian memicu maturasi sel T-helper 1 (TH1). Sel limfosit ini mendekati makrofag dan mengaktivasi makrofag sehingga bersifat bakterisidal.
TH1 yang aktif kemudian akan memproduksi interferon-γ (IFN-γ). IFN-γ akan diterima oleh makrofag sehingga makrofag akan diaktivasi. Makrofag yang diaktivasi TH1 kemudian akan membunuh MTB baik di paru maupun di kelenjar getah bening.
Caranya adalah pertama, IFN-γ menstimulai maturasi fagolisosom pada makrofag yang mengandung MTB. Hal ini menyebabkan MTB dalam makrofag akan dipaparkan dengan lingkungan asam dan kaya oksidan yang mematikan bagi bakteri.
Kedua, IFN-γ juga menginduksi ekspresi NO sintase yang menghasilkan NO. Gabungan NO dengan oksidan lain akan menghasilkan intermediet nitrogen reaktif yang akan menghancurkan bakteri.
Ketiga, IFN-γ akan memobilisasi peptida antimikrobial defensins untuk melawan bakteri MTB. Terakhir, IFN-γ menstimulasi autofagi, sebuah proses yang mengsekuester dan menghancurkan organel makrofag yang rusak serta bakteri intraseluler yang berada dalam sel makrofag, termasuk MTB.
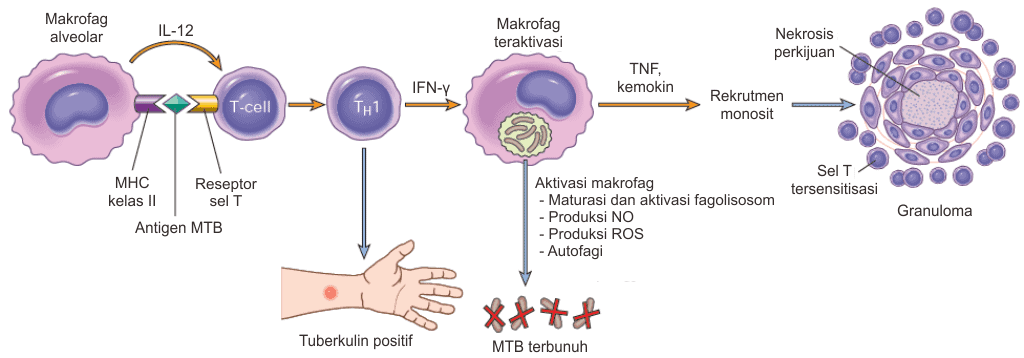
Pembentukan Granuloma
Disamping mengaktivasi makrofag, TH1 juga menyebabkan terbentuknya granuloma dan nekrosis kaseosa atau nekrosis perkijuan. Makrofag yang teraktivasi akan berdiferensiasi menjadi histiosit epiteloid yang bergabung satu sama lain membentuk granuloma. Beberapa makrofag bergabung menjadi sel raksasa yang bernama sel datia Langhans.
Pada banyak kasus, reaksi ini dapat menghentikan progresi penyakit. Namun, pada keadaan imunodefisiensi misalnya pada usia lanjut atau AIDS, proses infeksi dapat berlanjut dan reaksi imun kemudian akan membentuk nekrosis perkijuan. Makrofag yang teraktifasi akan menghasilan TNF dan kemokin yang akan mengundang lebih banyak lagi makrofag ke tempat terjadinya infeksi. Pentingnya TNF ini terlihat dimana pada pasien dengan rheumatoid arthritis yang mendapat terapi anti-TNF memiliki peningkatan risiko untuk reaktivasi tuberkulosis.
Selain TH1, sel lain yang berperan dalam reaksi imun terhadap MTB seperti sel NKT (natural killer T lymphocyte) yan mengenali antigen lipid mikobakterial yang terikat dengan CD1 pada sel APC. Sel T lain yang mengekspresikan reseptor sel T-γδ juga berperan dengan memproduksi IFN-γ.

Proses MTB Lolos dari Sistem Imun
MTB bertahan dan berkembang biak di dalam makrofag menyebabkan infeksi kronik yang persisten. Hal ini dicapai dengan menghentikan proses pembentukan fagolisosom sehingga mencegah pembentukan lingkungan intraseluler yang berbahaya, mencegah mekanisme efektor sel makrofag, dan melindungi MTB dari jalur pemrosesan antigen.
Salah satu ciri dari maturasi fagolisosom adalah asidifikasi dari lumen fagosom (pH 5,0 ke bawah). Lingkungan asam akan menghambat aktivitas bakteri, mengoptimasi aktivitas dari hidrolisis protease dan meyakinkan terjadinya mobilisasi vesikel untuk terjadinya fusi antara fagosom dengan lisosom. Fusi ini akan menyebabkan antigen yang ada di fagosom akan didegradasi menjadi komponen antigen untuk diolah dan dipresentasikan oleh APC di MHC kelas II sehingga terjadi respon imun yang dimediasi oleh sel. Asidifikasi ini dicapai dengan rekruitmen V-ATP-ase ke fagosom yang akan memompa ion hidrogen ke fagosom.
Fagosom yang di dalamnya terdapat MTB hanya mampu melakukan asidifikasi sampai pH 6,4 sehingga gagal untuk berfusi dengan lisosom. Hal ini dicapai karena MTB mencegah kerja V-ATP-ase melalui kerja protein tirosin fosfatase PtpA yang dimiliki bakteri. Protein ini menempek ke subunit H dari V-ATP-ase, menghambat mobilisasi fagosom untuk berfusi dengan lisosom.
Penghentian fusi fagosom yang terdapat MTB dengan lisosom juga terjadi akrena kegagalan konversi Rab5 endosomal menjadi Rab7. Konversi Rab terjadi melalui jalur calcium/calmodulin/calmodulin kinase II-dependent phosphatidylinositol-3-kinase (PI3K)/phosphatidylinositol-3-phosphate (PI3P). Kaskade ini memediasi rekrutmen dari efektor Rab5 yaitu early endosomal antigen 1 (EEA1) yang berperan dalam fusi fagosom-lisosom.
Beberapa produk bakteri yang menghambat kaskade ini misalnya LAM yang mengganggu fluks kalsium. Protein lain ManLam menghambat rekrutmen PI3K oleh calcium/calmodulin sehingga mencegah pembentukan PIP3 dan rekrutmen EEA1. Fosfatase PI3P bakteri, SapM akan mendegradasi PI3P yang lolos dari blokade ManLam sehingga efek kombinasi ini akan menghambat pembentukan fagolisosom.
Dengan terjadinya pencegahan pembentukan fagolisosom ini, bakteri dapat hidup dan berkembang di dalam makrofag. Selain itu, pencegahan fagolisosom juga mencegah pemrosesan antigen oleh makrofag. Akibatnya, hal ini akan mengurangi presentasi dan rekognisi antigen bakteri oleh sel T, menunda perkembangan reaksi imunitas adaptif terhadap MTB.
Faktor Kerentanan Genetik
Beberapa individu memiliki kerentan terhadap infeksi MTB. Individu tersebut diantaranya yang memiliki pola genetik yang menyebabkan defisiensi jalur IL-12 dan IFN-γ.
Individu yang mengalami defisiensi STAT1 juga rentan terhadap infeksi TB. STAT1 adalah sinyal transduser dari IFN-γ. Selain rentan terinfeksi, orang dengan defisiensi sinyal STAT1 juga lebih berisiko mengalami infeksi mikobakteri yang berat.
Faktor genetik lain yang berkaitan dengan kerentanan infeksi TB adalah polimorfisme pada berbagai gen seperti HLA, IFN-γ, reseptor IFN-γ, dan TLR2. Namun, kontribusi polimorfisme ini kepada perjalanan penyakit tuberkulosis masih diteliti lebih lanjut.
Sebenarnya masih belum jelas bagaimana alasan seseorang mengalami progresi dari infeksi laten menjadi infeksi aktif. Beberapa penelitian memperlihatkan bahwa pada orang yang mengalami progresi, pada neutrofil orang tersebut terdapat peningkatan ekspresi sekelompok gen yang disebabkan oleh interferon tipe I dan II. Tingkat ekspresi gen ini berkaitan dengan luasnya keterlibatan paru secara radiologis.
Hal ini menunjukan bahwa respon interferon berperan dalam reaktivasi penyakit tuberkulosis. Namun, walaupun sebagian penderita TB laten tidak memiliki pola peningkatan gen ini, tapi 10-20% orang dengan TB laten mengalami peningkatan ekspresi gen-gen yang terkait interferon.
Tuberkulosis Primer
Secara klinis tuberkulosis terbagi menjadi penyakit primer yang terjadi pada infeksi orang non imun atau dalam kata lain pada orang yang pertama kali terinfeksi dan penyakit sekunder pada orang yang sudah terbentuk imunitas terhadap MTB.
Pada tuberkulosis primer, gejala signifikan terjadi pada 5% dari semua tuberkulosis primer. Gejala berat berupa tuberkulosis primer progresif memiliki gambaran klinis mirip pneumonia bakteri akut yaitu adanya konsolidasi lobus paru, adenopati hilar, dan efusi pleura. Diseminasi limfohematogenik mengikuti infeksi primer akan menyebabkan meningitis tuberkulosis dan TB milier.
Fokus awal dari infeksi primer adalah di paru. Kuman terbawa sampai ke saluran napas distal bagian bawah lobus atas paru yang umumnya dekat ke pleura. Ketika muncul sensitisasi, muncul konsolidasi peradangan dengan ukuran 1 – 1,5 cm berwarna abu-abu yang dikenal dengan fokus Ghon.
Dari fokus Ghon ini, bakteri terbawa ke saluran getah bening regional, menimbulkan peradangan dan membentuk nekrosis perkijuan. Gabungan dari lesi parenkim paru ditambah keterlibatan nodal getah bening ini dinamakan kompleks Ghon.
Pada 95% kasus, saat imunitas adaptif terbentuk, kompleks Ghon akan mengalami fibrosis ekstensif yang secara radiologis terdeteksi sebagai kalsifikasi dan dinamakan kompleks Ranke.
Tuberkulosis Sekunder/Reaktivasi/TB Pascaprimer
Pada tuberkulosis sekunder, gambaran klasik tempat lesi adalah di apeks dari lobus atas paru. Dikarenakan sudah ada imunitas, maka terjadi reaksi radang yang lebih jelas dengan reaksi jaringan yang cenderung membentuk batas dinding yang mengelilingi lesi infeksi. Dalam keadaan ini, keterlibatan getah bening relatif kurang dibandingkan dengan pada infeksi primer.
Di sisi lain, pembentukan kavitasi pada tuberkulosis sekunder lebih kentara dan hampir selalu terbentuk. Erosi kavitas yang diikuti terbentuknya hubungan antara kavitas dengan saluran napas menjadi sumber penting penyebaran infeksi dari tuberkulosis.

Manifestasi Klinis
Tuberkulosis merupakan penyakit yang paling banyak mengenai paru namun dapat menginfeksi berbagai organ atau bagian dari tubuh yang lain (kecuali rambut atau kuku). Secara umum berdasarkan tempat infeksinya, tuberkukosis dapat terbagi menjadi tuberkulosis paru dan ekstraparu.
Sebelum munculnya epidemi HIV, sebagaian besar atau 80% kasus merupakan tuberkulosis paru saja. Adapun pada penderita HIV, dua pertiga kasus menderita tuberkulosis paru dan ekstraparu sekaligus atau hanya ekstraparu saja. Jadi, pada orang yang mengalami penurunan imunitas, jenis tuberkulosis paru murni justru menjadi minoritas.
Untuk gejala sendiri terdapat gejala sistemik dan gejala yang tergantung dari organ yang terkena/terinfeksi MTB. Gejala sistemik infeksi MTB adalah sebagai berikut:
- Malaise/badan merasa lemas
- Berat badan turun
- Nafsu makan turun
- Demam
- Menggigil
- Berkeringat di malam hari.
Adapun gejala berdasarkan per organ adalah sebagai berikut:
Tuberkulosis Paru
TB paru merupakan bentuk klinis tuberkulosis yang paling banyak ditemui. Gambaran klinis TB paru terbagi menjadi dua yaitu TB paru primer dan TB paru pascaprimer/posprimer. Gejala TB paru umumnya dapat berupa salah satu atau beberapa gejala sebagai berikut:
- Batuk
- Batuk berdahak
- Batuk berdahak dengan darah (hemoptisis)
- Nyeri dada
- Sesak napas
Selain gejala di atas, disertai pula dengan gejala sistemik yang telah disebutkan di atas. Namun, tidak semua TB paru menimbulkan batuk. Hal ini terutama tergantung apakah jenis TB paru primer atau pascaprimer.
TB Paru Primer
TB paru primer berasal dari proses infeksi MTB untuk pertama kalinya. Di daerah dengan prevalensi tinggi TB seperti Indonesia, TB paru primer sering ditemukan pada anak-anak dengan lesi biasanya berupa konsolidasi lobus tengah atau bawah dan kadang bisa disertai efusi dan kavitasi.

Lesi yang muncul pada TB paru primer setelah infeksi umunya berada di area perifer dan disertai dengan limfadeonpati hilar atau paratrakheal. Limfaedonpati ini dapat tidak terlihat pada foto toraks. Pada kebanyakan kasus, lesi ini akan sembuh secara spontan dan dapat tampak nantinya sebagai lesi nodul kecl dengan kalsifikasi (lesi Ghon).

TB paru primer pada anak dan individu yang imunokompromais dapat memiliki perjalanan klinis yang cepat. Lesi awal dapat bertambah besar dan berkembang menjadi beberapa cara. Apabila lesi ini kemudian mempenetrasi atau menembus selaput pleura dan masuk ke rongga pelura maka akan menimbulkan efusi pleura. Efusi pleura merupakan salah satu yang sering ditemukan sebagai bentuk gambaran TB paru primer.
Pada kasus yang berat, lesi primer akan bertambah besar secara cepat dan bagian tengahnya nekrosis dan muncul kavitas akut. Pada anak, TB paru primer hampir selalu disertai pembesaran KGB hilar atau mediastinal. Pembesaran KGB ini dapat menyempitkan saluran bronkhus sehingga bisa menyebabkan atelektasis. Obstruksi parsial juga bisa menyebabkan gambaran emfisema dan juga bisa menyebabkan gambaran bronkiektasis.
TB Paru Pascaprimer
Bentuk ini merupakan yang paling banyak ditemukan pada populasi dewasa. Disebut juga TB reaktivasi atau TB sekunder. TB paru pascaprimer berasal dari reaktivasi endogen infeksi laten dan biasanya berlokasi di daerah apeks dan segmen posterior dari lobus atas dimana konsenterasi oksigen tinggi menguntungkan pertumbuhan kuman MTB. Sebagai tambahan, segmen superior dari lobus paru bawah juga kadang terlibat. Keterlibatan parenkim paru bervariasi mulai dari infiltrat kecil sampai munculnya kavitas yang besar.
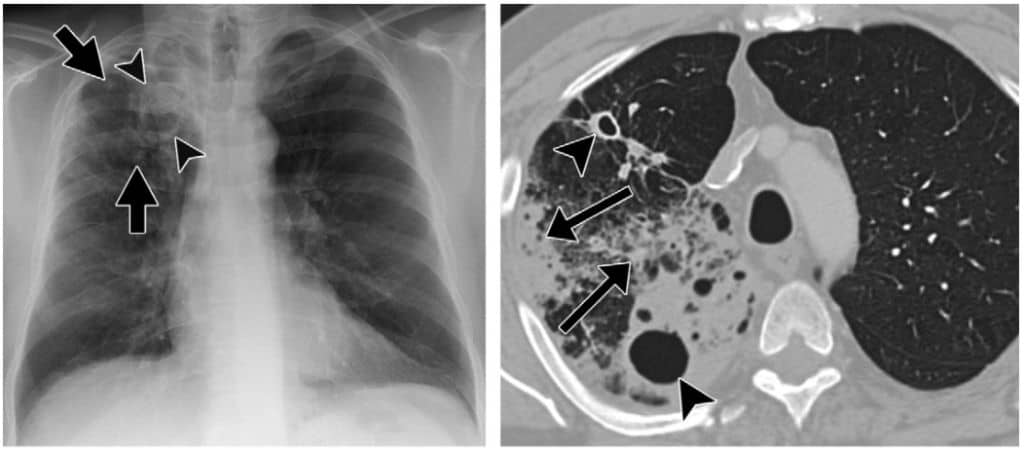
Adanya keterlibatan massif dari segmen atau lobus paru yang bergabung menjadi satu lesi akan menyebabkan pneumonia tuberkulosa. Sepertiga penderita akan jatuh ke dalam TB paru berat dalam hitungan minggu hingga bulan sedangkan sisanya dapat sembuh atau menjadi kondisi kronik (dahulu dikenal sebagai “penyakit konsumsi”). Dalam keadaan ini, lesi akan menjadi parut fibrotik dengan kalsifikasi dan kavitas tetap tersisa di bagian paru yang lain.
Di awal perjalanan penyakit, gejala dan tanda sering kali tidak spesifik dan berupa keringat malam dan demam, penurunan berat badan, anoreksia, malaise, dan lemas. Namun, pada kebanyakan kasus sudah muncul batuk yang awalnya tidak berdahak yang kemudian berubah menjadi batuk berdahak yang kadang disertai dengan darah (hemoptisis).
Hemoptisi massif atau berat terjadi akibat erosi pembuluh darah besar pada dinding kavitas. Hemoptisis juga dapat terjadi akibat ruptur pembuluh darah yang berdilatasi (aneurisma Rasmussen) di dalam kavitas atau karena munculnya tuberkuloma pada kavitas yang lama.
Nyeri dada terjadi karena lesi yang dekat dengan pleura (subpelura) namun bisa juga akibat otot dada yang tertarik akibat batuk yang terus-menerus. Penyakit TB paru yang luas akan menyebabkan gangguan pernapasan sehingga muncul sesak napas dan bahkan ARDS.
Pada pemeriksaan fisik kadang terbatas namun sering kali di jumpai rhonki basah kasar karena obstruksi bronkhi serta pada cavitas dapat dijumpai suara khas berupa suara napas amforik (seperti meniup di atas lubang botol). Dapat pula disertai clubbing finger. Pemeriksaan penunjang dapat dijumpai leukositosis dan anemia ringan. Selain itu, kadang dijumpai hiponatremia akibat SIADH.
Tuberkulosis Ekstraparu
Seperti disebutkan sebelumnya bahwa MTB dapat menginfeksi semua organ. Infeksi MTB di luar dari organ paru disebut TB ekstraparu. Urutan TB ekstraparu yang paling banyak ditemui adalah TB kelenjar getah bening atau limfadenopati TB, pleuritis TB, TB saluran kemih, TB tulang dan sendi, meningitis TB, peritonitis TB, dan perikarditis TB. Saat ini, dengan endemi HIV, tuberkulosis ekstraparu semakin banyak dijumpai.
Limfadenitis TB
Limfadenitis TB meliputi sekitar 25% kasus TB ekstraparu dan banyak dijumpai pada penderita HIV. Wanita dan anak-anak juga banyak yang terkena. Dahulu, mayoritas kasus linfadenitis TB disebabkan oleh M. bovis namun sekarang MTB menjadi etiologi yang predominan.
Kelenjar getah bening yang terkena biasanya membengkak tidak nyeri dan kebanyakan mengenai regio leher dan supraklavikula (kondisi yang disebut skrofula). Awalnya KGB yang terindeksi hanya berupa nodul di bawah kulit yang kenyal namun dapat membentuk fistel dan supurasi pada kulit.
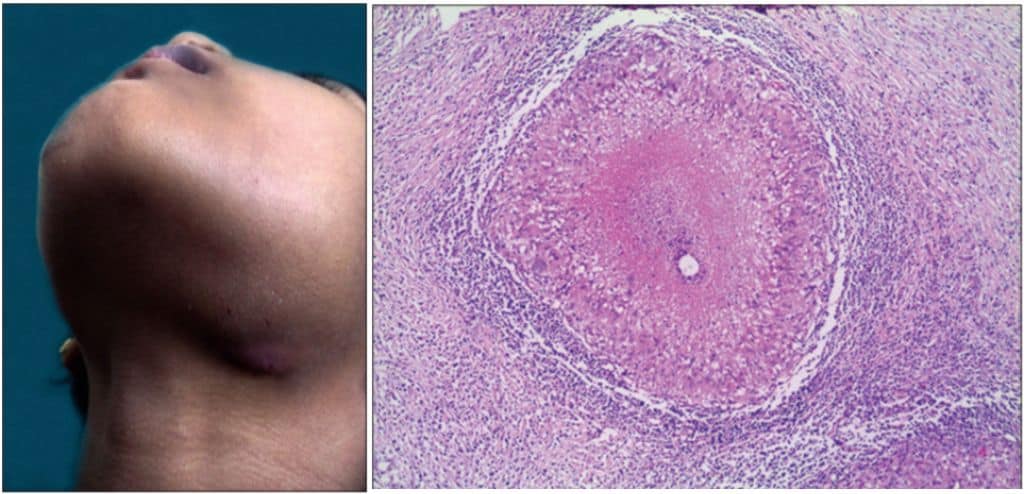
Gejala sistemik TB umumnya dominan dijumpai pada penderita limfadenitis TB yang terkena HIV. Diagnosis dilakukan dengan pemeriksaan FNAB atau biopsi aspirasi jarum halus (BAJAH) atau bisa juga dengan eksisi KGB. Pada pemeriksaan histopatologi akan dijumpai granuloma walaupun pada penderita HIV granuloma ini bisa tidak ditemukan. Adapun diagnosis diferensialnya yaitu limfoma atau massa metastasis dari suatu keganasan.
Pleuritis TB
Pada pleuritis TB, dapat muncul menyertai baik TB paru primer maupun reaktivasi. Kondisi ini bisa muncul saat granuloma pecah dan isinya masuk ke ruang kavitas dan menyebabkan inflamasi lokal. Jika didapatkan efusi disertai efusi perikardial atau peritoneal dinamakan tuberculous polyserositis.
Tergantung dari derajat reaktivitas, efusi dapat sedikit, tidak terdeteksi, dan kemudian dapat menghilang. Dalam kondisi sebaliknya, efusi dapat besar dan menyebabkan gejala seperti demam, sesak, dan nyeri dada pleuritik. Pemeriksaan fisik pada kondisi dapat dijumpai hilangnya suara napas dan pekak saat perkusi di sisi paru yang terkena. Pada pemeriksaan rontgen toraks didapatkan gambaran efusi dengan sepertiga kasus juga memperlihatkan lesi di parenkim paru.

Torakosentesis diperlukan untuk memeriksa lebih lanjut cairan efusi. Warna cairan pleura pada pleuritis TB berwarna seperti jerami kadang hemoragik, bersifat eksudat dengan protein cairan >50% protein serum, konsenterasi glukosa cairan normal atau rendah, pH cairan <7,2, dan terdapat kenaikan leukosit pada cairan (250 – 2500 /μL). Di awal tahapan penyakit predominan neutrofil sedangkan pada pleuritis yang sudah agak lama predominan mononuklear.
Sel mesotel biasanya tidak dijumpai pada cairan pleura. Adapun pulasan BTA seringkali negatif namun biakan lebih sering positif. Kadang diperlukan biopsi dari pleura yang memperlihatkan granuloma dan biakan jaringan dapat positif sampai pada 70%.
Empiema TB lebih jarang dijumpai dan biasanya disebabkan oleh ruptur kavitas ke rongga pleura atau dari fistel dari lesi bronkhiolar. Pada radiogtafi dijumpai piopneumotoraks dengan air-fluid level. BTA lebih banyak positif dengan jumlah kuman yang banyak. Cairan pleura kental, purulen, dan banyak mengandung limfosit. Biasanya harus disertai dengan drainase bedah selain OAT untuk penanganan emiema RB. Seringkali empiema TB diikuti dengan sequelae fibrosis pleura berat dan penyakit paru restriktif.
Tuberkulosis Saluran Napas Atas
TB pada saluran napas atas biasanya merupakan komplikasi dari TB paru dengan kavitas. Saluran napas atas yang terkena bisa berupa larynx, pharynx, dan epiglotis. Gejalanya bisa berupa serak dan sulit menelan (disfagia) serta tambahannya adalah batuk kronik. Adapun lesi sesuai dengan lokasi tempat terkena dan pada laringoskopi dapat dijumpai adanya tukak atau ulkus. Pemeriksaan BTA biasanya positif namun tetap diperlukan biopsi untuk menegakan diagnosis. Lesi keganasan bisa serupa dengan lesi TB namum pada keganasan biasanya tidak disertai gejala nyeri (painless).
TB Organ Urogenital
TB saluran kemih meliputi sekitar 15% kasus TB ekstraparu. Dapat mengenai bagian mana saja dan merupakan konsekuensi dari penyebaran hematogenik dari TB primer. Gejala lokal biasanya predominan seperti frekuensi, disuria, hematuria, dan nyeri pinggang. Seringkali asimtomatik dan diketahui setelah muncul lesi destruktif ginjal.
Urinalisis seringkali abnormal pada 90% kasus dimana dijumpai piuria dan hematuria. Adanya piuria dengan biakan negatif dan urin yang asam mengarah pada kecurihaan TB saluran kemih. Untuk membantu diagnosis dapat dilakukan pielogram IV. Lesi kalsifikasi dan striktur uretra sugestif ke arah TB saluran kemih. Biakan spesimen urin pagi merupakan diagnostik definitif dari TB saluran kemih. Jika terjadi striktur berat dapat mengakibatkan hidronefrosis dan kerusakan ginjal.
Tuberkulosis genital lebih sering dijumpai pada wanita dibandingkan pria. Pada wanita, biasanya mengenai tuna falopii dan endometrium sehingga bisa menyebabkan gangguan kesuburan, nyeri panggul/pelvis, dan gangguan menstruasi. Diagnosis memerlukan biopsi dan biakan spesimen dari dilatasi dan kuretase.
Pada pria, TB mengenai epididimis sehingga menimbulkan massa yang nyeri jika ditekan dan dapat menimbulkan fistel ke kulit. Orchitis dan prostatitis juga dapat terjadi karena TB. Pada setengah kasus TB genital juga dijumpai TB saluran kemih secara bersamaan.
TB Tulang, Sendi, dan Spondilitis Tuberkulosa
TB tulang dan sendi meliputi sekitar 10% kasus TB ekstraparu di Amerika Serikat. Kondisi ini disebabkan oleh reaktivasi foci hematogenik atau dari penyebaran perkontinuitatum KGB paravertebra. Sendi weight-bearing (spinal, panggul, dan lutut) sering kali terkena. Tuberkulosis spinal atau nama lainnya pernyakit Pott atau spondilitis TB sering melibatkan dua atau lebih segmen vertebra yang berdekatan.
Spinal torakal atas merupakan tempat yang sering terkena pada kasus anak sedangkan pada dewasa paling banyak mengenai spinal torakal bagian bawah.dari angulus anterior superior atau inferior dari badan vertebra, lesi akan mencapai badan vertebra yang berdekatan dan disertai dengan proses perusakan diskus intervertebralis. Pada penyakit spondilitis TB yang lanjut kolapsnya badan vertebra akan menyebabkan kiposis (gibbus). “Abses dingin” paravertebra juga dapat terbentuk. Pada spinal atas, abses ini dapat menyebar ke dinding dada sebagai massa sedangkan di spinal bagian bawah dapat menyebar ke ligamentum inguinalis atau muncul sebagai abses psoas.
Pemeriksaan CT-scan atau MRI dapat memperlihatkan ciri lesi yang cukup khas dan dapat mengarahkan diagnostik spondilitis TB. Adapun diagnosis banding dari lesi TB ini adalah infeksi lain dan tumor. Untuk konfirmasi diagnosis dapat dilakukan dengan aspirasi abses atau biopsi tulang. Biakan biasanya positif dan karakter histopatologi juga cukup khas.

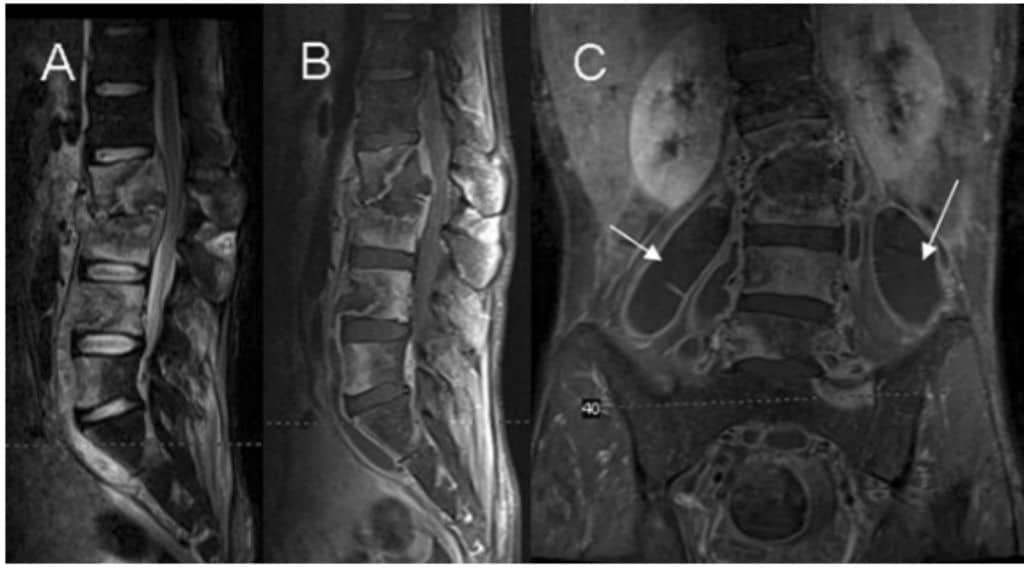
Komplikasi yang berat dari penyakit Pott adalah paraplegia yang terjadi ketika abses atau lesi menekan medulla spinalis. Paraplegia Pott ini memiliki lima stadium
- Stadium 1: defisit muncul hanya pada pemeriksaan seperti adanya klonus, refleks tendon meningkat, atau refleks Babinski positif
- Stadium 2: pada pasien terdapat defisit motorik tipe UMN dengan spastisitas namun masih bisa menjalani aktivitas mandiri. Defisit sensoris terjadi melibatkan kolumna lateralis
- Stadium 3: pasien tirah baring dan spastis. Defisit sensoris terjadi melibatkan kolumna lateralis
- Stadium 4: pasien tirah baring dengan defisit sensoris berat dan adanya ulkus dekubitus. Defisit sensoris terjadi melibatkan kolumna lateralis dan posterior.
- Stadium 5: sama dengan stadium 4 ditambah gangguan berkemih atau buang air besar, dapat disertai spasme fleksor atau paraplegia/tetraplegia flasid
Jika terjadi paraparesis akibat abses besar merupakan kondisi emergensi yang memerlukan drainase abses. Tuberkulosis pada sendi panggul menimbulkan nyeri dan gangguan mobilisasi sedangkan TB lutut menyebabkan nyeri dan bengkak dan seringkali didahului oleh trauma. Jika tidak diobati maka sendi akan rusak. Bisanya TB sendi dan tulang berespon dengan OAT namun pada kasus berat seringkali harus dibantu dengan terapi bedah.
Meningoensefalitis TB dan Tuberkuloma
Meningitis TB terjadi meliputi 5% kasus TB ekstraparu dan biasanya terjadi pada anak-anak dan juga dewasa yang terkena HIV. Kondisi dapat terjadi akibat penyebaran hematogenik kuman TB dari penyakit TB primer maupun pascaprimer. Dapat pula terjadi karena ruptur tuberkel subependimal ke ruang subarachnoid. Pada lebih dari setengah kasus, lesi paru lama dapat terlihat pada pemeriksaan foto toraks.
Gambaran penyakit dapat berupa gejala ringan seperti nyeri kepala dan perubahan kondisi mental atau dapat pula muncul secara akut seperti kebingungan, letargi, gangguan sensorik, dan kaku kuduk. Biasanya penyakit berkembang dalam 1-2 minggu yang umumnya lebih lama dibandingkan meningitis bakterialis. Paresis nervus kranialis terutama nervus okular sering didapat dan adanya keterlibatan arteri serebralis dapat memunculkan gejala iskemia fokal. Selain itu dapat pula terjadi hidrosefalus.
Untuk menegakan diagnosis pemeriksaan pungsi lumbal memegang peranan penting. Lumbal pungsi bertujuan untuk mendapatkan cairan serebrospinalis (CSF). Pada pemeriksaan cairan tersebut biasanya didapatkan hitung leukosit tinggi (predominan limfosit namun dapat predominan neutrofil pada awal penyakit). Jumlah protein juga meningkat 100-800 mg/dL disertai dengan konsenterasi glukosa cairan yang rendah. Akan tetapi, parameter-parameter tadi bisa saja normal.
Pemeriksan BTA hanya positif dari 20% sampel sedimen CSF namun dengan pengambilan pungsi berulang dapat meningkat hasil positif pemeriksaan BTA tersebut. Adapun pemeriksaan biakan dari CSF hasil positifnya dapat sampai 80%.
Pada pemeriksaan CT-scan atau MRI dapat tampak adanya hidrosefalus dan penyangatan ependima atau sisterna. Jika tidak tediagnosis, meningitis TB umumnya fatal. Biasanya dapat berespon terhadap OAT tetapi pada 25% kasus dapat terjadi gejala sisa atau sequelae terutama apabila terjadi keterlambatan diagnosis. Pemberian steroid dapat membantu mempercepat perbaikan abnormalitas CSF, percepatan penururnan tekanan intrakranial, menurunkan mortalitas, dan menurunkan sequalae dari meningitis TB.
Tuberkuloma merupakan gambaran jarang dari tuberkulosis. Lesinya berupa lesi desak ruang intrakranial dan biasa menyebabkan kejang dan defisit neurologis fokal. CT-scan dan MRI dapat memperlihatkan gambaran contrast-enhanced ring lesion namun umumnya perlu dilakukan pemeriksaan biopsi sebagai konfirmasi.
Tuberkulosis Gastrointestinal
Setiap bagian dari saluran cerna dapat terinfeksi oleh kuman MTB. Mekanisme jalur infeksi MTB pada saluran cerna dapat berupa tertelannya kuman secara langsung, penyebaran secara hematogenik, dan mengonsumsi susu sapi yang tercemar M. bovis. Bagian yang sering menjadi tempat infeksi adalah ileum terminal dan caecum.
Gejala yang sering didapatkan adalah nyeri perut yang sering kali mirip dengan gejala apendisitis akut, diare, obstruksi/ileus, hematokskezia, dan teraba massa di abdomen. Gejala sistemik seperti demam, berat badan turun, dan keringat malam sering dijumpai.
Apabila ada lesi dengan keterlibatan mukosa atau dinding usus, ulkus yang timbul serta fistulasi dapat mirip menyerupai penyakit Crohn. Ditemukannya fistel anal harus disertai pemeriksaan ke arah TB rektal. Sering kali dalam penanganannya diperlukan pembedahan dan umumnya diagnosis TB saluran cerna dilakukan dengan memeriksa sampel hasil biopsi jaringan dan/atau biakan dari jaringan tersebut.


Peritonitis TB terjadi baik sebagai akibat penyebaran hematogenik maupun dari rupturnya tuberkel KGB maupun organ intraabdomen. Gejala yang terjadi adalah nyeri perut yang tidak spesifik, demam, dan terjadinya asites. Keberadaan peritonitis TB dengan sirosis cukup menyulitkan dalam dilakukannya diagnosis.
Cairan asites pada peritonitis TB memperlihatkan sifat cairan eksudat dengan kandungan protein tinggi dan leukosit (predominan linfosit namun dapat pula neutrofil). Hasil BTA dan biakan dari cairan asites biasanya rendah dan pengambilan sampel dengan volume besar dapat membantu meningkatkan hasil BTA dan biakan. Akan tetapi, sering kali diperlukan biopsi melalui peritonoskopi untuk menegakan diagnosis TB. Metode lain dalam diagnosis adalah dengan mengukur kadar ADA cairan asites.
Perikarditis TB
Masuknya kuman TB ke rongga perikardial terjadi akibat progresi fokus primer di perikardium dan dapat pula akibat reaktivasi fokus laten atau rupturnya KGB yang berdekatan. Biasanya perikarditis TB terjadi pada populasi lansia di negara maju namun meningkat di usia muda terutama pada populasi dengan HIV.
Tingkat fatalitas akibat perikarditis TB dapat mencapai 40%. Onset gejala biasanya subakut dan dapat akut disertai dengan gejala demam, nyeri tumpul retrosternal, dan friction rub. Efusi perikadial kemudian muncul pada kebanyakan kasus dan bila cukup besar dapat muncul gejala-gejala tamponade jantung. Selain itu, perikarditis TB juga dapat pula terjadi perikarditis restriktif.
Pada kondisi dimana efusi perikardia terdeteksi oleh foto toraks, maka perikarditis TB harus menjadi salah satu diagnosis banding khususnya pada pasien risiko TB tinggi (HIV positif, lansia, berasal dari wilayah dengan prevalensi TB tinggi). Tanda lain yang mengarah ke perikarditis TB adalah apabila pada ekhokardiografi tampak gambaran seperti benang kasar di ruang perikardium.
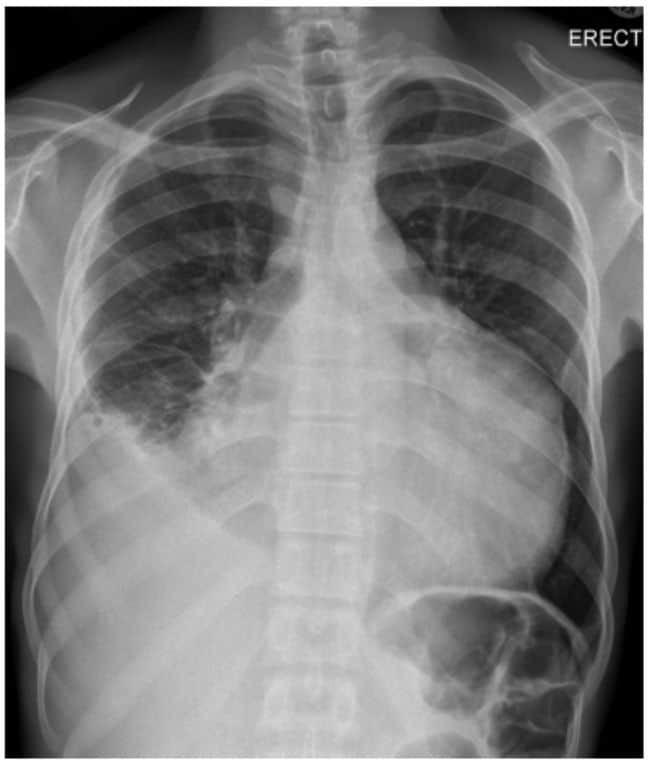

Untuk menegakan diagnosis diperlukan pengambilan cairan perikardia dengan pungsi dibantu ekhokardiografi. Cairan yang diambil kemudian dianalisa secara mirobiologi, analisa sitologi, dan biokimia. Pada perikarditis TB cairan perikardia yang didapat bersifat eksudat dengan kenaikan leukosit predominan sel mononuklear. Selain itu, dapat pula disertai dengan cairan hemoragik.
Pemeriksaan biakan kuman hanya 30% yang positif sehingga kadang harus dibantu dengan pemeriksaan biopsi jaringan untuk menegakan diagnosis. Tingginya kadar ADA (adenosine deaminase) dan IFN-γ pada cairan perikardia dapat mengarahkan ke diagnosis perikarditis TB.
Tanpa pengobatan, perikarditis TB memiliki tingkat fatalitas tinggi. Walaupun dengan pengobatan pun sering kali terjadi sequalae berupa perikarditis konstriktif kronik akibat penebalan selaput perikardium akibat fibrosis dan kalsifikasi.
Pada kasus perikarditis TB, selain OAT juga dianjurkan pemberian kortikosteroid. Namun, dalam penelitian terakhir diungkapkan bahwa pemberian kortikosteroid pada perikarditis TB hanya untuk kelompok pasien dengan risiko komplikasi inflamasi dan risiko perikarditis konstriktif yang tinggi.
Tuberkulosis Diseminata dan TB Milier
Penyebaran secara hematogenik (melalui peredaran darah) sering terjadi. Proses ini bisa tidak bergejala namun dapat pula berubah mejadi bentuk TB paru primer yang paling berat. Penyebaran hematogen yang paling khas adalah TB milier. TB milier merupakan penyebaran akut bakteri MTB secara hematogen yang biasanya didapat pada individu dengan imunosupresi, DM, alkoholisme, lansia, atau malnutrisi. Pada TB milier, didapat gejala konstitusional (demam, keringat malam, dan penurunan berat badan) yang signifikan. Pada pencitraan ditemukan lesi kecil menyebar (2-4 mm) yang merata di paru.

Penyebaran secara hematogen juga menyebabkan kuman MTB bisa berdiseminasi ke berbagai organ dan membentuk lesi granuloma di organ tersebut. Jika organ yang terkena adalah susunan saraf pusat, maka terjadi meningoensefalitis TB. Pada individu yang asimtomatik, lesi di berbagai organ ini bisa sembuh sendiri namun individu tersebut masuk ke fase penyakit TB laten.
Gejala klinis dari TB milier atau diseminata tidak spesifik dan tergantung dari organ yang terkena. Seperti disebutkan di atas, predominan muncul gejala demam, keringat malam, dan penurunan berat badan. Akibat keterlibatan paru terdapat pula batuk dapat disertai sesak napas. Sering kali muncul gejala gangguan saluran cerna dan pada pemeriksaan fisik bisa didapat hepatomegali, splenomegali, dan limfadenoapti. Pemeriksaan mata dapat memperlihatkan tuberkel di koroid mata (30% kasus) yang merupakan ciri patognomonik TB milier. Meningismus muncul pada <10% kasus.
Pada pemeriksaan penunjang dijumpai gambaran milier sedangkan pemeriksaan BTA negatif pada 80% kasus. Gangguan hematologis yang dapat ditemukan biasanya anemia, leukopenia, leukositosis neutrofilik, reaksi leukemoid, dan bisa pula polisitemia. Pada pasien dengan keterlibatan hati akan dijumpai kenaikan transaminase, alkali fosfatase, dan kelainan tes fungsi hati lainnya. Tes tuberkulinn negatif pada lebih dari setengah kasus namun akan menjadi reaktif saat menjalani terapi OAT.
Manifestasi klinis yang jarang pada lansia dengan sebutan cryptic miliary tuberculosis dimana perjalanan penyakitnya kronik dengan gejala demam intermiten, anemia, dan tanda keterlibatan meningeal sebelum kondisi memburuk dan pasien kemudian meninggal. Bentuk lain berupa setikemia akut nonreactive miliary tuberculosis yang sangat jarang dan terjadi akibat penyebaran kuman secara hematogen yang massif. Pansitopenia merupakan gambaran hematologi yang didapat dan umumnya fatal. Pada otopsi ditemukan lesi nekrotik nongranulomatosa sehingga disebut reaksi nonreaktif.
Tuberkulosis Ekstraparu Lainnya
TB dapat menyebabkan gangguan pada mata berupa korioretinitis, uveitis, panoftalmitis, konjungtivitis phlyctenular terkait gejala hipersensitivitas yang nyeri. Otitis tuberkulosis jarang dan muncul dengan gejala penurunan pendengaran, keluar cairan dari telinga, dan perforasi membran timpani. Di nasopharinx, lesi TB dapat menyerupai granulomatosis Wagener. Manifestasi pada kulit berupa inokulasi langsung yang menyebabkan lesi primer, ulkus kronik, abses, skrofuloderma, lupus vulgaris, lesi miler, dan eritema nodosum.

Tuberkulosis adrenal merupakan manifestasi infeksi TB yang lanjut dan muncul sebagai sindrom insufisiensi adrenal. Pada penyebaran MTB ke plasenta dapat muncul TB kongenital baik disebabkan penyebaran tuberkel lewat plasenta atau tertelan kuman oleh fetus lewat cairan amnion. Kondisi ini jarang dan menyerang hati, limpa, kelenjar getah bening, dan organ lainnya.
Diagnosis Tuberkulosis
Diagnosis TB adalah dengan menemukan bakeri MTB dari sampel tubuh. Adapun sampel yang diambil bisa berupa dahak, aspirasi kelenjar getah bening, cairan pleura, cairan serebrospinal, dan lain sebagainya. Adapun untuk identifikasi terdapat cara konvensional yaitu dengan pemeriksaan tes tahan asam, biakan bakteri, dan tes biokimia. Adapun tes yang terbaru berupa pemeriksaan molekuler dengan PCR.
Pemeriksaan Mikroskopis
Pemeriksaan mikroksopis terutama tes tahan asam merupakan metode yang paling banyak dipakai dalam deteksi MTB. Bakteri akan tewarnai merah oleh fuchsin dengan metode pewarnaan Ziehl-Neelsen.
Pemeriksaan dengan mikroskop fluoresensi atau pewarnaan auramine lebih sensitif dibandingkan Ziehl-Neelsen. Pada pemeriksaan ini bakteri akan terwarnai oleh zat warna luminesen seperti auramine atau rhodamine.

Pemeriksaan Biakan Bakteri
Telah disebutkan sebelumnya bahwa media yang digunakan dapat berupa media agar padat seperti agar Lowenstein-Jensen atau media agar Finn. Kelemahan cara ini adalah lamanya bakteri tumbuh yang dapat mencapai 15 – 60 hari. Cara yang cepat dipakai dengan memakai biakan non konvensional seperti BACTEC yang bisa memberikan hasil dalam 7-8 hari.
Diagnosis Molekuler Tuberkulosis
Deteksi molekuler dengan PCR memungkinkan untuk mendeteksi secara cepat dari MTB. Sebenarnya PCR merupakan cara yang paling efektif dan efisien. Selain mendeteksi adanya bakteri, PCR juga bisa mendeteksi adanya faktor resistensi terhadap obat-obatan, misalnya resistensi terhadap rifampicin atau isoniazid. Saat ini sudah ada cara cepat yang mudah misalnya dengan sistem GeneXpert yang ada di Indonesia yang dapat digunakan sebagai tes cepat diagnosis maupun tes resistensi MTB.
Tes Tuberkulin dan IGRA
Dalam kondisi untuk deteksi infeksi primer pada anak atau TB laten dapat menggunakan tes tuberkulin atau reaksi mantoux atau PPD (purified protein derivative). Caranya adalah dengan menginjeksi secara intrakutan protein tuberkulin dan kemudian melihat adanya indurasi maupun kemerahan di tempat injeksi setelah 24 – 72 jam. Berikut adalah interpretasi dari tes tuberkulin:
| Ukuran indurasi | Pasien yang dianggap tes PPD positif |
|---|---|
| >5 mm | HIV positif atau supresi imun (misal, prednison 15 mg/hari >1 bulan) Kontak erat dengan pasien TB aktif; CXR dengan fibrosis apikal |
| >10 mm | Populasi risiko tinggi atau dengan prevalensi tinggi TB Konversi baru (peningkatan indurasi >10 mm dalam 2 thn terakhit) |
| >15 mm | Semua orang/pasien |
| False negative | Penyuntikan yang salah, anergi (termasuk TB aktif), TN akut (perlu 2-10 minggu konversi), mikobakteria non-TB akut, keganasan |
| False positive | Pembacaan salah, reaksi silang dengan mikobakteria non-TB, vaksinasi BCG (biasanya <10 mm saat dewasa) |
| Efek booster | Peningkatan indurasi karena booster imunologis oleh tes kulit sebelumnya pada pasien yang telah tersensitisasi (oleh TB, mikobakteria non-TB, atau BCG). Tes negatif menjadi positid tapi bukan konversi sebenarnya karena infeksi terdahulu. Dapat berlangsung satu tahun setelah tes awal. |
Salah satu kelemahan tes tuberkulin adalah hasil positif pada pasien yang menerima vaksinasi BCG. Cara lain dengan melihat reaksi hipersensitivitas tipe lambat adalah dengan menggunakan antigen CFP-10 dan ESAT-6. Pada reaksi ini, pasien yang menerima BCG tidak memperlihatkan reaksi sehingga lebih spesifik dalam deteksi infeksi MTB.
Adapun metode diagnosis pemeriksaan darah adalah dengan tes IGRA (interferon-gamma release assay). Limfosit dari darah diambil dan kemudian dibiakan. Kemudian, pada limfosit tersebut diberikan atau dipaparkan antigen spesifik MTB dan kemudian dilihat reaksi pelepasan interferon-γ.
Alur Diagnosis Tuberkulosis
Untuk Indonesia, menurut PNPK Tatalaksana Kasus Tuberkulosis 2019 diagnosis kasus TB mengikuti alut sebagai berikut:

Prinsip Penegakan Diagnosis TB
- Diagnosis TB Paru pada orang dewasa harus ditegakkan terlebih dahulu dengan pemeriksaan bakteriologis. Pemeriksaan bakteriologis yang dimaksud adalah pemeriksaan mikroskopis, tes cepat molekuler TB dan biakan.
- Pemeriksaan TCM digunakan untuk penegakan diagnosis TB, sedangkan pemantauan kemajuan pengobatan tetap dilakukan dengan pemeriksaan mikroskopis.
- Tidak dibenarkan mendiagnosis TB hanya berdasarkan
pemeriksaan foto toraks saja. Foto toraks tidak selalu
memberikan gambaran yang spesifik pada TB paru, sehingga
dapat menyebabkan terjadi over diagnosis ataupun under
diagnosis. - Tidak dibenarkan mendiagnosis TB dengan pemeriksaan
serologis.
Fasilitas Pelayanan Kesehatan (Fasyankes) yang Memiliki TCM
- Fasyankes yang mempunyai akses pemeriksaan TCM, penegakan diagnosis TB pada terduga TB dilakukan dengan pemeriksaan TCM. Pada kondisi dimana pemeriksaan TCM tidak memungkinkan (misalnya alat TCM melampaui kapasitas pemeriksaan, alat TCM mengalami kerusakan, dll.), penegakan diagnosis TB dilakukan dengan pemeriksaan mikroskopis.
- Jika terduga TB adalah kelompok terduga TB RO dan terduga TB dengan HIV positif, harus tetap diupayakan untuk dilakukan penegakan diagnosis TB dengan TCM TB, dengan cara melakukan rujukan ke layanan tes cepat molekuler terdekat, baik dengan cara rujukan pasien atau rujukan contoh uji.
- Jumlah contoh uji dahak yang diperlukan untuk pemeriksaan TCM sebanyak 2 (dua) dengan kualitas yang bagus. Satu contoh uji untuk diperiksa TCM, satu contoh uji untuk disimpan sementara dan akan diperiksa jika diperlukan (misalnya pada hasil indeterminate, pada hasil RIF resisten pada terduga TB yang bukan kriteria terduga TB RO, pada hasil RIF resistan untuk selanjutnya dahak dikirim ke Laboratorium LPA untuk pemeriksaan uji kepekaan lini-2 dengan metode cepat)
- Contoh uji non-dahak yang dapat diperiksa dengan MTB/RIF terdiri atas cairan serebrospinal (cerebro spinal fluid/CSF), jaringan biopsi, bilasan lambung (gastric lavage), dan aspirasi cairan lambung (gastric aspirate).
- Pasien dengan hasil MTB resisten rifampisin tetapi bukan berasal dari kriteria terduga TB-RO harus dilakukan pemeriksaan TCM ulang. Jika terdapat perbedaan hasil, maka hasil pemeriksaan TCM yang terakhir yang menjadi acuan tindakan selanjutnya.
- Jika hasil TCM indeterminate, dilakukan pemeriksaan TCM ulang. Jika hasil tetap sama, berikan pengobatan TB lini 1, lakukan biakan dan uji kepekaan.
- Pengobatan standar TB-MDR segera diberikan kepada semua pasien TB-RR, tanpa menunggu hasil pemeriksaan uji kepekaan OAT lini 1 dan lini 2 keluar. Jika hasil resistensi menunjukkan MDR, lanjutkan pengobatan TB MDR. Bila ada tambahan resistensi terhadap OAT lainnya, pengobatan harus disesuaikan dengan hasil uji kepekaan OAT.
- Pemeriksaan uji kepekaan menggunakan metode LPA (line probe assay) lini-2 atau dengan metode konvensional
- Pengobatan TB pre XDR/ TB XDR menggunakan paduan standar TB pre XDR atau TB XDR atau menggunakan paduan obat baru.
- Pasien dengan hasil TCM MTB negatif, lakukan pemeriksaan foto toraks. Jika gambaran foto toraks mendukung TB dan atas pertimbangan dokter, pasien dapat didiagnosis sebagai pasien TB terkonfirmasi klinis. Jika gambaran foto toraks tidak mendukung TB kemungkinan bukan TB, dicari kemungkinan penyebab lain.
Fasyankes yang Tidak Memiliki TCM
- Fasyankes yang tidak mempunyai alat TCM dan kesulitan mengakses TCM, penegakan diagnosis TB tetap menggunakan mikroskop.
- Jumlah contoh uji dahak untuk pemeriksaan mikroskop sebanyak 2 (dua) dengan kualitas yang bagus. Contoh uji dapat berasal dari dahak sewaktu-sewaktu atau sewaktu-pagi.
- BTA (+) adalah jika salah satu atau kedua contoh uji dahak menunjukkan hasil pemeriksaan BTA positif. Pasien yang menunjukkan hasil BTA (+) pada pemeriksaan dahak pertama, pasien dapat segera ditegakkan sebagai pasien dengan BTA (+)
- BTA (-) adalah jika kedua contoh uji dahak menunjukkan hasil BTA negatif. Apabila pemeriksaan secara mikroskopis hasilnya negatif, maka penegakan diagnosis TB dapat dilakukan secara klinis menggunakan hasil pemeriksaan klinis dan penunjang (setidak-tidaknya pemeriksaan foto toraks) yang sesuai dan ditetapkan oleh dokter.
- Apabila pemeriksaan secara mikroskopis hasilnya negatif dan tidak memilki akses rujukan (radiologi/TCM/biakan) maka dilakukan pemberian terapi antibiotika spektrum luas (non-OAT dan non-kuinolon) terlebih dahulu selama 1-2 minggu. Jika tidak ada perbaikan klinis setelah pemberian antibiotik, pasien perlu dikaji faktor risiko TB. Pasien dengan faktor risiko TB tinggi maka pasien dapat didiagnosis sebagai TB Klinis. Faktor risiko TB yang dimaksud antara lain:
- Terbukti ada kontak dengan pasien TB
- Ada penyakit komorbid: HIV, DM
- Tinggal di wilayah berisiko TB: Lapas/Rutan, tempat penampungan pengungsi, daerah kumuh, dll.
Uji Kepekaan MTB terhadap Antibiotik dan Diagnosis Tuberkulosis Resisten Obat (TB-RO)
Uji kepekaan terhadap antibiotik penting terutama maraknya MTB resisten obat akhir-akhir ini. Saat ini uji kepekaan minimal terhadap RIF dan INH harus dilakukan pada kelompok pasien berikut:
- Semua pasien dengan riwayat pengobatan OAT. Hal ini dikarenakan TB resisten obat banyak ditemukan terutama pada pasien yang memiliki riwayat gagal pengobatan sebelumnya.
- Semua pasien dengan HIV yang didiagnosis TB aktif. Khususnya mereka yang tinggal di daerah dengan prevalensi TB resistan obat yang tinggi.
- Pasien dengan TB aktif yang terpajan dengan pasien TB resisten obat
- Semua pasien baru di daerah dengan kasus TB resistan obat primer >3%.
- Pasien baru atau riwayat OAT dengan sputum BTA tetap positif
pada akhir fase intensif. Sebaiknya dilakukan pemeriksaan
sputum BTA pada bulan berikutnya.
Adapun cara pemeriksaan kepekaan ini dilakukan dengan dua cara yaitu cara metode uji konvensional dan metode uji cepat.
Metode Konvensional Uji Kepekaan Obat
Pemeriksaan biakan MTB dapat dilakukan menggunakan 2 macam medium padat (Lowenstein-Jensen /LJ atau Ogawa) dan media cair MGIT (Mycobacterium growth indicator tube). Biakan MTB pada media cair memerlukan waktu yang singkat minimal 2 minggu, lebih cepat dibandingkan biakan pada medium padat yang memerlukan waktu 28-42 hari.
Metode Cepat Uji Kepekaan Obat (Uji Diagnostik Molekuler Cepat)
Pemeriksaan molekular untuk mendeteksi DNA MTB saat ini merupakan metode pemeriksaan tercepat yang sudah dapat dilakukan di Indonesia. Metode molekuler dapat mendeteksi MTB dan membedakannya dengan Non-Tuberculous Mycobacteria (NTM). Selain itu metode molekuler dapat mendeteksi mutasi pada gen yang berperan dalam mekanisme kerja obat antituberkulosis lini 1 dan lini 2. WHO merekomendasikan penggunaan Xpert MTB/RIF untuk deteksi resistan rifampisin.
Resisten obat antituberkulosis lini 2 direkomendasikan untuk menggunakan second line line probe assay (SL-LPA) yang dapat mendeteksi resistensi terhadap obat antituberkulosis injeksi dan obat antituberkulosis golongan fluorokuinolon. Pemeriksaan molekuler untuk mendeteksi gen pengkode resistensi OAT lainnya saat ini dapat dilakukan dengan metode sekuensing, yang tidak dapat diterapkan secara rutin karena memerlukan peralatan mahal dan keahlian khusus dalam menganalisisnya. WHO telah merekomendasi pemeriksaan molekular line probe assay (LPA) dan TCM, langsung pada spesimen sputum.
Pemeriksaan dengan TCM dapat mendeteksi M. tuberculosis dan gen pengkode resistan rifampisin (rpoB) pada sputum kurang lebih dalam waktu 2 jam. Konfirmasi hasil uji kepekaan OAT menggunakan metode konvensional masih digunakan sebagai baku emas (gold standard). Penggunaan TCM tidak dapat menyingkirkan metode biakan dan uji kepekaan konvensional yang diperlukan untuk menegakkan diagnosis definitif TB, terutama pada pasien dengan pemeriksaan mikroskopis apusan BTA negatif, dan uji kepekaan OAT untuk mengetahui resistensi OAT selain rifampisin.
Pasien Terduga TB Resisten Obat (TB RO)
Seperti juga pada diagnosis TB maka diagnosis TB-RO juga diawali dengan penemuan pasien terduga TB-RO. Terduga TB-RO adalah pasien yang memiliki risiko tinggi resistan terhadap OAT, yaitu pasien yang mempunyai gejala TB yang memiliki riwayat satu atau lebih di bawah ini:
- Pasien TB gagal pengobatan kategori 2.
- Pasien TB pengobatan kategori 2 yang tidak konversi setelah 3 bulan pengobatan.
- Pasien TB yang mempunyai riwayat pengobatan TB yang tidak standar serta menggunakan kuinolon dan obat injeksi lini kedua paling sedikit selama 1 bulan.
- Pasien TB gagal pengobatan kategori 1.
- Pasien TB pengobatan kategori 1 yang tidak konversi setelah 2 bulan pengobatan.
- Pasien TB kasus kambuh (relaps), dengan pengobatan OAT kategori 1 dan kategori 2.
- Pasien TB yang kembali setelah loss to follow-up (lalai berobat/default).
- Terduga TB yang mempunyai riwayat kontak erat dengan pasien TB- RO, termasuk dalam hal ini warga binaan yang ada di lapas/rutan, hunian padat seperti asrama, barak, buruh pabrik.
- Pasien ko-infeksi TB-HIV yang tidak respons secara bakteriologis maupun klinis terhadap pemberian OAT, (bila pada penegakan diagnosis awal tidak menggunakan TCM TB).
Selain 9 kriteria di atas, kasus TB-RO dapat juga dijumpai pada kasus TB baru, sehingga pada kasus ini perlu juga dilakukan penegakan diagnosis dengan TCM yang saat ini sudah tersedia. Kriteria terduga TB-MDR menurut program manajemen TB resistan obat di Indonesia
- Pasien TB gagal pengobatan kategori 2 yaitu pasien TB dengan hasil pemeriksaan dahak positif pada bulan ke-5 atau pada akhir pengobatan
- Pasien TB pengobatan kategori 2 yang tidak konversi setelah 3 bulan pengobatan yaitu pasien TB dengan hasil pemeriksaan dahak positif setelah pengobatan tahap awal
- Pasien TB yang mempunyai riwayat pengobatan TB yang tidak standar serta menggunakan kuinolon dan obat injeksi lini kedua minimal selama 1 bulan.
- Pasien TB pengobatan kategori 1 yang gagal yaitu pasien TB dengan hasil pemeriksaan dahak positif pada bulan ke-5 atau pada akhir pengobatan.
- Pasien TB pengobatan kategori 1 yang tetap positif setelah 3 bulan pengobatan (yang tidak konversi) atau pasien TB dengan hasil pemeriksaan dahak tetap positif setelah pengobatan tahap awal
- Pasien TB kasus kambuh (relaps) kategori 1 dan 2, yaitu pasien TB yang pernah dinyatakan sembuh atau pengobatan lengkap dan saat ini diagnosis TB berdasarkan hasil pemeriksaan bakteriologis atau klinis
- Pasien TB yang kembali setelah loss to follow up (lalai berobat/default). Bisa pula pasien TB yang pernah diobati dan dinyatakan putus berobat selama dua bulan berturut-turut atau lebih
- Terduga TB yang mempunyai riwayat kontak erat dengan pasien TB-MDR
- Pasien ko-infeksi TB-HIV yang tidak respons secara klinis maupun bakteriologis terhadap pemberian OAT (bila penegakan diagnosis awal tidak menggunakan TCM). Respon klinis berarti dalam penggunaan OAT selama dua minggu tidak memperlihatkan perbaikan klinis
Diagnosis Banding Tuberkulosis
Tuberkulosis dapat mirip dengan banyak penyakit lain. Misalnya TB kongenital mirip dengan sifilis kongentital atau infeksi CMV. Berikut adalah peyakit yang bisa menyerupai TB paru:
- Blastomycosis
- Tularemia
- Actinomycosis
- Infeksi Mycobacterium avium-intracellulare
- Infeksi M chelonae
- Infeksi M fortuitum
- Infeksi M gordonae
- Infeksi M kansasii
- Infeksi M marinum
- Infeksi M xenopi
- Karsinoma sel skuamosa
Adapun penyakit yang mirip dengan tuberkulosis ekstraparu adalah sebagai berikut:
- Blastomycosis
- Tularemia
- Actinomycosis
- Hidradenitis suppurativa
- Granuloma eosinophilic
- Infeksi Mycobacterium avium-intracellulare
- Infeksi M chelonae
- Infeksi M fortuitum
- Infeksi M gordonae
- Infeksi M kansasii
- Infeksi M marinum
- Infeksi M xenopi
- Sidilis endemik
- Erythema induratum (nodular vasculitis)
- Erythema nodosum
- Leishmaniasis
- Lepra
- Cat scratch disease
- Syphilis
- Syringoma
- Rheumatoid arthritis
Untuk TB kulit, beberapa diagnosis banding adalah sebagai berikut:
- Membedakan inokulasi primer TB dengan kompleks ulseroglandular dan mycobacteria lainnya
- Membedakan Tb verrucosa cutis dengan penyakit lain seperti blastomycosis, chromoblastomycosis, iododerma dan bromoderma, chronic vegetative pyoderma, verruca vulgaris, verrucous carcinoma, infeksi mycobacteria atipikal, dan verrucous lupus vulgaris
- Memebdakan TB milier dari kulit dengan reaksi erupsi obat
- Membedakan skrofuloderma dengan limfadenitis supurativa dengan sinus seperti blastomycosis atau coccidioidomycosis
- Membedakan TB cutis orificialis dengan glossitis, apotheosis, dan deep fungal infections
- Membedakan lupus vulgaris dari lupoid rosacea, deep fungal atau infeksi atipikal mycobacteria, penyakit granulomatosa kronik, granulomatous rosacea, dan granulomatosis Wegener
- Membedakan erythema induratum dari nodular panniculitides (misal, penyakit Weber-Christian) dan vaskulitis nodular (misal, gumma sifilis, nodular pernio)
- Membedakan papulonecrotic tuberculid dari jenis papulonecrotic lainnya, seperti leukocytoclastic vasculitis, lymphomatoid papulosis, papular eczema, dan prurigo simplex dengan ekskoriasi nekrotikan
- Membedakan lichen scrofulosorum dari keratosis spinulosa, lichenoid sarcoid, dan lichenoid sekunder dari sifilis
Klasifikasi Pasien TB
Dalam penanganan kasus tuberkulosis, terdapat beberapa definisi. Terduga atau presumtif pasien TB adalah pasien dengan keluhan atau gejala klinis mendukung TB. Sebelumnya pasien ini disebut sebagai terduga. Jika pasien tersebut pada pemeriksaan bakteriologis positif, baik itu dari sputum, cairan tubuh, atau jaringan (baik dengan mikroskopis langsung maupun TCM TB), maka dinamakan pasien TB yang terkonfirmasi bakteriologis. Termasuk ke dalam pasien ini adalah:
- Pasien TB paru BTA positif
- Pasien TB paru hasil biakan MTB positif
- Pasien TB paru hasil tes cepat MTB positif
- Pasien TB ekstraparu terkonfirmasi secara bakteriologis, baik dengan BTA, biakan, maupun TCM TB dari contoh jaringan yang terkena
- TB anak yang terdiagnosis dengan pemeriksaan bakteriologis.
Terkadang terdapat pula kasus dimana secara gejala sesuai dengan TB namun belum terdiagnosis secara bakteriologis dan kemudian diputuskan diobati sebagai kasus TB. Keadaan ini dimasukan ke dalam kelompok pasien TB terdiagnosis secara klinis. Termasuk ke dalam kelompok ini adalah:
- Pasien TB paru BTA negatif dengan hasil pemeriksaan foto toraks mendukung TB.
- Pasien TB paru BTA negatif dengan tidak ada perbaikan klinis
setelah diberikan antibiotika non OAT, dan mempunyai faktor risiko
TB - Pasien TB ekstra paru yang terdiagnosis secara klinis maupun
laboratoris dan histopatologis tanpa konfirmasi bakteriologis. - TB anak yang terdiagnosis dengan sistim skoring.
Apabila pasien yang masuk kategori TB terdiagnosis klinis ini kemudian terkonfirmasi seacra bakteriologis positif, maka dimasukan ke dalam kelompok pasien TB yang terkonfirmasi bakteriologis. Adapun untuk menghindari over diagnosis, pemberian OAT pada kelompok pasien yang terdiagnosis klinis dianjurkan untuk kondisi:
- Keluhan, gejala dan kondisi klinis sangat kuat mendukung diagnosis TB
- Kondisi pasien perlu segera diberikan pengobatan misal: pada
kasus meningitis TB, TB milier, pasien dengan HIV positif,
perikarditis TB dan TB adrenal.
Klasifikasi Kasus TB
Setelah melakukan diagnosis, kemudian kasus TB tersebut dilakukan klasifikasi. Klasifikasi ini berperan dalam menentukan jenis terapi dan durasi terapi. Adapun klasifikasi tersebut berdasarkan parameter berikut:
Klasifikasi TB Berdasarkan Letak Anatomis
Maksudnya adalah manifestasi klinis berdasarkan organ yang terkena. Seperti dijelaskan pada bagian manifestasi klinis, klasifikasi TB berdasarkan letak anatomis terbagi dua yaitu TB paru dan TB ekstraparu.
Klasifikasi Berdasarkan Riwayat Pengobatan
Dalam anamnesis diperlukan keterangan apakah pasien pernah mendapat terapi OAT sebelumnya. Identifikasi ini bertujuan untuk menyeleksi risiko kasus TB resisten obat. Berdasarkan ananmesis tersebut, maka kasus TB terbagi menjadi:
- Kasus baru adalah pasien yang belum pernah mendapat OAT sebelumnya atau riwayat mendapatkan OAT kurang dari 1 bulan (< dari 28 dosis bila memakai obat program).
- Kasus dengan riwayat pengobatan adalah pasien yang pernah mendapatkan OAT 1 bulan atau lebih (≥28 dosis bila memakai obat program). Kasus ini diklasifikasikan lebih lanjut berdasarkan hasil pengobatan terakhir sebagai berikut :
- Kasus kambuh adalah pasien yang sebelumnya pernah mendapatkan OAT dan dinyatakan sembuh atau pengobatan lengkap pada akhir pengobatan dan saat ini ditegakkan diagnosis TB episode kembali (karena reaktivasi atau episode baru yang disebabkan reinfeksi).
- Kasus pengobatan gagal adalah pasien yang sebelumnya pernah mendapatkan OAT dan dinyatakan gagal pada akhir pengobatan.
- Kasus setelah loss to follow up adalah pasien yang pernah menerima OAT 1 bulan atau lebih dan tidak meneruskannya selama lebih dari 2 bulan berturut-turut dan dinyatakan loss to follow up sebagai hasil pengobatan.
- Kasus lain-lain adalah pasien sebelumnya pernah ndapatkan OAT dan hasil akhir pengobatannya tidak diketahui atau tidak didokumentasikan.
- Kasus dengan riwayat pengobatan tidak diketahui adalah pasien yang tidak diketahui riwayat pengobatan sebelumnya sehingga tidak dapat dimasukkan dalam salah satu kategori di atas.
Penting diidentifikasi adanya riwayat pengobatan sebelumnya karena terdapat risiko resistensi obat. Sebelum dimulai pengobatan sebaiknya dilakukan pemeriksaan biakan dan uji kepekaan obat menggunakan tercepat yang telah disetujui WHO (TCM TB MTB/Rif atau LPA (Hain test dan genoscholar) untuk semua pasien dengan riwayat pemakaian OAT.
Klasifikasi Kasus TB Berdasarkan Hasil Pemeriksaan Uji Kepekaan Obat
Setelah dilakukan uji hasil kepekaan obat, maka kasus TB dapat dikelompokan menjadi:
- Monoresisten: resistensi terhadap salah satu jenis OAT lini pertama.
- Poliresisten: resistensi terhadap lebih dari satu jenis OAT lini pertama selain isoniazid (H) dan rifampisin (R) secara bersamaan.
- Multidrug resistant (TB MDR) : minimal resistan terhadap isoniazid (H) dan rifampisin (R) secara bersamaan.
- Extensive drug resistant (TB XDR) : TB-MDR yang juga resistan terhadap salah satu OAT golongan fluorokuinolon dan salah satu dari OAT lini kedua jenis suntikan (kanamisin, kapreomisin, dan amikasin).
- Rifampicin resistant (TB RR) : terbukti resistan terhadap Rifampisin baik menggunakan metode genotip (tes cepat) atau metode fenotip (konvensional), dengan atau tanpa resistensi terhadap OAT lain yang terdeteksi. Termasuk dalam kelompok TB RR adalah semua bentuk TB MR, TB PR, TB MDR dan TB XDR yang terbukti resistan terhadap rifampisin.
Klasifikasi Berdasarkan Status HIV
Penderita HIV berisiko tinggi terkena tuberkulosis. Koinfeksi HIV/TB menjadi masalah penting karena tingginya kasus koinfeksi tersebut. Oleh sebab itu, pada penderita TB juga perlu dikonfirmasi status apakah pasien tersebut juga terkena HIV atau tidak. Berdasarkan status HIV terebut maka klasifikasi kasus TB adalah sebagai berikut:
- Kasus TB dengan HIV positif adalah kasus TB terkonfirmasi bakteriologis atau terdiagnosis klinis pada pasien yang memiliki hasil tes HIV-positif, baik yang dilakukan pada saat penegakan diagnosis TB atau ada bukti bahwa pasien telah terdaftar di register HIV (register pra ART atau register ART).
- Kasus TB dengan HIV negatif adalah kasus TB terkonfirmasi bakteriologis atau terdiagnosis klinis pada pasien yang memiliki hasil negatif untuk tes HIV yang dilakukan pada saat ditegakkan diagnosis TB. Bila pasien ini diketahui HIV positif di kemudian hari harus kembali disesuaikan klasifikasinya.
- Kasus TB dengan status HIV tidak diketahui adalah kasus TB terkonfirmasi bakteriologis atau terdiagnosis klinis yang tidak memiliki hasil tes HIV dan tidak memiliki bukti dokumentasi telah terdaftar dalam register HIV. Bila pasien ini diketahui HIV positif dikemudian hari harus kembali disesuaikan klasifikasinya.
Penatalaksanaan/Terapi Tuberkulosis
Terapi tuberkulosis difokuskan untuk menyembuhkan individu yang terkena penyakit dan mengurangi transmisi atau penyebaran Mycobacterium tuberculosis (MTB) ke orang lain. Keberhasilan terapi akan menguntungkan baik pasien sendiri maupun kesehatan lingkungan secara keseluruhan.
Dalam sejarah pengobatan tuberkulosis, terdapat kesulitan yang cukup kentara. Kesulitan ini dikarenakan perbedaan tingkat metabolisme MTB di dalam tubuh. Terdapat populasi MTB yang aktif dan bereplikasi cepat. Kelompok ini bertanggung jawab pada kondisi klinis yang cepat dan mengancam nyawa.
Kelompok kedua adalah MTB yang persisten dengan tingkat metabolisme yang rendah. Bakteri kelompok ini tahan terhadap antibiotik dan bertanggung jawab terhadap relapsnya tuberkulosis pada penderita yang menerima pengobatan.
Melalui penelitian selama hampir 7 dekade, didapat bahwa untuk mendapatkan hasil terapi yang baik dan konsisten memerlukan regimen dengan beberapa obat sekaligus, memberikan regimen dengan toksisitas yang seminimal mungkin, dan memaksimalkan kepatuhan penderita untuk berobat sampai tuntas.
Untuk mengobati dan memberantas kuman MTB yang bereplikasi secara cepat, obat yang paling efektif adalah INH dan fluoroquinolon. Adapun untuk kelompok MTB yang persisten obat yang efektif adalah rifamycin dan PZA. Walaupun demikian, PZA kemampuannya terbatas pada kondisi khusus yaitu tempat yang memiliki keasaman yang meningkat.
Dengan demikian, jelas bahwa untuk memberantas kedua kelompok kuman tadi memerlukan regimen dengan multipel obat. Selain itu, pemberian lebih dari satu jenis obat juga bertujuan untuk menghambat munculnya kuman MTB resisten. Selain pemberian untuk terapi, OAT ini juga diberikan sebagai regimen profilaskis atau pencegahan khususnya untuk kelompok individu yang rentan terinfeksi. Berikut akan dibahas mengenai penanganan tuberkulosis dalam berbagai situasi klinis:
Kapan Pemberian Terapi Empiris Obat Antituberkulosis (OAT) Diberikan?
Terkadang kita menghadapi kasus dimana diagnosis pasti belum tegak namun kondisi pasien memerlukan penanganan segera karena kondisi yang mengancam nyawa. Pada kondisi tersebut, pemberian obat bersifat empiris. Pada prinsipnya, pemberian terapi empiris ini ditujukan pada kondisi dimana kemungkinan besar penyebab dari kondisi tersebut adalah tuberkulosis. Adapun keputusan dalam pemberian terapi empiris ini berdasarkan klinis, radiografi, hasil laboratorium, dan faktor kesehatan masyarakat.

Pada kondisi dimana gejala klinis menunjukan ke arah tuberkulosis, hasil BTA positif merupakan petunjuk kuat diagnosis tuberkulosis. Jika diagnosis kemudian dikonfirmasi dengan isolasi MTB atau hasil positif dengan tes molekuler cepat maka terapi dilanjutkan sampai selesai sesuai standar. Jika pasien memiliki BTA positif namun tes molekuler cepat negatif (termasuk dengan penilaian kemungkinan adanya faktor inhibitor PCR yang ditemukan pada 2-5% spesimen), maka didapat kesimpulan bahwa besar kemungkinan BTA positif bukan disebabkan oleh MTB terutama jika tes molekuler juga negatif untuk BTA positif spesimen ulang kedua.
Jika terapi empiris dimulai, hasil biakan sebelum dan selama pemberian hasilnya negatif serta tidak ada respon pemberian namun tes IGRA dan tuberkulin positif, maka lanjutkan terapi sebagai kasus tuberkulosis laten. Pemberian pengobatan dilanjutkan dengan penyesuaian regimen untuk TB laten (pembahasan TB laten di bawah).
Rekomendasi Regimen Obat Antituberkulosis (OAT)
Berikut adalah regimen OAT yang direkomendasikan untuk diberikan sebagai terapi kasus tuberkulosis tanpa resistensi:
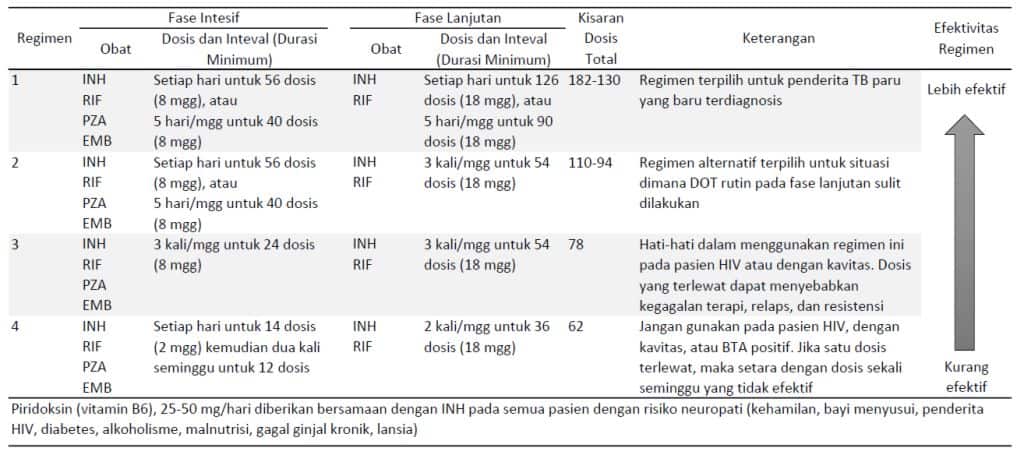
Di tabel di atas tampak bahwa regimen OAT pada fase intensif terdiri dari empat obat. Hal ini dikarenakan proporsi yang signifikan MTB yang resisten terhadap INH. Namun, jika sebelumnya telah dilakukan tes resistensi dan MTB yang didapat rentan terhadap RIF dan INH maka tidak perlu diberikan EMB sehingga fase intensif hanya terdiri dari INH, RIF, dan PZA. Piridoksin atau vitamin B6 diberikan pada pasien yang mendapat INH dan berisiko terkena neurotoksisitas (wanita hamil, bayi dengan ASI, penderita HIV, diabetes, alkoholisme, malnutrisi, gagal ginjal kronik, atau lansia).
Pada panduan penatalaksanaan TB di Indonesia (PNPK Tatalaksana TB Indonesia 2019), streptomisin masuk ke dalam salah satu OAT lini pertama. Adapun dosis untuk masing-masing obat adalah sebagai berikut:
- Isoniazid
- Sediaan: tablet (50 mg, 100 mg, 300 mg); eliksir 50 mg/5 mL; cairan IV/IM 100 mg/mL
- Catatan: Tambahkan piridoksin 25-50 mg pada pasien berisiko neuropati, sedangkan pada penderita neuropati perifer berikan piridoksin 100 mg/hari
- Dosis:
| Populasi | Sekali sehari | Sekali seminggu | Dua kali seminggu | Tiga kali seminggu |
|---|---|---|---|---|
| Dewasa | 5 mg/kg biasanya 300 mg | 15 mg/kg biasanya 900 mg | 15 mg/kg biasanya 900 mg | 15 mg/kg biasanya 900 mg |
| Anak | 10-15 mg/kg | 20-30 mg/kg | Dosis optimal 3x/mgg belum diketahui. Beberapa ahli menyamakan dengan dosis dewasa dan pada anak usia lebih muda disamakan dengan dosis 2x/mgg |
- Rifampin
- Sediaan: kapsul (150 mg, 300 mg). Suspensi untuk sediaan oral.
- Dosis:
| Populasi | Sekali sehari | Dua kali seminggu | Tiga kali seminggu |
|---|---|---|---|
| Dewasa | 10 mg/kg biasanya 600 mg | 10 mg/kg biasanya 600 mg | 10 mg/kg biasanya 600 mg |
| Anak | 10-20 mg/kg | 10-20 mg/kg | Dosis optimal 3x/mgg belum diketahui. Beberapa ahli menyamakan dengan dosis dewasa dan pada anak usia lebih muda disamakan dengan dosis 2x/mgg |
- Rifabutin
- Sediaan: kapsul 150 mg
- Dosis:
| Populasi | Sekali sehari | Dua kali seminggu | Tiga kali seminggu |
|---|---|---|---|
| Dewasa | 5 mg/kg biasanya 300 mg | Tidak direkomendasikan | Tidak direkomendasikan |
| Anak | Tidak diketahui, diperkirakan 5 mg/kg |
- Rifapentine
- Tablet salut 150 mg
- Dosis:
| Populasi | Sekali seminggu |
|---|---|
| Dewasa | 10-20 mg/kg |
| Anak | Tb aktif usia ≥12 tahun dosis sama dengan dewasa, berikan sekali seminggu. Tidak direkomendasikan diberikan pada anak usia <12 tahun. |
- Pyrazinamide
- Sediaan: tablet 500 mg
- Dosis anak
- Sekali sehari: 35 (30-40) mg/kg
- Dua kali/mgg: 50 mg/kg
- Tiga kali/mgg: dosis optimal 3x/mgg belum diketahui. Beberapa ahli menyamakan dengan dosis dewasa dan pada anak usia lebih muda disamakan dengan dosis 2x/mgg
- Dosis untuk dewasa:
| Regimen | BB 40-55 kg | BB 56-75 kg | BB 76-90 kg |
|---|---|---|---|
| Sekali sehari | 1000 mg (18,2-25 mg/kg) | 1500 mg (20-26,8 mg/kg) | 2000 mg (22,2-26,3 mg/kg) |
| Dua kali/mgg | 1500 mg (27,3-37,5 mg/kg) | 2500 mg (33,3-44,6 mg/kg) | 3000 mg (33,3-39,5 mg/kg) |
| Tiga kali/mgg | 2000 mg (36,4-50 mg/kg) | 3000 mg (40-53,6 mg/kg) | 4000 mg (44,4-52,6 mg/kg) |
- Ethambutol
- Sediaan: tablet 1000 mg; 400 mg
- Keterangan: untuk menghindari toksisitas EMB pada mata, beberapa klinisi menggunakan 3 obat (INH, RIF, PZA) sebagai terapi intensif pada anak tanpa infeksi HIV, tanpa riwayat TB sebelumnya, tinggal di daerah prevalensi TB rendah, dan tidak ada riwayat paparan dengan penderita TB dari tempat yang memiliki tingkat resistensi tinggi. Namun, karena prevalensi resistensi obat tidak diketahui dengan pasti, EMB tetap direkomendasikan diberikan sebagai terapi intensif pada anak.
- Dosis anak:
- Sekali sehari: 20 (15–25) mg/kg
- Dua kali seminggu: 50 mg/kg
- Tiga kali seminggu: dosis optimal 3x/mgg belum diketahui. Beberapa ahli menyamakan dengan dosis dewasa dan pada anak usia lebih muda disamakan dengan dosis 2x/mgg
- Dosis dewasa:
| Regimen | BB 40-55 kg | BB 56-75 kg | BB 76-90 kg |
|---|---|---|---|
| Sekali sehari | 800 mg (14,5-20 mg/kg) | 1200 mg (16-21,4 mg/kg) | 1600 mg (17,8-21,1 mg/kg) |
| Dua kali/mgg | 1200 mg (21,8-30 mg/kg) | 2000 mg (26,7-35,7 mg/kg) | 2400 mg (25,7-31,6 mg/kg) |
| Tiga kali/mgg | 2000 mg (36,4-50 mg/kg) | 2800 mg (37,3-50 mg/kg) | 4000 mg (44,4-52,6 mg/kg) |
- Streptomisin
- Dosis dewasa:
- Harian: 15 (12-18) mg/kg/hari
- Dosis 3 kali/mgg: 15 (12-18)
- Keterangan: Pasien berusia diatas 60 tahun tidak dapat mentoleransi lebih dari 500-700 mg perhari, beberapa pedoman merekomendasikan dosis 10 mg/kg BB pada pasien kelompok usia ini. Pasien dengan berat badan di bawah 50 kg tidak dapat mentoleransi dosis lebih dari 500-750 mg perhari.
- Dosis dewasa:
Sediaan OAT FDC (Fix-Dose Combination)
Untuk memudahkan dan menaikan kepatuhan pengobatan, maka tersedia sediaan OAT berupa FDC. FDC OAT ini terdiri dari dua jenis yaitu kaplet fase intensif, terdiri dari kombinasi RIF 150 mg, INH 75 mg, PZA 400 mg, dan EMB 275 mg. Adapun kaplet fase lanjut berwarna kuning tediri dari RIF 150 mg dan INH 150 mg. Panduan dosis dapat dihitung berdasarkan berat badan atau mengikuti tabel berikut:
| Berat badan (dewasa) | Tahap intensif (RHZE) (150/75/400/275) | Tahap lanjutan (RH) (150/150) |
|---|---|---|
| 30-37 kg | 2 tablet | 2 tablet |
| 38-54 kg | 3 tablet | 3 tablet |
| 55-70 kg | 4 tablet | 4 tablet |
| ≥70 kg | 5 tablet | 5 tablet |
Untuk FDC OAT anak, terdiri dari kombinasi RIF 75 mg, INH 50 mg, dan PZA 150 mg untuk fase intensif dan RIF 75 mg dan INH 50 mg per tablet untuk fase lanjutan. Adapun panduan berdasarkan berat badan adalah sebagai berikut:
| Berat badan (anak) | Tahap intensif (RHZE) (75/50/150) | Tahap lanjutan (RH) (75/50) |
|---|---|---|
| 5-9 kg | 1 tablet | 1 tablet |
| 10-14 kg | 2 tablet | 2 tablet |
| 15-19 kg | 3 tablet | 3 tablet |
| 20-32 kg | 4 tablet | 4 tablet |
Komposisi Alternatif Regimen OAT Lini Pertama
Dalam kondisi dimana salah satu obat tidak ditoleransi atau adanya monoresistensi, maka diperlukan regimen dengan komposisi alternatif. Jika PZA tidak bisa ditoleransi atau adanya resistensi terhadap PZA (kondisi jarang kecuali pada M. bovis dan M. bovis var BCG), maka para ahli merekomendasikan fase intensif terdiri dari INH, RIF, dan EMB untuk 2 bulan diikuti INH dan RIF selama 7 bulan.
Pada skenario dimana EMB dan atau INH tidak dapat diberikan, beberapa ahli memberikan moxifloxacin atau levofloxacin pada fase intensif untuk mengganti PZA dan pada keseluruhan fase terapi untuk mengganti INH. Namun, peran kedua obat golongan fluoroquinolon ini dalam mengganti baik EMb atau INH belum dipastikan melalui suatu uji klinis.
Selain itu, tidak ada bukti yang bisa mendukung pemberian moxifloxacin maupun levofloxacin untuk menggantikan RIF atau PZA dalam regimen dengan durasi pengobatan 6 bulan. Jika RIF tidak diberikan karena intoleransi atau resistensi, maka sebaiknya diterapi sesuai dengan kasus resistensi obat. Begitu juga ketika beberapa regimen lini pertama tidak diberikan sekaligus, maka prinsip terapi diberikan sesuai dengan pada kasus resistensi OAT.
Penting untuk dicatat bahwa semua regimen alternatif yang menggunakan fluoroquinolon sebagai pengganti EMB atau INH digunakan dalam tempo durasi 6 bulan atau lebih. Terdapat uji definitif dimana pemberian regimen moxifloxacin atau gatifloxacin untuk EMB atau moxifloxacin untuk INH dalam dosis harian selama 4 bulan kurang efektif dibandingkan terapi standar 6 bulan.
Sebuah RCT yang mencoba memberikan dosis harian moxifloxacin/RIF/PZA/EMB selama 2 bulan diikuti sekali sehari RPT 1200 mg + 400 mg moxifloxacin memberikan hasil yang serupa dengan standar regimen standar 6 bulan dosis harian. Oleh sebab itu, penggunaan moxifloxacin harian dapat dipertimbangkan. Harus dicatat pula bahwa pada RCT ini, sebelum meminum RPT, pasien terlebih dahulu mengonsumsi 2 butir telur rebus dan selembar roti untuk meningkatkan absoprsi RPT. Oleh sebab itu, penggunaan regimen ini harus dalam program uji yang disertai dengan pemantauan yang mencukupi.
Cara Konsumsi OAT
Secara umum semua OAT dikonsumsi dalam waktu bersamaan agar mencapai konsenterasi obat dalam darah yang maksimum serta memfasilitasi DOT. Bioavailibilitas semua obat (kecuali RPT) akan maksimal jika dikonsumsi dalam keadaan perut kosong. Pengecualiannya adalah RPT dimana bioavailibilitasnya meningkat 86% jika dikonsumsi bersamaan dengan makanan tinggi lemak.
Apabila obat harus dikonsumsi bersama dengan makanan atau minuman perlu diingat bahwa absorpsi INH berkurang ketika dikonsumsi bersama dengan glukosa atau laktosa. Oleh sebab itu, jika harus dikonsumsi bersama dengan makanan, INH dikonsumsi dengan makanan rendah gula.
Evaluasi Baseline dan Follow-Up
Pemeriksaan untuk evaluasi baseline dan follow-up dapat disimak ringkasannya di gambar di bawah ini:

Di baseline atau saat pertama kali sebelum terapi, pasie harus mendapat pemeriksaan spesimen dahak atau sputum minimal dua kali dengan salah satu spesimen berasal dari sputum pagi. Tujuannya adalah untuk diagnosis mendeteksi adanya BTA serta untuk dilakukan pemeriksaan tes molekuler cepat baik deteksi MTB maupun resistensi terhadap rifamycin.
Pada kasus TB paru, pemeriksaan dua sputum tadi dengan jeda pemeriksan 8-24 jam. Adapun pada pasien yang tidak produktif, dilakukan induksi sputum dengan inhalasi cairan salin hipertonik atau dengan bronkoskopi.
Saat menjalani terapi, pemeriksaan sputum untuk BTA atau biakan diperoleh tiap bulan untuk memastikan terjadi konversi sputum pada fase intensif. Walaupun demikian, pemeriksaan sputum ini dapat dilakukan dengan interval yang lebih pendek misalnya dalam jeda waktu dua minggu khususnya pada pasien dengan BTA positif.
Perlu diperhatikan bahwa seringkali didapatkan pemeriksaan BTA atau tes molekuler cepat positif namun biakan negatif. Hal ini terutama pada pasien dengan kavitas paru yang menjalani pengobatan dalam bulan pertama. Hal ini menandakan organisme MTV non vital atau mati. MTB yang mati dapat memberikan hasil BTA dan tes molekuler cepat positif.
Pemanjangan fase intensif dilakukan jika hasil biakan masih positif setelah dua bulan pengobatan. Hal ini dapat terjadi terutama pada pasien dengan berat badan >10% berat ideal, perokok, infeksi HIV, kondisi imunkompromais lain, diabetes, atau penyakit ekstensif dari pemeriksaan Rontgen toraks.
Putus Pengobatan OAT
Panjanganya durasi terapi dapat berisiko untuk terjadinya putus obat. Yang terpenting jika menghadapi kasus putus pengobatan adalah memutuskan apakah pasien meneruskan terapi sebelumnya atau harus dimulai kembali dari awal. Secara umum, semakin awal terjadinya putus obat dan semakin lama durasi putus obat maka pengobatan harus dimulai dari awal kembali. Berikut ini adalah tabel panduan mengenai pendekatan yang harus dilakukan dalam berbagai kondisi skenario putus OAT:
| Periode putus obat | Keterangan | Pendekatan |
|---|---|---|
| Periode intensif | Durasi putus obat <14 hari | Lanjutkan pengoabtan sampai seluruh dosis periode intensif lengkap |
| Durasi putus ≥14 hari | Ulangi pengobatan dari awal | |
| Fase lanjutan | Menerima ≥80% dosis yang direncanakan dan sputum negatif saat mulai terapi | Tidak diteruskan terapi |
| Menerima ≥80% dosis yang direncanakan dan sputum positif saat mulai terapi | Lanjutkan sampai seluruh dosis pengobatan lengkap | |
| Menerima <80% dosis yang direncanakan dan akumulasi durasi putus obat <3 bulan | Lanjutkan sampai lengkap kecuali dalam satu waktu putus obat >2 bulan secara berturut-turut Jika terapi tidak mungkin diselesaikan dalam waktu yang ditentukan maka mulai kembali terapi dari fase intensif | |
| Menerima <80% dosis yang direncanakan dan akumulasi durasi putus obat ≥3 bulan | Mulai kembali dari awal fase intensif |
Definisi Selesai Menjalani Terapi
Dalam menentukan apakah seseorang telah menyelesaikan terapi OAT tidak hanya dilihat dari durasi lama pemberian namun juga jumlah dosis yang telah diterima. Apabila kita meninjau jumlah dosis, maka seluruh dosis yang diberikan pada fase intensif harus dikonsumsi paling lambat setidaknya 3 bulan dan seluruh dosis fase lanjutan dalam waktu paling lambat 6 bulan. Jika target ini tidak tercapai, maka pasien dianggap putus pengobatan OAT sehingga harus mengikuti aturan seperti tabel di atas.
Adapun menurut program nasional, penilaian hasil pengobatan adalah sebagai berikut:
| Hasil | Definisi |
|---|---|
| Sembuh | Pasien TB paru dengan konfirmasi bakteriologis positif pada awal pengobatan dan BTA sputum negatif atau biakan negatif pada akhir pengobatan dan memiliki hasil pemeriksaan negatif pada salah satu pemeriksaan sebelumnya |
| Pengobatan lengkap | Pasien TB yang telah menyelesaikan pengobatan secara lengkap dan tidak memiliki bukti gagal pengobatan tetapi juga tidak memiliki hasil BTA sputum atau biakan negatif pada akhir pengobatan dan satu pemeriksaan sebelumnya, baik karena tidak dilakukan atau karena hasilnya tidak ada. |
| Pengobatan gagal | Pasien TB dengan hasil pemeriksaan BTA sputum atau biakan positif pada bulan kelima atau akhir pengobatan. |
| Meninggal | Pasien TB yang meninggal dengan alasan apapunsebelum dan selama pengobatan TB |
| Putus obat | Pasien TB yang tidak memulai pengobatan setelah terdiagnosis TB atau menghentikan pengobatan selama 2 bulan berturut-turut atau lebih |
| Tidak dievaluasi | Pasien yang tidak memiliki hasil pengobatan pada saat akhir pelaporan kohort pengobatan, termasuk pasien yang sudah pindah ke fasilitas kesehatan lain dan tidak diketahui hasil pengobatannya oleh fasilitas yang merujuk pada batas akhir pelaporan kohort pengobatan. |
| Keberhasilan pengobatan | Jumlah kasus dengan hasil pengobatan sembuh dan lengkap. |
Penatalaksanaan Efek Samping OAT
OAT merupakan kombinasi beberapa obat sehingga risiko munculnya efek samping juga cukup besar. Gejala ringan biasanya dapat ditatalaksana dengan memberi pengobatan yang mengontrol gejala tersebut. Pada efek samping yang berat terkadang perlu disertai dengan penghentian pemberian OAT.
Gangguan Pencernaan
Gejala saluran cerna seperti tidak nyaman di perut, mual, muntah, dan penurunan nafsu makan dapat dijumpai. Untuk meminimalisasi gejala ini, disarankan untuk mengonsumsi OAT sebelum tidur. Selain itu, nyeri perut dapat diantisipasi dengan pemberian antasida atau penekan asam lambung.
Jika terdapat keluhan ini maka selain pemeriksaan fisik juga sebaiknya diperiksa fungsi hati (AST, ALT, bilirubin, dan alkali fosfatase) untuk menilai apakah ada hubungannya gejala tersebut dengan gangguan hati. Apabila bukan karena hepatotoksisitas, selain OAT diminum sebelum tidur, dianjurkan juga untuk mengonsumsi makanan ringan rendah lemak untuk mengurangi gejala.
Jika gejala masih belum membaik, pilihan lainnya adalah membagi dosis menjadi beberapa kali atau mengganti obat yang dicurigai menyebabkan gejala ke obat lainnya. Perlu diingatkan bahwa makanan yang mengandung kation divalen (kalsium, besi, zinc) dapat mengganggu penyerapan obat golongan fluorokuinolon.
Kemerahan Kulit
Semua OAT dapat menimbulkan kemerahan di kulit. Jika kemerahan tersebut terutama disertai gatal tanpa adanya tanda sistemik seperti demam maka terapinya adalah antihistamin dan OAT tetap dilanjutkan.
Kemerahan berupa peteki menandakan tanda yang lebih serius yang bisa saja disebabkan trombositopenua yang bisa disebabkan oleh hipersensitivitas terhadap rifamycin (RIF, RBT, RPT). Apabila memang trombost rendah, maka rifamycin tidak diberikan untuk seterusnya.
OAT juga dihentikan apabila terdapat rash eritematosa generalisata. Jika terdapat demam dan keterlibatan mukosa sangat mungkin merupakan bagian dari sindrom Steven-Johnson, toxic epidermal necrosis, atau reaksi obat dengan eosinofilia dan systemic symptoms syndrome atau drug hypersensitivity syndrome.
Beberapa ahli menatalaksana reaksi berat dengan merawat pasien dan setelah beberapa hari obat dihentikan diberikan kembali satu per satu sambil melihat perubahan gejala untuk mengidentifikasi obat penyebab yang pasti. Interval pemberian obat ini biasanya 2-3 hari. RIF diberikan pertama (obat paling poten) ddikuti INH, kemudian EMB atau PZA.
Demam Akibat Obat
Untuk menentukan penyebab demam akibat obat harus menyingkirkan terlebih dahulu penyebab lain. Tuberkulosis sendiri menyebabkan demam dengan kemungkingan lain seperti reaksi paradoksikal (IRIS) pada penderita HIV. Pasien dengan demam akibat obat biasanya mengalami demam ≥39°C, tidak mengikuti pola demam tertentu, dan tidak ada eosinofilia. Penghentian obat akan menyebabkan demam reda dalam 24 jam. Setelah demam reda, OAT diberikan kembali satu per satu setiap 2-3 hari sama dengan yang dijelaskan sebelumnya.
Hepatitits Imbas Obat/Drug-Induce Liver Injury (DILI) Akibat OAT
Hepatitis imbas obat merupakan efek samping serius OAT lini pertama yang paling sering ditemui. INH, RIF, dan PZA adalah OAT lini pertama dengan potensi hepatotoksisitas yang paling besar. Terjadinya hepatitis imbas obat ini disangkakan apabila terjadi kenaikan kadar ALT ⩾3 batas atas normal apabila ada gejala, atau ⩾5 kali batas atas normal jika tanpa gejala. Adapun tingkat keparahannya adalah sebagai berikut:
- Ringan jika ALT <5 kali batas atas normal
- Sedang jika ALT 5-10 kali batas atas normal
- Berat jika ALT >10 kali batas atas normal
Sebenarnya kenaikan ALT tanpa gejala terjadi pada sebanyak 20% pasien yang diberikan OAT dengan kombinasi 4 obat. Dalam keadaan tanpa gejala, kenaikan ALT ringan bukan merupakan indikasi penghentian OAT. Namun, monitoring klinis dan laboratorium harus dilakukan lebih sering.
Namun, jika ALT naik ⩾5 kali batas atas normal dengan atau tanpa gejala atau naik ⩾3 kali batas atas normal disertai gejala maka OAT yang bersifat hepatotoksik harus segera dihentikan dan pasien langsung dievaluasi. Selain kenaikan ALT, kenaikan signifikan bilirubin dan alkali fosfatase juga dapat menjadi alasan penghentian OAT. Kenaikan signigfikan bilirubin dan alkali fosfatase yang lebih signifikan dibandingkan kenaikan ALT dapat dijumpai pada hepatotoksisitas akibat rifampin (hepatotoksisitas tipe kolestatik).
Ketika OAT dihentikan dan ALT turun <2 kali batas atas normal, maka pemberian OAT dimulai kembali satu demi satu. Pada pasien yang memiliki penyakit hati sebelumnya, pemberian kembali OAT dilakukan saat ALT kembali ke kadar baseline.
Pendekatan optimal pemberian kembali OAT tidak diketahui namun biasanya dilakukan secara sekuensial. Dikarenakan RIF memiliki potensi hepatotoksik yang lebih kecil dibandingkan INH dan PZA, maka RIF diberikan pertama kali saat reintroduksi OAT.
Jika dalam seminggu tidak ada kenaikan ALT, maka dilanjutkan dengan pemberian INH. Setelah satu minggu tidak ada kenaikan ALT, maka yang terakhir adalah diberikan kembali PZA. Jika kemudian terjadi kenaikan ALT, maka hanya obat terakhir yang ditambahkan distop dan tidak diberikan untuk selanjutnya.
Neuritis Optik
Gangguan penglihatan akibat EMB pada pengobatan TB aktif terjadi pada sekitar 22,5 per 1000 orang (2,25%) pada pasien yang menerima EMB dengan dosis standar. Onset munculnya neuritis optik biasanya terjadi setelah >1 bulan dimulainya terapi namun dapat pula terjadi dalam hitungan hari.
Pendapat ahli menyarankan pemeriksaan visus (tes Snellen) dan tes warna dilakukan pertama sebagai baseline dan dilakukan ulang satu bulan kemudian sebagai follow-up. Untuk menghindari defisit penglihatan permanen, EMB segera dihentikan jika ditemukan adanya gangguan penglihatan. Jika setelah penghentian EMB penglihatan tidak membaik, disarankan untuk dihentikan pula INH karena obat ini juga berpotensi menyebabkan neuritis optik walaupun lebih jarang.
Interaksi Obat
Interaksi obat terjadi jika satu obat mempengaruhi konsenterasi obat yang lain. Perubahan konsenterasi ini dapat berupa kenaikan kadar sehingga muncul efek toksik atau sebaliknya, menurunkan kadar obat sehingga menurunkan efektivitas obat tersebut. Interaksi obat dapat terjadi terhadap obat OAT maupun antara OAT dengan obat lain.
Interaksi Terhadap OAT
Hampir semua OAT kecuali RFB dengan fluoroquinolon tidak dipengaruhi oleh obat yang lain sama lain. Penyebab interaksi RFB dan fluoroquinolon adalah sebagai berikut:
- Inhibitor CYP3A meningkatkan kadar serum dari RFB dan salah satu metabolitnya (25-O-desacetyl-rifabutin), dapat menyebabkan toksisitas. Contohnya ritonavir yang merupakan inhibitor poten CYP3A dengan RFB dosis standar (300 mg) akan meningkatkan konsenterasi serum RFB sampai 4 kali dan 25-O-desacetyl-rifabutin 35 kali. Peningkatan ini berhubungan dengan meningkatnya kejadian leukopenia, atralgia, diskolorasi kulit, dan uveitis anterior. Sebaliknya, pemberian RFB dengan induser CYP3A seperti efavirenz atau fenitoin dapat menurunkan kadar RFB dan berpotensi menyebabkan kegagalan pengobatan OAT.
- Absoprsi fluotroquinolon berkurang secara signifikan jika diminum bersanaab dengan obat atau zat yang mengandung kation divalen (kalsium, besi, zinc) misalnya antasida atau suplemen yang kaya akan kalsium, besi, dan zinc. Interaksi ini dapat dihindari dengan mengonsumsi obat dengan kation divalen secara terpisah setidaknya 2 jam diantaranya. Sebagai tambahan, konsenterasi moxifloxacin berkurang 25-30% jika dikonsumsi bersama-sama dengan RIF karena induksi enzim metabolisme fase II (sulfasi dan glukuronidasi). RPT dan RFB juga dapat mengurangi konsenterasi moxifloxacin walaupun signifikansinya secara klinis masih belum jelas.
Interaksi Obat Akibat Rifamycin
Kebanyakan interaksi OAT dengan obat lain disebabkan oleh efek rifamycin (RIF, RPT, dan RBT) terhadap metabolisme obat lain. Semua rifamycin merupakan induser berbagai jalur metabolisme terutama yang berkaitan atau diperankan oleh berbagai sistem isoenzim cytochrome P450 (CYP). Dengan menginduksi enzim metabolisme, rifamycin akan mengurangi konsenterasi obat lainnya dan terkadang sampai ke level subterapeutik.
RIF merupakan induser yang paling poten sedangkan RFB adalah yang paling kecil potensinya. Potensi RPT tergantung dari dosis yang diberikan dimana pemberian harian RPT memberikan potensi setara dengan RIF sedangkan dosis sekali seminggu memberikan dampak yang minimal terhadap obat lainnya. Interaksi obat yang berkaitan dengan rifamycin dan secara klinis relevan dapat disimaik ditabel berikut:
| Kelas obat | Obat dengan konsenterasi berkurang secara substansial akibat rifampicin | Keterangan |
|---|---|---|
| Antiretroviral | Protease inhibitor HIV-1 (lopinavir/ritonavir, darunavir/ ritonavir, atazanavir, atazanavir/ritonavir | Lebih baik gunakan RFB. Pada regimen /r, RFB 150 mg per hari. Dosis ganda LPV/r bisa digunakan jika menggunakan RIF namun kemungkinan toksisitas bertambah. Jangan gunakan RIF dengan PI lainnya |
| NNRTI Nevirapine Efavirenz Rilpivirine Etravirine | RIF mengurangi paparan pada semua NNRTI. Pada nevirapine dengan RIF, dosis awal naikan dari 200 mg menjadi 400 mg. Pada penggunaan RIF dengan efavirenz, berikan dosis standar 600 mg walaupun ada yang menyarankan naikan menjadi 800 mg pada orang dengan BB >60 kg. Rilpivirine dan etravirine tidak boleh dipakai bersamaan dengan RIF. RFB dapat diberikan bersamaan dengan nevirapine dan etravirine pada dosis biasa. Pada evafirenz dan RFB naikan dosis RFB sampai 600 mg sehari. Rilpivirine tidak boleh dipakai bersamaan dengan RFB | |
| INSTI Raltegravir Dolutegravir Elvitegravir | Naikan dosis raltegravir sampai 800 mg dua kali sehari dengan RIF walaupun data klinis menunjukan efektivitas setara pada pemberian 400 mg dua kali sehari. Dosis dolutegravir harus dinaikan menjadi 50 mg tiap 12 jam dengan RIF. Jangan memakai RIF bersamaan dengan elvitegravir. Semua INSTI dapat dipakai bersamaan dengan RFB | |
| Inhibitor CCR5 Maraviroc | Maraviroc tidak dipakai bersamaan dengan RIF, bisa bersamaan dengan RFB. | |
| Antibiotika dan antiparasit | Makrolida (azithromycin, clarithromycin, erythromycin) Doxycycline | Azithromycin tidak berinteraksi secara signifikan dengan RIF. Pemberian RFB dengan clarithromycin dapat terjadi interaksi bidireksional yang bisa meningkatkan toksisitas RFB sehingga menyebabkan uveitis. Erythromycin merupakan substrat CYP3A4 dan clearance obat bisa meningkat dengan adanya RIF. |
| Doksisiklin | Disarankan diganti doksisiklin dengan obat lain. | |
| Antijamur azole (ketoconazole, itraconazole, voriconazole, fluconazole, posaconazole, isavuconazole) Atovaquone | Konsenterasi itraconazole, ketoconazole, dan voriconazole dapat turun ke level subterapeutik jika digunakan bersamaan dengan RIF. Fluconazole dapat dipakai bersamaan dengan RIF namun dosisnya sebaiknya dinaikan. | |
| Atovaquone | Saran untuk diganti dengan alternatif lain | |
| Kloramfenikol | Saran untuk diganti dengan alternatif lain | |
| Mefloquine | Saran untuk diganti dengan alternatif lain | |
| Terapi hormonal | Ethinylestradiol, norethindrone | Bagi wanita yang memakai cara ini disarankan ditambah dengan kontrasepsi lain |
| Tamoxifen | Saran untuk diganti dengan alternatif lain | |
| Levothyroxine | Monitor TSH lebih sering, sering memerlukan penambahand osis levothyroxine | |
| Narkotik | Methadone | Penggunaan RIF maupun RFB memerlukan penaikan dosis methadone. RFB lebih jarang menyebabkan methadone withdrawal. |
| Antikoagulan | Warfarin | Monitor PT, sering memerlukan kenaikan dosis 2-3 kali lipat dari dosis sebelumnya. |
| Imunosupresan | Cyclosporine, tacrolimus | RFB memungkinkan untuk penggunaan bersamaan dengan cyclosporine. Monitor kadar obar cyclosporine dan tacrolimus untuk membantu penyesuaian obat. |
| Kortikosteroid | Monitor secara klinis, dapat membutuhkan peningkatan dosis steroid 2-3 kali lipat. | |
| Antikejang | Fenitoin, lamotrigine | Memerlukan monitoring kadar obat, memerlukan penambahan dosis antikejang |
| Kardiovaskuler | Verapamil, nifedipine, diltiazem (interaksi serupa juga diperkirakan terjadi pada penggunaan felodipine dan nisoldipine) | Monitor secara klinis, mungkin harus mengganti obat. |
| Propranolol, metoprolol | Monitor secara klinis, mungkin harus menaikan dosis atau mengganti obat. | |
| Enalapril, losartan | Monitor secara klinis, mungkin harus menaikan dosis atau mengganti obat. | |
| Digoxin (pada pasien dengan gangguan ginjal), digitoxin | Monitor kadar obat untuk penyesuaian penaikan dosis | |
| Quinidine | Monitor kadar obat untuk penyesuaian penaikan dosis | |
| Mexiletine, tocainide, propafenone | Monitor secara klinis, mungkin harus mengganti obat. | |
| Theophylline | Theophylline | Monitor kadar obat untuk penyesuaian penaikan dosis |
| Sulfonilurea | Tolbutamide, chlorpropamide, glyburide, glimepiride, repaglinide Simvastatin, | Monitor kadar glukosa darah, mungkin membutuhkan penambahan dosis atau penggantian obat. |
| Antilipid | Simvastatin, fluvastatin | Monitor kadar lipid, mungkin membutuhkan penggantian obat. |
| Psikotropik | Nortriptyline | Memerlukan monitoring kadar obat untuk meningaktkan dosis atau mengganti obat. |
| Haloperidol, quetiapine | Monitor secara klinis, mungkin harus menaikan dosis atau mengganti obat. | |
| Benzodiazepin (misalnya diazepam, triazolam, zolpidem, buspiron) | Monitor secara klinis, mungkin harus menaikan dosis atau mengganti obat. |
Efek induktif dari rifamycin ini muncul 1-2 minggu setelah steady state dan dampaknya hilang 2 minggu setelah pemberian rifamycin dihentikan. Jika sebelumnya dosis obat dinaikan untuk kompensasi pemberian RIF, maka dosis tersebut juga harus diturunkan dalam waktu 2 minggu setelah RIF dihentikan.
RFB dapat diberikan untuk menggantikan RIF jika interaksi obat tidak dapat ditoleransi seperti antara RIF dengan cyclosporine dan kebanyakan protease inhibitor HIV-1. Semua rifamycin dapat menyebabkan penurunan dramatis konsenterasi beberapa obat seprti itraconazole.
Interaksi Obat Akibat INH
INH memiliki sifat inhibitor yang relatif poten terhadap beberapa isoenzim CYP sehingga dapat meningkatkan konsenterasi beberapa obat sampai ke tahap munculnya toksisitas seperti antikonvulsan fenitoin dan karbamazepin. INH juga meningkatkan konsenterasi benzodiazepin yang dimetabolisme melalui proses oksidasi seperti diazepam dan triazolam namun tidak mempengaruhi obat yang dimetabolisme oleh konjugasi seperti oxazepam. Efek induktif RIF pada isoenzim mengalahkan efek inhibitor dari INH sehingga pemberian OAT menurunkan konsenterasi fenitoin dan diazepam.
INH juga dapat meningkatkan toksisitas obat lain seperti asetaminiofen, asam valproat, dan teofilin. Tetapi, efek klinis interaksi ini belum sepenuhnya dipelajari. Interaksi INH dengan disulfiram awalnya dicurigai namun pada penelitian retrospektif didapat bahwa disulfiram aman diberikan secara bersamaan dengan OAT yang mengandung INH yang diberikan secara intermiten.
Interaksi Obat Akibat Fluoroquinolon
Ciprofloxacin dapat menghambat metabolisme dari teofilin dan dapat menyebabkan toksisitas teofilin namun levofloxacin, gatifloxacin, dan moxifloxacin tidak mempengaruhi metabolisme teofilin.
Monitoring Kadar Obat
Monitoring kadar obat biasanya berupa pengukuran kadar obat dalam serum yang dilakukan pada 2 dan 6 jam setelah obat diberikan. Sampel darah diambil dan dilakukan sentrifugasi kemudian serum diambil untuk dibekukan. Monitoring kadar obat ini tidak bisa memperkirakan pasien mana yang akan gagal terapi, relaps, atau sembuh. Tetapi, pemeriksaan ini bermanfaat dalam memberi informasi dalam situasi tertentu.
Pemeriksaan kadar obat dalam darah biasanya berguna dalam situasi misalnya malabsoprsi obat, dosis yang kurang, atau dimana terjadi kecurigaan terjadi interaksi obat. Pada kasus tuberkulosis, monitoring kadar obat dilakukan misalnya dalam keadaan:
- Pasien dengan konversi sputum yang lambat yang tidak dapat dijelaskan oleh ketidakpatuhan atau resistensi obat
- Pasien dengan kondisi medis khusus yang disangkakan menyebabkan kadar obat subterapeutik atau konsenterasi toksik
- Pasien yang menjalani pengobatan untuk tuberkulosis resisten obat.
Tatalaksana Kondisi Khusus pada Tuberkulosis
Beberapa kondisi klinis khusus memerlukan perhatian dan penanganan yang khusus. Berikut ulasannya:
Koinfeksi HIV dan Tuberkulosis
Pada penderita HIV, dikarenakan kondisi imunitas yang lemah, maka sangat rentan terkena tuberkulosis. Selain itu, pada HIV, progresivitas penyakit TB juga berlangsung lebih cepat. Salah satunya karena kuman MTB dapat berkembang biak lebih banyak di tubuh penderita HIV. Dikarenakan kondisi imunitas yang relatif lemah ini, terdapat beberpa perbedaan pengobatan tuberkulosis pada penderita HIV yakni sebagai berikut:
Durasi OAT pada Koinfeksi TB/HIV
Dalam kondisi koinfeksi HIV/TB, pada pasien yang diberikan ARV lebih awal, pemberian OAT dapat diberikan selama 6 bulan (2 bulan fase intensif, 4 bulan fase lanjutan). Apabila akibat suatu kondisi ARV tidak diberikan, maka disarankan untuk menambah fase lanjutan 3 bulan (total 9 bulan).
Perbedaan lainnya adalah pemberian OAT pada fase lanjutan. Pemberian OAT pada fase lanjutan biasanya intermiten 3 kali seminggu. Namun, pada koinfeksi HIV/TB, pemberian intermiten ini meningkatkan relaps sehingga disarankan pada fase lanjutan, pemberian OAT tetap diberikan tiap hari pada pasien koinfeksi HIV/TB.
Waktu Mulai Pemberian ARV pada Koinfeksi TB/HIV dan Immune Reconstitution Inflammatory Syndrome (IRIS)
Apabila pada saat diketahui ada koinfeksi HIV/TB dan pasien masih belum mendapatkan ARV, maka pemberian ARV adalah sebagai berikut:
- CD4 <50 sel/μL ARV diberikan dalam 2 minggu setelah dimulainya pemberian OAT.
- CD4 ≥50 sel/μL, maka ARV diberikan dalam 8-12 minggu setelah dimulainya pemberian OAT.
Perlu ditambahkan pula bahwa pada pasien koinfeksi HIV/TB terdapat risiko terjadinya immune reconstitution inflammatory syndrome (IRIS). IRIS adalah kondisi dimana terjadi reaksi paradoksikal yakni perburukan gejala walaupun terjadi perbaikan sistem imunitas. IRIS ini terjadi lebih banyak pada kelompok dengan CD4 <50 sel/μL.
Gejala dari IRIS dapat berupa demam tinggi, sesak memberat, peningkatan ukuran radang, limfadenopati baru, menambahnya ukuran lesi intrakranial, atau peningkatan efusi dan abses. Untungnya kebanyakan IRIS ringan dan cukup OAT maupun ARV dapat terus dilanjutkan dengan tambahan obat antiinflamasi seperti ibuprofen.
Untuk kasus efusi atau abses bertambah mungkin perlu dilakukan drainase. Adapun pada IRIS berat, dapat diberikan steroid. Pada penelitian dengan IRIS sedang, pemberian prednison 1,25 mg/kg BB secara signifikan mengurangi gejala IRIS. Prednison ini dapat diberikan selama 2-4 minggu dengan periode tapering 6-12 minggu atau lebih lama. Pengecualian pemberian ARV ini pada kasus meningitis TB dimana ARV tidak diberikan pada 8 minggu setelah dimulai diberikannya OAT.
Penyesuaian Dosis ARV saat Diberikan Bersama dengan OAT
Dikarenakan rifampycin merupakan induser dari enzim metabolisme hati dan banyak ARV dimetabolisme di hati, maka pada penggunaan ARV bersama-sama dengan OAT memerlukan perhatian. Perhatian tersebut berupa ada obat yang tidak bisa diberikan bersamaan dengan RIF dan ada pula yang memerlukan penyesuaian dosis. Untuk kemungkinan interaksi tersebut, perhatikan tabel di bawah ini:
| Kelas ARV | Keterangan |
|---|---|
| Protease inhibitor HIV-1 (lopinavir/ritonavir, darunavir/ ritonavir, atazanavir, atazanavir/ritonavir | Lebih baik gunakan RFB. Pada regimen /r, RFB 150 mg per hari. Dosis ganda LPV/r bisa digunakan jika menggunakan RIF namun kemungkinan toksisitas bertambah. Jangan gunakan RIF dengan PI lainnya |
| NNRTI Nevirapine Efavirenz Rilpivirine Etravirine | RIF mengurangi paparan pada semua NNRTI. Pada nevirapine dengan RIF, dosis awal naikan dari 200 mg menjadi 400 mg. Pada penggunaan RIF dengan efavirenz, berikan dosis standar 600 mg walaupun ada yang menyarankan naikan menjadi 800 mg pada orang dengan BB >60 kg. Rilpivirine dan etravirine tidak boleh dipakai bersamaan dengan RIF. RFB dapat diberikan bersamaan dengan nevirapine dan etravirine pada dosis biasa. Pada evafirenz dan RFB naikan dosis RFB sampai 600 mg sehari. Rilpivirine tidak boleh dipakai bersamaan dengan RFB |
| INSTI Raltegravir Dolutegravir Elvitegravir | Naikan dosis raltegravir sampai 800 mg dua kali sehari dengan RIF walaupun data klinis menunjukan efektivitas setara pada pemberian 400 mg dua kali sehari. Dosis dolutegravir harus dinaikan menjadi 50 mg tiap 12 jam dengan RIF. Jangan memakai RIF bersamaan dengan elvitegravir. Semua INSTI dapat dipakai bersamaan dengan RFB |
| Inhibitor CCR5 Maraviroc | Maraviroc tidak dipakai bersamaan dengan RIF, bisa bersamaan dengan RFB. |
Tatalaksana Tuberkulosis Ekstraparu
Tuberkulosis dapat menyerang organ atau jaringan mana saja. Prinsip pengobatannya pada dasarnya sama dengan pengobatan TB paru. OAT untuk TB ekstraparu dimulai dengan fase intensif dengan INH, RIF, PZA, dan EMB selama dua bulan. Selanjutnya diberikan terapi fase lanjutan dengan INH dan RIF. Dari data penelitian didapat bahwa fase lanjutan 6-9 bulan efektif untuk mayoritas kasus TB ekstraparu. Pengecualiannya adalah meningitis tuberkulosa dimana durasi optimal terapi belum dikonfirmasi melalui sebuah uji klinis acak tersamar ganda. Namun para ahli banyak yang memberikan terapi dengan durasi 12 bulan. Selain itu, untuk dosis OAT fase lanjutan dianjurkan adalah yang harian dibandingkan pemberian secara intermiten.
Terapi dengan kortikosteroid dimulai secara intravena secepatnya pada tuberkulosis ekstraparu tertentu, kemudian disulih oral tergantung perbaikan klinis. Rekomendasi kortikosteroid yang digunakan adalah deksametason 0,3-0,4 mg/kg di tapering-off selama 6-8 minggu atau prednison 1 mg/kg selama 3 minggu, lalu tapering-off selama 3-5 minggu. Evaluasi pengobatan TB ekstra paru dilakukan dengan memantau klinis pasien, tanpa melakukan pemeriksaan histopatologi ataupun biakan.
Tatalaksana Limfadenitis TB
Pemberian regimen pengobatan selama 6 bulan cukup untuk pengobatan limfadenitis TB. Selama pengobatan, regio KGB yang tekena dapat membesar dan nodul baru dapat muncul namun biasanya tanpa bukti adanya relaps bakteriologis. Selain pemberian OAT, terapi pembedahan umumnya tidak lazim dilakukan.
Eksisi terapeutik KGB tidak direkomendasikan kecuali pada kondisi yang tidak biasa. Pada nodul yang berfluktuasi dan hampir pecah dapat dilakukan aspirasi walaupun ada laporan bahwa insisi dan darinase pada limfadenitis servikal justru memperpanjang terbukanya luka dan menambah jaringan parut. Di luar negeri yaitu Amerika Serikat, kasus limfadenitis pada anak akibat mycobacteria lebih banyak disebabkan oleh mycobacteria non-TB.
Tatalaksana Tuberkulosis Tulang, Sendi, dan Spondilitis TB
Pemberian OAT yang mengandung RIF selama 6-9 bulan sama efektifnya dengan OAT tanpa RIF selama 18 bulan untuk pengobatan tuberkulosis pada tulang, sendi, dan spinal. Pada kasus ini terdapat kesulitan terutama menilai respon terapi. Dikarenakan demikian, maka biasanya lebih dipakai regimen yang lebih lama yaitu 9 bulan dan bahkan ada yang memberikan sampai 12 bulan.
Pada kasus spondilitis TB tanpa komplikasi, biasanya cukup diberikan terapi medis yaitu OAT. Namun terapi pembedahan diperlukan dalam kondisi berikut ini:
- Respon buruk terhadap OAT dengan bukti adanya perburukan gejala infeksi
- Mengurangi kompresi ke sumsum tulang belakang terutama pada pasien yang memiliki keluhan atau defisit neurologis yang persisten atau berulang
- Terdapat instabilitas spinal
Kasus spondilitis TB dengan adanya bukti meningitis diperlakukan sama dengan mengitis TB termasuk pertimbangan untuk memberikan terapi kortikosteroid adjungktif.
Tatalaksana Perikarditis Tuberkulosa
Untuk pemberian OAT, pemberian 6 bulan pada penelitian cukup untuk kasus perikarditis TB. Sebelumnya pada semua kondisi perikarditis tuberkulosa diberikan pemberian steroid. Akan tetapi, pada uji klinis ditemukan bahwa pemberian secara umum kortikosteroid tidak memberi manfaat lebih dibandingkan dengan palsebo.
Walaupun demikian, dari analisis subgrup ditemukan bahwa keuntungan pemberian kortikosteroid dapat mencegah perikarditis konstriktif. Oleh sebab itu, pemberian kortikosteroid tidak diberikan secara umum pada perikarditis tuberkulosa namun pada kondisi terpilih yaitu pada pasien yang memiliki risiko tinggi komplikasi inflamasi.
Kondisi risiko tinggi komplikasi inflamasi tersebut misalnya pada efusi yang besar, hasil analisa cairan menunukan tingginya petanda dan sel radang, dan tanda awal perikarditis konstriksi.
Tatalaksana Pleuritis TB
Untuk pleuritis TB, pemberian regimen standar 6 bulan juga cukup pada penanganan kasus ini. Adapun pemberian kortikosteroid tidak terbukti bermanfaat sehingga tidak rutin diberikan. Pada kasus dengan empiema, pengobatan harus disertai dengan pemasangan drainase pleura dan kadang memerlukan intervensi bedah. Sayangnya, pada kasus empiema TB, durasi optimal pemberian OAT masih belum diketahui.
Tatalaksana Meningitis Tuberkulosa
Sampai saat ini, meningitis TB masih menjadi momok yang besar dengan tingkat mortalitas dan morbiditas yang tinggi baik pada pasien dewasa maupun anak. Infeksi HIV merupakan faktor risiko yang meningkatkan kejadian meningitis TB. Mortalitas jangka pendek sama antara penderita HIV/TB dengan penderita TB tanpa HIV. Tetapi, kesintasan 9 bulan pada pasien dengan HIV dan menderita meningitis TB lebih kecil dibandingkan penderita tanpa HIV.
Pemberian pengobatan meningitis tuberkulosa dimulai dengan kombinasi INH, RIF, PZA, dan ethionamide di fase inisial 2 bulan pertama. Setelah itu diikuti dengan fase lanjutan INH dan RIF selama 7-10 bulan. Namun, fase lanjutan yang optimal sebenarnya masih belum diketahui.
Pemeriksaan pungsi lumbal terutama pada awal pemberian terapi dianjutkan untuk menilai respon pengobatan. Pemeriksaan ini menilai perubahan jumlah sel, glukosa, dan protein cairan serebrospinal.
Selain OAT, pemberian kortikosteroid memberikan keuntungan. Oleh sebab itu, disamping OAT ditambahkan pula kortikosteroid berupa deksametason atau prednisolon selama pemberian OAT dan di-tapering off dalam 6-8 minggu. Rekomendasi dosis kortikosteroid yang digunakan adalah deksametason 0,3-0,4 mg/kg di tapering-off selama 6-8 minggu atau prednison 1 mg/kg selama 3 minggu, lalu tapering-off selama 3-5 minggu.
Tatalaksana Tuberkulosis Diseminata
Maksud TB diseminata adalaj kondisi tuberkulosis yang menyerang lebih dari satu tempat atau terdapat TB milier. Pada kondisi ini pemberian regimen OAT 6 bulan dianggap cukup. Dalam kasus TB diseminata dengan gejala pernapasan yang berat atau munculnya insufisiensi adrenal maka diperlukan pemberian terapi adjungtif berupa kortikosteroid. Untuk TB diseminata dengan keterlibatan saraf pusat maka penatalaksanaannya mengikuti penatalaksanaan untuk meningitis TB.
Tatalaksana TB Genitourinaria
TB pada ginjal cukup diterapi dengan terapi medis dengan pemberian OAT regimen 6 bulan. Indikasi bedah misalnya jika terjadi obstruksi saluran kemih. Nefrektomi dilakukan jika ginjal tidak berfungsi terutama jika ada hipertensi dan nyeri pinggang yang persisten.
Tatalaksana TB Abdomen dan Saluran Cerna
Pada kasus peritonitis TB atau TB usus, pemberian OAT selama 6 bulan dianggap sudah cukup. Terkadang diberikan pula pemberian kortikosteroid untuk mencegah perlengeketan pada peritonitis TB. Tetapi, data yang mendukung pemberian kortiksoteroid ini pada TB abdominal masih terbatas sehingga pemberiannya tidak disarankan dilakukan secara rutin.
Tatalaksana Tuberkulosis dengan Biakan MTB Negatif
Jika pada pemeriksaan radiologis sugestif tuberkulosis namun tidak ditemukan MTB pada sputum atau biakan tetap tidak menyingkirkan seseorang menderita tuberkulosis. Penyebab hasil bakteriologi yang negatif ini adalah jumlah bakteri yang rendah, spesimen sputum yang tidak adekuat, perubahan variasi jumlah MTB yang dikeluarkan, adanya tumbuh bakteri lain yang berlebihan di media biakan, dan kesalahan pemrosesan spesimen.
Pengobatan bisa lebih pendek namun tetap diberikan fase intensif 2 bulan dan fase lanjutan 4 bulan. Adapun penilaian respon pengobatan adalah dengan membandingkan pemeriksaan radiologis secara serial (2-3 bulan setelah dimulai pengobatan).
Sebenarnya panjangnya fase pengobatan yang optimal pada kelompok pasien tuberkulosis dengan biakan MTB negatif belum diketahui. Terdapat data bahwa pemberian regimen empat bulan sudah cukup untuk mengobati kondisi ini. Namun, jika terdapat kekhawatiran pemberian regimen 4 bulan tidak adekuat, maka pemberian regimen standar 6 bulan juga dapat dibenarkan.
Tuberkulosis pada Kehamilan dan Ibu Menyusui
Pemberian OAT diberikan segera terutama jika tuberkulosis tersebut mengancam kesehatan ibu dan janin. Walaupun OAT melintasi sawar darah pasenta, namun dari penelitian tidak didapat efek teratogenik dari OAT lini pertama terhadap janin. Namun, terdapat kekhawatiran akan pemberian PZA pada kehamilan terutama di negara Amerika Serikat. Jika dengan alasan tertentu PZA tidak dapat diberikan, maka pemberian regimen OAT diperpanjang minimal menjadi 9 bulan.
Pada wanita menyusui, adanya OAT pada ASI juga tidak menjadi masalah yang serius. Tidak lupa pada pemberian INH juga disertakan pemberian piridoksin 25-50 mg/hari terutama pada ibu hamil dan menyusui.
Tuberkulosis pada Penderita CKD atau Penyakit Ginjal Kronik
Dalam kondisi penurunan fungsi ginjal seperti pada penyakit ginjal kronik atau CKD, kadang diperlukan penyesuaian dosis. Berikut paparannya:
- Rifampisin: Diekskresikan terutama oleh hati namun 30% diekskresikan lewat ginjal. Namun, pada kondisi CKD tidak diperlukan penyesuaian dosis
- Isoniazid: Sama seperti rifampisin, diekskresikan terutama di hati sehingga tidak perlu penyesuaian dosis.
- Pirazinamid: Disekresikan terutama lewat hati namun ada yang disekresikan lewat ginjal. Selain itu, obat ini bisa menyebabkan hiperurisemia yang juga merupakan masalah pada kondisi CKD. Oleh sebab itu, direkomendasikan diberikan secara intermiten 25-35 mg/kg/hari tiga kali per minggu. Dosis maksimum 1,5 g untuk individu dengan berat 50 kg ke bawah dan 2 g untuk berat badan >50 kg. Pada pasien dialisis, pirazinamid diberikan setelah dialisis
- Ethambutol: Obat ini terutama dieksresikan di ginjal sehingga penggunaannya sebaiknya dihindari pada CKD. Namun, dalam kondisi khusus seperti kasus resisten, obat ini dapa diberikan dengan pengawasan ketat terutama dengan pemeriksaan mata yang rutin. Dosis yang diberikan pada CKD adalah:
- Bersihan kreatinin 50-100 mL/mnt 25 mg/kg/hari tiga kali seminggu
- Bersihan kreatinin 30-50 mL/mnt dua kali seminggu
- Bersihan kreatinin 10-30 mL/mnt 15 mg/kg/hari tiap 36-48 jam
- Hindari penggunaan jika bersihan kreatinin <10 mL/mnt
- Streptomisin: Diberikan hanya jika bisa monitoring kadar obat dalam darah dengan dosis 12-15 mg/kg/hari tiga kali seminggu setelah dialisis.
| Obat | Perubahan Frekuensi | Dosis dan frekuensi pemberian jika CrCl <30 mL/menit atau pasien hemodialisis |
|---|---|---|
| Isoniazid | Tidak | 300 mg sekali sehari atau 900 mg 3 kali/mgg |
| Rifampin | Tidak | 600 mg sekali sehari atau 600 mg 3 kali/mgg |
| Pyrazinamide | Ya | 23-35 mg/kg/dosis 3 kali/mgg |
| Ethambutol | Ya | 20-25 mg/kg/dosis 3 kali/mgg |
| Levofloxacin | Ya | 750-1000 mg/dosis 3 kali/mgg |
| Moxifloxacin | Tidak | 400 mg sekali sehari |
| Cycloserine | Ya | 250 mg sekali sehari atau 500 mg/dosis 3 kali/mgg |
| Ethionamide | Tidak | 250-500 mg/dosis per hari |
| Para-amino salicylic acid | Tidak | 4 g/dosis dua kali sehari |
| Streptomycin | Ya | 15 mg/kg/dosis 2-3 kali/mgg |
| Capreomycin | Ya | 15 mg/kg/dosis 2-3 kali/mgg |
| Kanamycin | Ya | 15 mg/kg/dosis 2-3 kali/mgg |
| Amikacin | Ya | 15 mg/kg/dosis 2-3 kali/mgg |
Tuberkulosis dengan Penyakit Hati/Liver Kronis
Pengobatan tuberkulosis pada pasien yang sebelumnya memiliki penyakit hati berat memberi tantangan tersendiri. Seperti dijelaskan sebelumnya bahwa OAT memiliki efek samping berupa DILI (lihat di atas). Kemungkinan terjadinya efek samping ini meningkat pada orang yang memiliki penyakit hati lanjut, menjalani transplantasi hati, atau infeksi hepatitis C. Peningkatan enzim transaminase sendiri pun merupakan prediktor independen terhadap terjadinya DILI. Oleh sebab itu, pada pasien tuberkulosis juga disarankan untuk sebelumnya dilakukan pemeriksaan ALT, hepatitis B (HBsAg), dan hepatitis C (anti-HCV).
Bagi pasien yang memiliki kapasitas fungsi hati yang menurun, jika terjadi DILI maka dapat berupa reaksi berat yang bisa sampai mengancam nyawa. Selain itu, monitoring terjadinya DILI juga cukup sulit karena bisa saja kenaikan transaminase dan bilirubin tidak disebabkan oleh DILI tetapi oleh kondisi penyakit hati kronis yang pasien miliki sebelumnya. Bahkan, pada TB diseminata, kenaikan transaminase bisa disebabkan oleh hepatitis TB yang tentu akan membaik jika diberikan OAT.
Untuk menghindari perburukan fungsi hati serta menurunkan risiko DILI, maka pada pasien yang memiliki kadar ALT >3 kali batas atas normal dipilih OAT dengan potensi hepatotoksisitas yang rendah. Dikarenakan pentingnya posisi INH dan RIF maka kedua obat ini sebisa mungkin tetap diberikan. Regimen OAT alternatif yang dapat diberikan pada kondisi penyakit hati kronis adalah sebagai berikut:
- Regimen tanpa PZA. Regimen yang mungkin adalah INH, RID, dan EMB untuk 2 bulan dan diikuti dengan INH dan RIF selama 7 bulan.
- Regimen tanpa RIF dan PZA. Regimen ini untuk pasien dengan penyakit hati lanjut. Regimen terdiri dari RIF dan EMB diserta fluoroquinolon injeksi atau cycloserine selama 12-18 bulan, tergantung dari luasnya penyakit dan respon pengobatan.
- Regimen tanpa INH. Regimen ini berdasarkan pada penelitian TB resisten INH. OAT yang diberikan terdiri dari RIF, PZA, dan EMB dengan atau tanpa fluoroquinolon dengan total durasi setidaknya 6 bulan. Walaupun tetap ada dua obat dengan potensi hepatotoksisitas, namun durasi yang pendek (6 bulan) menjadi keuntungan tersendiri.
- Regimen tanpa obar dengan potensi hepatotoksisitas. Regimen ini untuk pasien dengan penyakit hati berat dan tidak stabil. Regimen dapat berupa EMB kombinasi dengan fluoroquinolon, cycloserine, dan obat injeksi lini kedua lainnya.
Untuk monitoring kondisi pasien dengan penyakit hati yang berat dan menerima OAT, disarankan untuk melakukan pemeriksaan aminotransferase (AST/ALT) dan bilirubin tiap 1-4 minggu pada 2-3 bulan pertama pengobatan. INR juga dapat diperiksa untuk melihat kondisi pasien dengan penyakit hari berat. Peningkatan ALT lebih spesifik untuk petanda kerusakan hati dari pada peningkatan AST. Peningkatan AST dapat juga terjadi akibat abnormalitas pada otot, jantung, atau ginjal.
Pada pasien dengan sirosis atau ensefalopati hepatikum, kadar ALT yang ditetapkan untuk dihentikannya pemberian OAT belum ditentukan. Namun, ahli menyarankan dihentikan jika terjadi kenaikan ALT setidaknya 3 kali walaupun tanpa gejala. Dikarenakan banyaknya perhatian yang harus diberikan, pemberian OAT pada pasien dengan gangguan hati sebaiknya dilakukan di fasilitas lengkap dan memiliki ahli multidisiplin.
Tuberkulosis pada Pasien Geriatri
Dikarenakan penurunan fungsi ginjal dan hati pada populasi lanjut usia, maka kemungkinan munculnya efek samping akan meningkat. Pemberian OAT harus mempertimbangkan tingkat keparahan penyakit dan risiko pemberian obat. PZA biasanya menjadi obat yang banyak menimbulkan efek samping khususnya DILI pada lansia. Oleh sebab itu, jika tuberkulosis yang diderita keparahannya ringa-sedang dan risiko resistensi rendah, maka pada fase intensif pada lansia usia >75 tahun hanya diberikan INH, RIF, dan EMB. Tetapi, untuk fase lanjutannya dilanjutkan lebih panjang sehingga durasi pengobatan menjadi 9 bulan.
Pada kondisi dimana jumlah kuman tinggi (misalnya kavitasi bilateral) maka risiko gagal terapi dan resistensi tinggi. Di kondisi tersebut, pemberian PZA atau fluoroquinolon menjadi lebih urgen sehingga tetap diberikan fase intensif dengan kombinasi empat obat. Selain itu, dikarenakan pada lansia sering didapatkan komorbid, maka perhatian terhadap interaksi obat juga penting dilakukan.
TB dengan Komorbid Lain
Selain komorbid atau keadaan khusus yang dibahas di atas, banyak komorbid atau penyakit lain yang sering muncul atau didapat bersamaan dengan tuberkulosis. Pada dasarnya, regimen standar 6 bulan dapat memberi efek terapi yang memadai. Namun, keputusan untuk menambah waktu fase lanjutan juga dapat dilakukan sesuai dengan kondisi individu dari pasien ke pasien.
Pada diabetes melitus tidak terkontrol misalnya, beberapa ahli menyarankan untuk pemberian OAT sampai 9 bulan. Begitu juga dengan kondisi lain misalnya silikotuberkulosis, penambahan fase lanjutan 2 bulan dapat meningkatkan respon terapi OAT. Hal yang sama juga tampak pada penerima transplantasi organ solid dimana pemberian OAT 9 bulan dapat mengurangi angka mortalitas.
Dalam kondisi immunosupresi lainnya misalnya pada pasien dengan penyakit autoimun yang menerima terapi imunosupresan dan terkena TB, harus dipertimbangkan antara risiko dan benefit penundaan atau pengurangan dosis obat imusupresan tersebut. Misalnya pada kondisi klinis autoimun yang stabil, pemberian inhibitor TNF-α sebaiknya ditunda sebisa mungkin jika terdapat tanda atau kecurigaan tuberkulosis. Namun, data menunjukan pemberian TNF-α dapat diberikan pada pasien TB yang stabil dan telah menerima OAT setidaknya selama 2 bulan dan berespon baik terhadap terapi OAT. Perlu ditambahkan reaksi IRIS-like berat dapat terjadi saat penghentian terapi TNF-α.
Pada pasien penerima transplantasi organ padat, OAT khususnya RIF sering berinteraksi terutama dengan calcineurin inhibitor (cyclosporine, tacrolimus, dan pimecrolimus) atau rafamycin (sirolimus). Dalam kondisi ini, monitoring kadar obat diperlukan untuk menjaga agar tidak terjadi reaksi rejeksi organ transplan.
Tuberkulosis pada Anak
Tuberkulosis pada anak biasanya merupakan lanjutan atau komplikasi dari TB primer. Gambaran radiologis dari TB primer pada anak berupa limfadenopati intratorakal dengan atau tanpa opasitas atau infiltrat paru. Biasanya berupa pembesaran kelenjar getah bening yang dapat menyebabkan kompresi saluran napas dengan atau tanpa adanya atelektasis atau hiperinflasi dari lobus paru.
Apabila ada pecahnya kelenjar getah bening yang berisi tuberkel ke saluran napas, dapat bermanifestasi sebagai infiltrat lobaris atau segmental dan dapat pula berupa pola milier. Oleh sebab itu, gambaran radiologis tuberkulosis pada anak tidak berupa adanya kavitas seperti orang dewasa.
Diagnosis TB pada Anak
Pada dasarnya, diagnosis tuberkulosis pada anak cukup sulit terutama pada balita karena sifat penyakit yang pausibasiler pada kondisi tersebut. Diagnosis mikrobiologis pada anak hanya dapat dilakukan pada 15-50% kasus TB anak sehingga diagnosis tuberkulosis pada anak biasanya berupa diagnosis klinis. Adapun di Indonesia memakai sistem skoring sebagai berikut:
| Parameter | Skor 0 | Skor 1 | Skor 2 | Skor 3 |
|---|---|---|---|---|
| Kontak TB | Tidak jelas | Laporan keluarga, BTA(-)/BTA tidak jelas/tidak tahu | BTA (+) | |
| Uji Tuberkulin (Mantoux) | Negatif | Positif (≥10mm atau ≥5 mm pada imuno-kompromais) | ||
| Berat badan | BB/TB<90% | Klinis gizi buruk atau BB/TB<70% atau BB/U<60% | ||
| Demam yang tidak diketahui penyebabnya | ≥ 2 minggu | |||
| Batuk kronik | ≥ 2 minggu | |||
| Pembesaran kelenjar limfe kolli, aksila, inguinal | ≥1 cm, lebih dari 1 KGB, tidak nyeri | |||
| Pembengkakan tulang/sendi panggul, lutut, falang | Ada | |||
| Fototoraks | Normal kelainan tidak jelas | Sugestif TB |
Setelah menghitung skor di atas, maka kemudian mengikuti alur diagnosis berikut ini:

Walaupun demikian, anak-anak usia lebih tua misalnya remaja juga dapat memberikan gambaran tuberkulosis seperti dewasa (opasitas lobus paru atas dan kavitasi yang disertai produksi dahak atau sputum).
Untungnya, lesi pada TB primer mengandung lebih sedikit kuman MTB dibandingkan tipe TB pada dewasa. Oleh karenanya, kejadian gagal terapi, relaps, dan munculnya resistensi primer atau sekunder lebih jarang terjadi pada anak ketika terapi standar diberikan.
OAT pada TB Anak
Adapun regimen standar bagi anak WHO menyarankan fase intensif 2 bulan yang terdiri dari INH, RIF, PZA, dan EMB diikuti dengan fase lanjutan 4 bulan berupa INH dan RIF. Namun, dikarenakan kekhawatiran toksisitas EMB terutama karena anak-anak sulit untuk menilai visus, terkadang pada fase intensif hanya diberikan INH, RIF, dan PZA. Namun, dikarenakan adanya potensi resistensi, regimen standar dengan 4 obat tetap direkomendasikan untuk kasus TB anak.
Piridoksin atau vitamin B6 juga diberikan dengan dosis 25-50 mg/hari terutama pada bayi, anak, dan remaja yang mendapat terapi INH jika terdapat defisiensi gizi, infeksi HIV simtomatik, atau bayi yang menerima ASI. Piridoksin juga diberikan pada ibu menyusui yang mendapatkan INH.
Namun, dengan sulitnya mendapat spesimen kuman, seringkali pemeriksaan resistensi pada kasus TB anak didapat dari spesimen orang dewasa yang dicurigai menjadi sumber penularan dari infeksi anak tersebut. Selain itu, cara isolasi kuman MTB dari anak apabila sangat diperlukan dapat diambil dari bilasan lambung pagi tiga kali, induksi, lavage bronkoalveolar, atau biopsi jaringan.
Selain diagnosis, monitoring terapi pada anak juga cukup sulit dilakukan. Perubahan gambaran radiologis tidak bisa diandalkan. Pembesaran KGB hilar memerlukan waktu 1-2 tahun untuk mengecil sehingga memandu pemanjangan terapi OAT pada anak yang sudah tidak bergejala kurang dapat dijustifikasi. Biasanya, perkembangan pertumbuhan anak yang baik sesuai usia menandakan efek positif terapi OAT.
Pada kasus TB ekstraparu pada anak, biasanya dapat diberikan terapi dengan durasi 6 bulan. Pengecualian pada meningoensefalitis TB dan TB osteoartikular. Pada meningitis TB, regimen OAT berupa INH, RIF, PZA, dan aminoglikosida atau ethionamide selama 2 bulan diikuti 7-10 bulan INH dan RIF. Pada daerah dengan resistensi terhadap streptomycin yang tinggi, disarankan untuk menggunakan aminoglikosida lain yaitu kanamycin, amikacin, atau capreomycin.
Peran Kortikosteroid pada TB Anak
Kortikosteroid dapat digunakan untuk TB dengan komplikasi seperti meningitis TB, sumbatan jalan napas akibat TB kelenjar, dan perikarditis TB. Steroid dapat pula diberikan pada TB milier dengan gangguan napas yang berat, efusi pleura dan TB abdomen dengan asites. Obat yang sering digunakan adalah prednison dengan dosis 2 mg/kg/ hari, sampai 4 mg/kg/hari pada kasus sakit berat, dengan dosis maksimal 60 mg/hari selama 4 minggu, kemudian tappering off bertahap 12 minggu sebelum dilepas.
Neonatus yang Lahir dari Ibu Penderita TB
ASI tetap diberikan, dengan ibu memakai masker untuk pencegahan, serta prinsip PPI secara umum Bayi tidak perlu dipisahkan dari ibu, bayi tetap disusui langsung, tetapi ibu harus memakai masker untuk mencegah penularan TB pada bayinya. Pada ibu yang sangat infeksius (BTA positif) dan kondisi klinis yang berat, bayi dipisahkan sampai terjadi konversi BTA sputum atau ibu tidak infeksius lagi, tetapi tetap diberikan ASI yang dipompa.
Jika neonatus tersebut tidak memiliki gejala (asimtomatik), dan ibunya terbukti TB yang sensitif dengan OAT, maka neonatus diberikan terapi pencegahan dengan isoniazid (10mg/kg) selama 6 bulan.Neonatus harus dipantau secara rutin setiap bulan, dan dievaluasi kemungkinan adanya gejala TB untuk memastikan TB aktif tidak berkembang.
Pada akhir bulan ke 6, bila bayi tetap asimptomatik, pengobatan dengan INH distop dan dilakukan uji tuberkulin. Jika uji tuberkulin negatif dan tidak terinfeksi HIV, maka dapat diberikan BCG 2 minggu setelahnya, Akan tetapi jika uji tuberkulin positif, harus dievaluasi untuk kemungkinan sakit TB.
Jika ibu terbukti tidak terinfeksi dan sakit TB, bayi harus diskrining TB.Jika tidak ada bukti infeksi TB, maka bayi harus dipantau secara teratur untuk memastikan penyakit TB aktif tidak berkembang.Jika diagnosis TB sudah dikonfirmasi atau bayi menunjukkan tanda klinis sugestif TB, pengobatan harus dimulai oleh dokter spesialis anak. Imunisasi BCG diberikan 2 minggu setelah terapi jika bayi tidak terinfeksi HIV.Jika terinfeksi HIV, BCG tidak diberikan. Neonatus yang lahir dari ibu yang MDR atau XDRTB harus dirujuk, pencegahaan dan pengendalian infeksi dengan ibu menggunakan masker.
Resistensi MTB terhadap OAT (TB MDR/XDR)
Akhir-akhir ini resistensi MTB terhadap OAT menjadi masalah tersendiri. Dengan adanya bakteri resisten, selain menyulitkan penyembuhan juga menambah jangka lama pengobatan serta biaya pengobatan. Terdapat dua kelompok besar MTB resisten yaitu MDR dan XDR.
MDR adalah MTB yang resisten terhadap rifampicin dan isoniazid. Sedangkan XDR adalah MDR yang juga resisten terhdap fluorokuinolon dan satu obat lain yang masuk ke dalam kelompok OAT lini kedua. Pada kedua kasus ini, pengobatan bisa memakan waktu 1,5 sampai 2 tahun.
Mekanisme Terjadinya Resistensi MTB terhadap OAT
Secara singkat, mekanisme resistensi kuman MTB terhadap antibiotika dapat di simak di bagan berikut ini:

Diagnosis TB Resisten Obat
Pemeriksaan laboratorium untuk uji kepekaan M. tuberculosis dilakukan dengan metode standar yang tersedia di Indonesia yaitu metode fenotipik dan metode genotipik.
Metode Fenotipik
Menggunakan media padat (Lowenstein Jensen / LJ) atau media cair (mycobacteria growth indicator tube / MGIT). Saat ini program TB menggunakan paket standar uji kepekaan yang menguji 5 (lima) obat berikut:
- INH (dosis rendah dan dosis tinggi)
- Ofloksasin / Levofloksasin
- Kanamisin
- Kapreomisin
- Moksifloksasin (dosis rendah dan dosis tinggi)
Tes Genotipik
Menggunakan Xpert MTB/RIF atau lebih dikenal dengan tes cepat molekuler (TCM):
- Merupakan tes amplifikasi asam nukleat secara otomatis sebagai sarana deteksi TB dan uji kepekaan untuk rifampisin.
- Hasil pemeriksaan dapat diketahui dalam waktu kurang lebih 2 jam
Menggunakan line probe assay (LPA):
- Dikenal sebagai Hain test/Genotype MTBDR plus (LPA lini pertama) dan MTBDRsl (LPA lini kedua). LPA lini pertama dapat mendeteksi resistansi terhadap obat rifampisin dan isoniazid. Sedangkan LPA lini kedua untuk mendeteksi resistansi pada obat golongan flurokuinolon dan obat injeksi lini kedua. Saat ini program TB hanya menggunakan LPA lini kedua.
- Hasil pemeriksaan dapat diperoleh dalam waktu kurang lebih 48 jam. Laboratorium LPA akan melakukan pemeriksaan LPA sebanyak satu sampai dua kali dalam seminggu agar lebih efisien. Sehingga turn around time (TAT) pemeriksaan LPA adalah 5 hari kerja
Hasil Pemeriksaan LPA lini dua dapat menunjukan :
- Mycobacterium tuberculosis (MTB) atau non-tuberculosis mycobacterium (NTM)
- Sensitif atau resistan fluorokuinolon
- Sensitif atau resistan obat injeksi lini kedua
Alur Diagnostik dan Pengobatan TB Resisten Obat
Berikut adalah alur penatalaksanaan TB resisten obat:

Panduan Pengobatan TB-RO dengan Paduan Jangka Pendek
Paduan pengobatan jangka pendek diberikan pada pasien TB-RR sesuai dengan kriteria yang terdapat pada alur di atas. Adapun jenis obat dan durasi pengobatan jangka pendek

- Durasi total pengobatan adalah 9–11 bulan, durasi tahap awal adalah 4–6 bulan dan tahap lanjutan 5 bulan
- Intoleransi Z tidak boleh mendapatkan paduan jangka pendek.
- Intoleransi / resistansi terhadap E, paduan jangka pendek diberikan tanpa Etambutol
- Capreomisin dapat menggantikan kanamisin apabila muncul efek samping di dalam masa pengobatan. Mengingat ketersediaan capreomisin yang terbatas, maka penggunaannya harus berkordinasi dengan tim logistik MTPTRO.
Adapun dosis obat berdasarkan pengelompokan berat badan dapat dilihat pada tabel berikut:
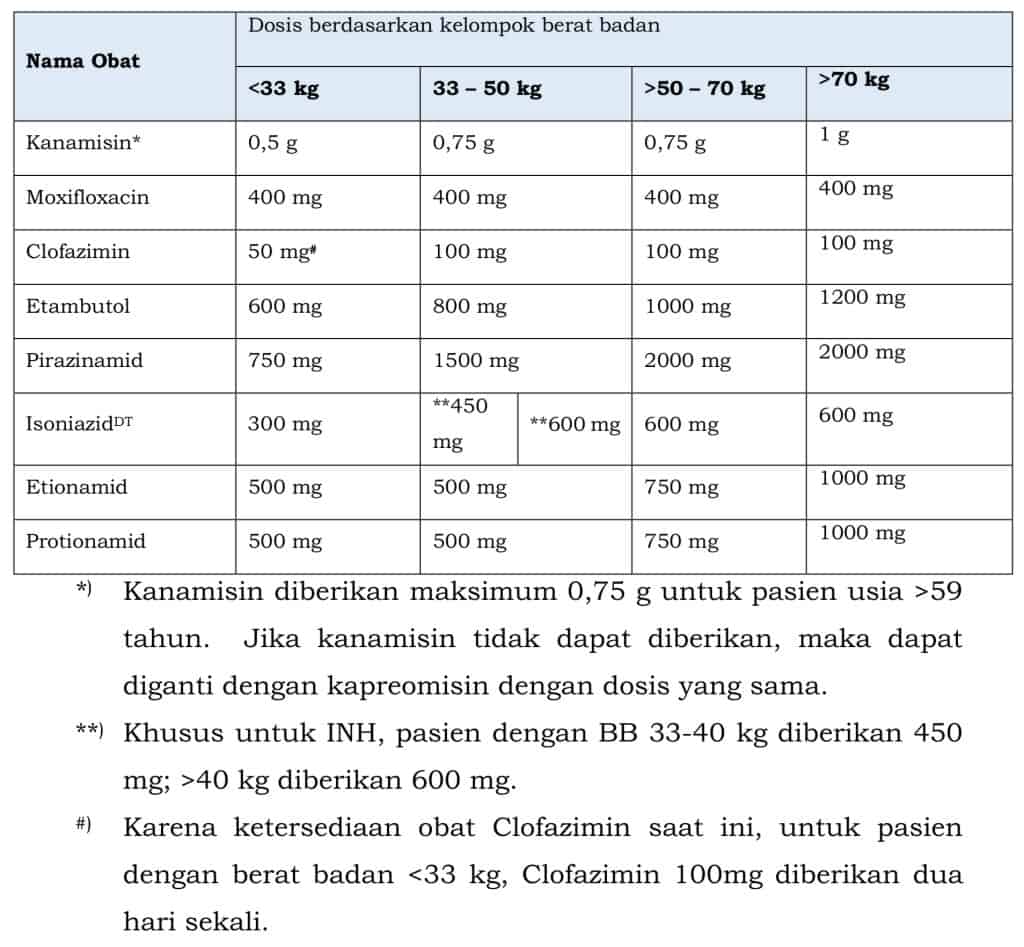
Cara pemberian obat:
- Pasien akan mendapatkan pengobatan paduan jangka pendek selama minimal 9 bulan, terdiri dari 4 bulan fase awal dan 5 bulan fase lanjutan.
- Pada tahap awal, obat oral dan injeksi diberikan setiap hari (7 hari, Senin s.d Minggu) selama 4 bulan dan pada tahap lanjutan, obat oral diberikan setiap hari (7 hari, Senin s.d Minggu).
- Satuan bulan yang dimaksud adalah bulan sesuai kalender (30 hari)
- Pada keadaan dimana tidak terjadi konversi BTA pada bulan ke-4, tahap awal diperpanjang menjadi 6 bulan sehingga durasi total pengobatan menjadi 11 bulan (6 bulan tahap awal dan 5 bulan tahap lanjutan). Pada bulan ke-5 dan ke-6, obat injeksi diberikan 3x seminggu (intermiten) dan obat oral tetap diberikan setiap hari (7 hari, Senin s.d Minggu).
Panduan Pengobatan TB-RO dengan Paduan Jangka Panjang/Individual
Pasien TB RO yang tidak memenuhi kriteria untuk pengobatan dengan paduan jangka pendek akan mendapatkan paduan pengobatan individual. Paduan individual diberikan untuk pasien:
- TB pre-XDR
- TB-XDR
- MDR dengan intoleransi terhadap salah satu atau lebih obat lini kedua yang digunakan pada paduan jangka pendek
- Gagal pengobatan jangka pendek
- Kembali setelah putus berobat
- TB-MDR kambuh
Untuk pengobatan, OAT lini kedua dikelompokan menjadi 3 kelompok sebagai berikut:
| Kelompok | Jenis Obat |
|---|---|
| Kelompok A | Levofloxacin (Lfx) atau Moxifloxacin (Mfx) Bedaquiline (Bdq) Linezolid (Lzd) |
| Kelompok B | Clofazimine (Cfz) Cycloserine (Cs) atau Terizidone (Trd) |
| Kelompok C | Ethambutol (E) Delamanid (Dlm) Pyrazinamide (Z) Imipenem-cilastatin (Ipm-Cln) atau meropenem (Mpm) Amikacin (Am) atau Streptomycin (S) Ethionamide (Eto) atau Prothionamide (Pto) p-aminosalicylic acid (PAS) |
Rekomendasi untuk paduan individual untuk TB-MDR.
- Pada pasien MDR / RR-TB yang memakai Paduan Individual (ITR):
- Pengobatan dimulai dengan setidaknya lima obat TB yang diperkirakan efektif dan setidaknya terdapat tiga obat untuk sisa perawatan setelah bedaquiline dihentikan
- Paduan pengobatan terdiri dari tiga obat dalam Grup A dan dua obat dari Grup B. Misal : 6 Bdq – Lfx – Lnz – Cfz-Cs // 14 Lfx – Lnz – Cfz-Cs
- Jika paduan tidak dapat dibentuk dengan obat dari Grup A dan B saja, obat dari Grup C ditambahkan untuk melengkapi paduan pengobatan. Misal : 6 Bdq – Lfx – Cfz – Cs – E // 14 Lfx – Cfz – Cs – E
- Kanamycin dan capreomycin tidak dimasukkan dalam paduan pengobatan Pasien MDR / RR-TB yang memakai ITR
- Levofloxacin atau moxifloxacin harus dimasukkan dalam pengobatan pasien MDR / RR-TB pada paduan pengobatan jangka panjang (rekomendasi kuat)
- Bedaquiline harus dimasukkan dalam paduan pengobatan TB-MDR jangka panjang untuk pasien berusia 18 tahun atau lebih (rekomendasi kuat).
- Bedaquiline juga dapat dimasukkan dalam paduan pengobatan TB-MDR jangka panjang untuk pasien berusia 6-17 tahun.
- Linezolid harus dimasukkan dalam pengobatan pasien MDR / RR-TB pada paduan pengobatan TB-MDR jangka panjang (rekomendasi kuat).
- Clofazimine dan cycloserine dapat dimasukkan dalam pengobatan pasien MDR / RR-TB yang menggunakan paduan TB RO jangka panjang.
- Etambutol dapat dimasukkan dalam pengobatan pasien MDR / RR-TB dengan paduan TB RO jangka panjang.
- Delamanid dapat dimasukkan dalam pengobatan pasien MDR / RR-TB berusia 3 tahun atau lebih dengan rejimen yang lebih lama.
- Pyrazinamide dapat dimasukkan dalam pengobatan pasien MDR / RR-TB dengan rejimen yang lebih lama.
- Amikacin dapat dimasukkan dalam pengobatan pasien MDR / RR-TB berusia 18 tahun atau lebih dengan paduan pengobatan jangka panjang jika terbukti masih susceptible/sensitif dan terdapat SPO yang memadai untuk monitoring ESO.
- Jika amikasin tidak tersedia, streptomisin dapat menggantikan amikasin dalam kondisi yang sama
- Ethionamide atau prothionamide hanya dapat dimasukkan dalam pengobatan pasien TB-MDR / RR yang memakai paduan pengobatan TB-MDR jangka panjang jika bedaquiline, linezolid, clofazimine atau delamanid tidak digunakan atau jika tidak ada pilihan untuk membuat rejimen yang lebih baik.
- Durasi pengobatan paduan individual tanpa injeksi
- Tidak ada tahap awal
- Lama pengobatan setelah konversi 15 bulan
- Total lama pengobatan 18 – 20 bulan
- Durasi pengobatan dengan injeksi Amikasin/Streptomicin
- Lama tahap awal dengan suntikan 6 bulan
- Lama pengobatan setelah konversi 15 bulan
- Total lama pengobatan 18 – 20 bulan
| Paduan jangka panjang | Tahap awal | Total lama pengobatan | Pemberian setelah konversi (n) |
|---|---|---|---|
| Dengan injeksi Am/S | 6 bulan | Min. 20 bulan | 16 bulan |
| Tanpa injeksi atau tanpa BDQ/DLM | Min. 20 bulan | 16 bulan | |
| Dengan BDQ/DLM | Min. 20 bulan | 16 bulan | |
| TB RO pada anak | 18–20 bulan | ||
| TB RO ekstra paru | Min. 20 bulan |
| Bulan konversi | Lama pengobatan setelah konversi | Total lama pengobatan |
|---|---|---|
| 1 | 15 | 18 |
| 2 | 15 | 18 |
| 3 | 15 | 18 |
| 4 | 15 | 19 |
| 5 | 15 | 20 |
| 6 | 15 | 20 |
- Pemberian paduan individual berdasarkan kelompok pasien
- TB MDR maupun TB pre-/XDR. Paduan pengobatan jangka panjang akan lebih efektif bila disusun berdasarkan hasil uji kepekaan obat. Untuk obatobat yang belum dapat dilakukan uji kepekaan (seperti Bdq, Lzd, Cfz) keputusan pemberian obat dapat didasarkan pada riwayat pengobatan pasien dan data surveilans.
- TB RR. Pasien TB RR tanpa resistansi INH dapat dioabati dengan paduan jangka panjang atau paduan jangka pendek. Meskipun INH dosis tinggi tidak lagi masuk dalam kelompok obat TB RO yang direkomendasikan, INH masih dapat diberikan bila terbukti sensitif.
- TB RO pada anak. Bdq direkomendasikan untuk anak >6 tahun, sementara Dlm untuk anak >3 tahun. Dosis Dlm untuk anak 3-5 tahun ialah 25 mg, sehingga diperlukan pembelahan tablet. Pemberian Dlm yang dibelah ataupun digerus dapat menyebabkan perubahan bioavailabilitas obat dan dosis yang tidak sesuai. Pemberian obat injeksi dapat menyebabkan gangguan pendengaran yang berdampak pada kemampuan bicara dan belajar. Audiometri rutin perlu dilakukan pada anak yang mendapatkan obat injeksi. Hasil studi menunjukkan pemberian INH dosis tinggi berhubungan dengan keberhasilan pengobatan pada anak dengan TB MDR.
- TB RO ekstra paru dan meningitis. Paduan pengobatan jangka panjang dapat diberikan pada pasien TB RO ekstra paru dan TB RO meningitis, dimana penyesuaian dosis mungkin diperlukan bergantung lokasi penyakit. Pengobatan TB RO meningitis terbaik ialah sesuai dengan hasil uji kepekaan dan kemampuan obat menembus blood-brain barrier (BBB). Obat yang dapat berpenetrasi baik ke system saraf pusat ialah Levofloxacin, Moxifloxacin, Etionamide/Protionamide, Sikloserin/Terizidone, Linezolid dan Imipenem-Silastatin. INH dosis tinggi dan Pirazinamid juga dapat mencapai kadar terapeutik dalam cairan serebrospinal dan dapat digunakan bila masih sensitif. PAS dan Etambutol tidak dapat menembus BB dan tidak dihitung sebagai obat meningitis untuk TB meningitis. Amikasin dan Streptomisin hanya dapat masuk ke otak bila terdapat peradangan meningeal. Data terkait kemampuan penetrasi Bdq, Dlm, dan Clofazimine ke otak masih terbatas.
- TB RO dengan kehamilan. Obat yang dikontraindikasikan pada kehamilan ialah Amikasin, Streptomisin, serta Eto/Pto. Data keamanan Bdq dan Dlm pada kehamilan dan menyusui masih terbatas. Pada kehamilan direkomendasikan untuk menyusun paduan pengobatan individual dengan obat yang sudah diketahui data keamanannya.
- TB RO dengan HIV. Interaksi obat yang perlu dihindari pada pasien HIV ialah Bdq dan Efavirenz.
Tuberkulosis (TB) Laten
Indonesia merupakan salah satu negara endemis tuberkulosis. Sebagian besar yang terinfeksi tidak mengalami gejala dan kelompok ini dinamakan penderita tuberkulosis laten. Dari penderita tuberkulosis laten ini sekitar 5-10% akan berprogresi menjadi tuberkulosis aktif. Sebagian besar kasus tuberkulosis yang kita lihat sehari-hari 80% merupakan penderita tuberkulosis laten yang berprogresi menjadi tuberkulosis aktif.
Dalam membuktikan seseorang merupakan penderita TB laten maka seseorang tidak terdapat tanda dan gejala klinik dengan gambaran foto toraks normal serta hasil uji imunologik seperti uji tuberkulin atau interferon gamma release assay (IGRA) positif.
Uji tuberkulin dilakukan dengan menyuntikan intradermal 0,1 ml PPD 5 TU dengan teknik Mantoux selanjutnya pembacaan hasil uji tuberkulin dilakukan dalam 48-72 jam oleh tenaga kesehatan terlatih. Pemeriksaan IGRA yang dapat digunakan saat ini adalah 2 jenis pemeriksaan IGRA yaitu: quantiFERON®-TB Gold-in-Tube test (QFT-GIT) plus dan T-SPOT®.TB
Untuk sebagian besar kasus TB laten tidak diobati. Akan tetapi, pada kelompok yang berisiko besar berprogresi menjadi TB aktif, maka pasien tersebut akan diobati. Pengobatan TB laten efektif menghambat progresi ke arah TB aktif.
WHO merekomendasikan pengobatan TB Laten di negara berpendapatan rendah atau sedang atau sumber daya terbatas pada anak usia dibawah 5 tahun yang kontak dengan pasien TB dan pasien HIV. Pengobatan diberikan setelah dilakukan evaluasi klinik dengan cermat dan tidak ditemukan TB aktif.
CDC merekomendasikan regimen terapi TB laten sebagai berikut:
| Prioritas | Regimen | Rekomendasi | Level Bukti |
|---|---|---|---|
| Diutamakan | 3 bln INH plus rifapentine sekali seminggu | Kuat | Moderat |
| Diutamakan | 4 bln rifampin setiap hari | Kuat | Moderat (HIV negatif)* |
| Diutamakan | 3 bln INH plus rifampin setiap hari | Kondisional | Sangat rendah (HIV negatif) Rendah (HIV positif) |
| Alternatif | 6 bln INH setiap hari | Kuat** Kondisional | Moderat (HIV negatif) Moderate (HIV positif) |
| Alternatif | 9 bln INH setiap hari | Kondisional | Moderat |
| Obat | Durasi | Dosis dan kelompok usia | Frekuensi | Dosis total |
|---|---|---|---|---|
| INH dan RPT | 3 bln | Dewasa dan anak ≥ 12 tahun INH: 15 mg/kg dibulatkan ke 50 atau 100 mg terdekat; maksimum 900 mg. Rifapentine: – 10-14 kg, 300 mg – 14,1-25 kg, 450 mg – 25,1-32 kg, 600 mg – 32,1-49,9 kg, 750 mg – ≥50 kg, maksimum 900 mg Anak usia 2-11 tahun INH: 25 mg/kg; maks 900 mg Rifapentine seperti di atas | Sekali seminggu | 12 |
| Rifampin | 4 bln | Dewasa: 10 mg/kg Anak: 15-20 mg/kg* Dosis maks: 600 mg | Sekali sehari | 120 |
| INH dan RIF** | 3 bln | Dewasa INH: 5 mg/kg; maks 300 mg RIF: 10 mg/kg; maks 600 mg Anak INH: 10-20 mg/kg**; maks 300 mg RIF: 15-20 mg/kg; maks 600 mg | Sekali sehari | |
| INH | 6 bln | Dewasa: 5 mg/kg Anak: 10-20 mg/kg** Maks: 300 mg | Sekali sehari | 180 |
| Dewasa: 15 mg/kg Anak: 20-40 mg/kg** Maks: 900 mg | Dua kali seminggu | 52 | ||
| 9 bln | Dewasa: 5 mg/kg Anak: 10-20 mg/kg** Maks: 300 mg | Sekali sehari | 270 | |
| Dewasa: 15 mg/kg Anak: 20-40 mg/kg** Maks: 900 mg | Dua kali seminggu | 76 |
Vaksin BCG dan Pencegahan Infeksi Tuberkulosis
Pencegahan dilakukan dengan cara non-spesifik, vaksin, maupun dengan medikamentosa. Cara profilaksis non spesifik adalah dengan isolasi, pemberian terapi adekuat pada pasien TB aktif, dan desinfeksi adekuat terutama di rumah sakit. Desinfeksi dapat dicapai dengan menggunakan cairan desinfektan yang mengandung asam karbolat 5% atau yang mengandung klorin.
Vaksin BCG
BCG merupakan vaksin pertama dan masih menjadi satu-satunya vaksinasi terhadap MTB. Vaksin ini mengandung strain avirulen dari M. bovis yang pertama kali ditemukan oleh Calmette dan Guerrin dengan melakukan biakan M. bovis dalam media empedu minimal selama 13 tahun. Vaksinasi BCG diberikan pada bayi neonatus usia 3 – 5 hari. Vaksinasi ini dapat mengurangi risiko terkena penyakit tuberkulosis sebanyak 50%.
Terapi Preventif
Pada kelompok berisiko, dapat diberikan pemberian terapi profilaksis. Pemberian terapi profilaksis ini untuk penderita HIV atau penurunan imunitas yang terpapar TB. Skenarionya sebagai berikut:
| Skenario | Regimen profilaksis |
|---|---|
| Sensitif INH | INH 300 mg PO qd + piridoksin 25 mg PO qd x 6-9 bulan atau regimen kombinasi (INH + rifapentine) 12 minggu |
| HIV positif | INH 300 mg PO qd + piridoksin 25 mg PO qd x 9 bulan |
| Kontak dengan kasus resisten INH | RIF x 4 bulan |
| Kontak dengan kasus dugaan atau konfirmasi TB MDR | Tidak ada regimen yang terbukti: PZA + EMB, PZA + FQ |
Profil Obat Anti-Tuberkulosis (OAT)
Pada bagian ini akan dibahas mengenai profil farmakokinetik dan farmakodinamik masing-masing dari antibiotika yang digunakan dalam regimen OAT.
Ringkasan Mekanisme Kerja OAT
Di bawah ini adalah ringkasan mengenai target OAT lini pertama:
| Antibiotik | Target obat |
|---|---|
| Isoniazid | InhA; KatG (aktivasi) |
| Rifampicin | RpoB |
| Ethambutol | EmbB |
| Pyrazinamide | RpsA; PncA (aktivasi) |
| Streptomycin | RpsL |
| Amikacin, kanamycin, capreomycin | Subunit 30S ribosom atau interbridge |
| Ethionamide | InhA; EthA (aktivasi) |
| Cyclosperine | D-alanin racemase dan ligase |
| Fluoroquinolon | GyrA |
| Para-aminosalicylic acid | Dihydropteroate synthase; metabolisme folat |

Rifamycin (Rifampicin/Rifampin [RIF], Rifabutin [RBT], dan Rifapentine [RPT])
Rifamycin merupakan antibiotika makrolida dengan struktur grup chromophoric naphthohydroquinone yang terbentang dari jembatan panjang alifatik dengan grup asetil di C25 (gambar di bawah). Anggota prototip dari rifampycin adalah rifampin dengan rifapentine dan rifabutin yang merupakan derivat dari rifampin

Mekanisme kerja dari rifamycin adalah dengan mengikat ke RNA polimerase dependen DNA subunit β (rpoB) membentuk struktur kompleks obat-enzim yang stabil. Pembetukan struktur ini akan menghentikan kerja RNA polimerase sehingga sintesis RNA terhenti. Selain terhadap MTB, RIF juga aktif menghambat pertumbuhan bakteri gram positif maupun gram negatif.
Prevalensi isolat MTB resisten terhadap RIF sekitar 1 tiap 107 sampai 108 basil. Mekanisme resisten adalah karena perubahan struktur dari rpoB dengan 86% resistensi akibat mutasi di kodon 526 dan 531 dari gen rpoB. Monoresistensi terhadap RIF meningkat pada pasien dengan koinfeksi HIV/TB dan TB paru dengan multikavitas yang diobati dengan RPT atau RBT.
RIF diabsorpsi di saluran cerna dengan berbagai tingkat absorpsi. Absorpsi RIF dihambat oleh makanan sampai 1/3-nya. Adapun absoprsi RPT ditingkatkan oleh makanan tinggi lemak (meningkatkan AUC). Untuk RBT absorpsinya di saluran cerna tidak dipengaruhi oleh makanan.
Rifamycin dimetabolisme oleh B-esterase mikrosomal dan kolinesterase yang menghilangkan gugus asetil di posisi 25 sehingga menghasilkan 25-O-desacetyl rifamycin. RIF juga dihidrolisis menjadi 3-formil rifampin sedangkan RPT dihidrolisis menjadi 3-formil rifapentine dan 3-formil-25-O-desacetyl rifapentine. Jalur mayor eliminase RBT adalah melalui CYP3A.
Ketiga obat ini mengalami autoinduksi dimana AUC menurun seiring pemberian berulang obat-obatan tersebut. Semua rifamycin dapat berpenetrasi ke banyak jaringan namun kadar di CNS hanya ~5% kadar plasma akibat aktivitas P-glycoprotein. Obat dan metabolitnya diekskresikan melalui sistem bilier dan feses dengan jalur urin berkontribusi dari kurang dari 1/3 proses eliminasi.
Isoniazid
Isoniazid atau hidrazida asam isonikotinat merupakan molekul kecil yang larut air yang memiliki struktur berkaitan dengan pyrazinamide (lihat gambar di bawah).

Obat isoniazid masuk ke bakteri melalui proses difusi pasif. INH tidak toksik secara langsung terhadap baskteri namun terlebih dahulu harus diubah di dalam basil oleh KatG. KatG merupakan enzim katalase-peroksidase multifungsi dan merubah isoniazid menjadi bentuk radikal isonicotinoyl yang berinteraksi dengan NAD dan NADP bakteri membentuk berbagai produk gabungan. Salah satu produk gabungan ini adalah isomer nicotinoyl-NAD yang menghambat aktivitas enoyl acyl carrier protein reductase (InhA) dan β-ketoacyl acyl carrier protein synthase (KasA). Penghambatan kedua protein ini akan mengganggu sintesis asam mikolat dan menyebabkan kematian bakteri. Produk adduct lain isomer nicotinoyl-NADP berpotensi menghambat dihydrofolate reductase bakteri sehingga dapat mengganggu proses sintesis asam nukleat.
Produk lain dari aktivasi KatG termasuk superoksida, H2O2, alkil hidroksiperoksida, dan radikal NO juga berkontribusi terhadap efek mikobakterisidal dari INH. MTB dapat lebih sensitif pada kerusakan radikal bebas ini karena basil MTB memiliki defek pada regulatoe pusat respon terhadap stres oksidatif, oxyR. Sistem pertahanan cadangan terhadap radikal ini diperankan oleh alkyl hydroxyperoxide reductase (dikodekan oleh ahpC) yang mendetoksifikasi peroksida organik yang berbahaya tadi. Peningkatan ekspresi dari ahpC akan mengurangi efektivitas dari INH.
Resitensi terhadap INH juga terjadi saat terjadi mutasi atau delesi dari gen KatG, overekspresi dari gen InhA dan ahpC, serta mutasi dari kasA. Mutan KatG memiliki sifat sangat resisten terhadap INH.
Ethambutol
Obat ini adalah sintetik congener dari 1,2-ethanediamine yang aktif terhadap MTB, M. bovis, dan beberapa mycobacteria nonspesifik. Ethambutol cepat diserap di saluran cerna, mencapai konsenterasi puncak dalam 2-4 jam dan paru eliminasi 3-4 jam. Ekskresi ethambutol adalah di urin baik dalam bentuk tidak diubah atau berupa metabolit inaktif hasil metabolisme di hati. Sekitar 20% ethambutol diekskresikan di feses dalam bentuk tanpa perubahan.

Ethambutol menghambat arabinosyl transferase III yang mengganggu transfer arabinosa ke arabinolactan sehingga menghambat pembentukan dinding sel. Enzim arabinosyl transferase dikodekan oleh enzim embAB.
Pyrazinamide
Pyrazinamide merupakan pyrazine sintetik analog nikotinamid. Nama lain dari pyrazinamide adalah asam amida pyrazinoat, pyrazine carbocylamide, dan pyrazinecarboximide. Pyrazinamide bersifat bakterisidal lemah terhadap MTB namun memiliki aktivitas sterilisasi terutama di tempat dengan suasana asam seperti lingkungan intraseluler di makrofag. Oleh sebab itu, obat ini adalah satu-satunya antibiotik yang dapat mempengaruhi bentuk intraseluler dari MTB.

Pyrazunamide diaktivasi oleh suasana lingkungan atau milieu asam. Awalnya dianggap bahwa kondisi asam dimana pyrazinamide diaktivasi adalah di dalam makrofag. Namun kita tahu ternyata pyrazinamide tidak terlalu efektif di dalam makrofag. Kondisi asam yang mengaktivasi pyrazinamide lebih karena lingkungan di pinggkir kavitas yang mengalami nekrosis saat sel inflamasi memproduksi asam laktat.
Saat masuk ke dalam bakteri, nikotinamidase atau pyrazinamnidase dari MTB akan mendeaminasi pyrazinamide menjadi asam pirazinoat. Asam pirazinoat (POA–) ini kemudian ditranspor oleh pompa efluks ke milieu ekstraseluler. Di lingkungan ekstraseluler yang asam, sebagian POA– akan terprotonisasi menjadi POAH. POAH memiliki sifat lebih lipofilik dan akan masuk kembali ke basil MTB.
POAH ini didalam MTB akan membunuh bakeri. Mekanisme pastinya tidak diketahui namun diperkirakan melalui proses berikut:
- Penghambatan jerha asam lemak sinthase tipe I yang menyebabkan terganggunya produksi asam mikolat
- Menurunkan pH intrasel
- Mengganggu membran transpor
Obat ini sangat efektif terutama di dua bulan pertama pengobatan saat proses peradangan berlangsung. Penggunaan pirazinamid memungkinkan regimen terapi dengan durasi lebih pendek dan risiko relaps juga berkurang.
Kontraindikasi dari pyrazinamide adalah adanya alergi serta fungsi hati yang memburuk. Pada pasien diabetes, pemakaian pyrazinamide harus disertai monitoring gula darah karena dapat menyebabkan turun naik kadar glukosa darah. Selain itu, obat ini juga dapat menyebabkan timbulnya serangan gout.
Mekanisme terjadinya resistensi MTB terhadap pyrazinamide adalah karena berkurangnya afinitas pyrazinamidase bakteri terhadap pyrazinamide. Berkurangnya afinitas ini akan menurunkan konversi pyrazinamide menjadi POA. Penurunan afinitas ini berhubungan dengan mutasi single point dari gen pncA yang ditemukan pada 70% isolat MTB yang resisten. Adapun mekanisme resistensi pada 30% sisanya masih belum diketahui.
Aminogliksida: Streptomycin, Amikacin, dan Kanamycin
Secara umum aminoglikosida memiliki struktur gula amino yang berikatan dengan cincin aminocyclitol. Dikarenakan molekul amonoglikosida berupa polikation, semua obat ini dapat diserap di saluran cerna sehingga harus diberikan secara parenteral, sulit menembus sawar darah otak, dan diekskresikan secara cepat oleh ginjal.
Streptomycin merupakan kelompok antibiotik aminoglikosida yang didapat dari derivat Streptomyces griseus. Pada kelompok kanamycin (termasuk kanamycin A dan B, amikacin, dan tobramycin), dua gula amino terikat ke moietas 2-deoxystreptamine yang terletak di tengah-tengah. Salah satu dari gula amino tersebut adalah 3-aminoheksosa. Sedangkan amikacin merupakan derivat dari kanamycin A melalui asilasi dari grup 1-amino pada moietas 2-deoxystreptamine dengan asam 2-hydroxy-4-aminobutirat.

Sifat aminoglikosida adalah bakterisidal dengan sifat concentration dependent. Antibiotika ini menembus membran sitoplasma bagian luar dari bakteri gram negatif, masuk ke ruang periplasmik. Dari ruang periplasmik, aminoglikosida harus ditranspor secara aktif ke dalam sitoplasma. Proses ini dihambat oleh kation divalen, hiperosmolaritas, pH rendah, dan kondisi anaerob. Di dalam sel, aminoglikosida kemudian akan mengikat polisom dan mengganggu sintesis protein dengan menyebabkan kesalahan pembacaan serta terminasi prematur dari translasi mRNA.
Mekanisme resistensi bakteri terhadap aminoglikosida dapat melalui beberapa mekanisme:
- Berkurangnya kemampuan obat menembus membran plasma bakteri
- Inaktivasi obat oleh enzim
- Berkurangnya afintias obat terhadap polisom akibat mutasi.
Adapun proses inaktivasi obat merupakan mekanisme resistensi yang paling banyak ditemukan. Enzim yang mengaktivasi aminoglikosida dibawa oleh plasmid. Enzim ini melakukan fosforilasi, adenilasi, atau asetilasi grup hidroksi atau amino spesifik dari aminoglikosida.
Efek samping dari obat ini adalah gangguan fungsi ginjal (nefrotoksik) dan vestibular. Oleh sebab itu. tidak boleh digunakan pada gangguan pendengaran. Selain itu, kontraindikasi lain adalah adanya alergi dan myasthenia gravis. Adapun efek samping lain berupa nyeri di tempat injeksi serta dapat menimbulkan anemia hemolitik, agranulositosis, trombositopenia, dan reaksi lupoid.
Clofazimine
Clofazimine merupakan zat warna riminophenazine yang larut dalam lemak. Disamping aktivitas antimikroba, diketahui pula bahwa clofazimine memiliki aktivitas antiinflamasi dengan menghambat makrofag, sel T, neutrofil, dan komplemen. Mekanisme biokimia terhadap bakteri tidak diketahui. Namun diperkirakan melalui mekanisme berikuti ini:
- Disrupsi membran
- Inhibisi fosfolipase A2 bakteri
- Inhibisi tranpsor K+
- Pembentukan hidrogen peroksida
- Interferensi dengan rantai transpor elektron bakteri

Bioavailibilitas clofazimine bervariaasi 45-60% dan meningkat apabila dikonsumsi bersama dengan makanan tinggi lemak dan berkurang dengan antasida. Obat ini memiliki penetrasi yang baik ke berbagai jaringan dan sering menimbulkan perubahan wana pada kulit dan cairan tubuh. yang membutuhkan waktu lama untuk menghilang. Metabolisme clofazimine terjadi di hati melalui empat tahap: dehalogenasi hirolitik, deaminasi hidrolitik, glukuronidasi, dan hidroksilasi.
Fluoroquinolon
Fluoroquinolon bekerja dengan menghambat DNA girase bakteri sehingga proses sintesis DNA bakteri akan terganggu. Ofloxacin dan ciprofloxacin telah dipakai sejak lama sebagai OAT lini ledua namun penggunaannya semakin terbatas akibat meluasnya resistensi obat. Saat ini levofloxacin dan moxifloxacin meruoakan antibiotika fluoroquinolon yang dipakai sebagai OAT lini kedua.

Bedaquiline
Obat ini merupakan salah satu jenis OAT yang paling baru. Bedaquiline merupakan OAT pertama dari kelompok atau kelas obat diarylquinoline.

Mekanisme kerja dari bedaquiline adalah dengan menargetkan subunit c dari ATP synthase MTB. Hal ini akan menghambat proses pembentukan ATP atau sumber energi dari bakteri. Walaupun termasuk obat baru namun resistensi terhadap bedaquiline sudah teridentifikasi. Resistensi terjadi akibat mutasi D32V dan A63P dari gen yang mengkodekan domain subunit c ATP synthase.

Efek samping yang sering didapat adalah mual ringan-sedang dan diare. Gejala efek samping adalah nyeri sendi, nyeri pada ekstremitas, dan dapat menyebabkan hiperurisemia. Selain itu, bedaquilie dapat berpotensi menimbulkan prolongasi QT pada jantung sehingga harus berhati-hati dipakai bersama-sama obat lain yang dapat memperpanjanga durasi QT.
Delamanide
Delamanide merupakan molekul nitroimidazopyran yang strukturnya memiliki keterkaitan dengan metronidazole. Obat ini menghambat sintesis asam mikolat dan protein di langkah antara hydroxymycolata dengan ketomycolate. Selain itu, obat ini dapat menghasilkan spesies nitrogen reaktif yang merusak komponen bakteri akibat proses reaksi radikal bebas.

Ethionamide
Ethionamid merupakan kongener dari thioisonicotinamide. Di dalam bakteri enzim EthA (monooksigenase spesifik NADPH yang mengandung FAD) akan mengubag ethionamide menjadi bentuk sulfoksida dan kemudian menjadi 2-ethyl-4-aminopyridine. Semua produk molekul ini tidak toksis terhadap mycobacteria namun bentuk intermediet dari molekul turunannya diperkirakan memiliki aktivitas antibiotik.

Ethionamide menghambat pertumbuhan bakteri dengan menghambat aktivitas protein yang dihasilkan gen inhA, enoyl-ACP reduktase dari asam lemak synthase II. Hal ini akan menghambat biosintesis asam mikolat dan menghentikan pembentukan dinding sel.
Para-Amino Salicylic Acid (PAS)
PAS merupakan OAT pertama yang efektif untuk terapi TB. Obat ini ditemukan oleh Lehman tahun 1943. PAS merupakan struktur analog rai asam para-aminobenxoat yang merupakan substrat dari dihydropteroate synthase (folP1/P2). Namun, mekanisme pasti PAS menghambat metabolisme asam folat tidak diketahui dan diyakini bekerja tidak hanya menghambat metabolisme asam folat. Mutasi pada gen thyA berperan dalam sebagian kecil isolat MTB yang resisten terhadap PAS.

Cycloserine
Cycloserine atau D-4-amino-3-isoxazolidone meruapakan antibiotika spektrum luas yang dihasilkan oleh Streptococcus orchidaceous. Cycloserine dan D-alanine merupakan dua molekul yang strukturnya saling berdekatan (analog). Oleh sebab itu, cycloserine akan menghambat alanine racemase mengubah L-alanine menjadi D-alanine. Selain itu, cycloserine menghambat D-alanine ligase yang menghentikan proses pemasukan D-alanine ke proses biosintesis dinding sel. Selain pada MTB cycloserine juga aktif terhadap MAC, enterococci, E. coli, S. aureus, spesies Nocardia, dan Chlamydia.
Capremoycin
Capremomcin merupakan antibiotika antimikobakterial dengan bentuk peptida siklik. Terdiri dari empat komponen aktif yaitu capremoycin IA, IB, IIA, dan IIB. Molekul yang dipakai dalam praktek klinik terutama adalah capremomycin IA dan IB. Aktivitas antimikrobial dari capreomycin sama dengan aminoglikosida dan juga memiliki efek samping yang serupa. Obat ini tidak boleh dipakai bersama dengan obat lain yang memiliki efek samping merusak nervus kranialis NVIII.

Resistensi muncul saat capreomycin diberikan secara tungal dan juga mikroorganisme yang memiliki resistensi terhadap kanamycin dan neomycin. Efek samping yang berkaitan dengan capreomycin adalah hilangnya pendengaran, tinitus, proteinuria transien, cylindruria, dan retensi nitrogen.
Linezolid
Linezolid merupakan antibiotika golongan oxazolidinone yang menghambat sintesis protein dengan mengikat kepada RNA ribosomal (rRNA) 23S yang merupakan bagian dari subunit ribosom 50S bakteri. Obat ini biasanya digunakan untuk infeksi bakteri gram positif resisten dengan dosis 600 mg dua kali sehari.

Pada MRB, linezolid memperlihatkan aktivitas bakteriostatik in vitro termasuk ke strain XDR. Adapun pada model binatang mencit dengan tuberkolosis, obat ini hanya memberi pengaruh yang sedang. Uji klinis memperlihatkan bahwa dengan pemberian dosis 600 mg per hari yang ditambahkan pada obat-obat lainnya pada pasien dengan TB XDR, dapat membentu mencapai konversi sputum pada 6 bulan pertama pemberian.
Kesimpulan
Secara umum, tuberkulosis merupakan penyakit kronis yang dapat disembuhkan. Akan tetapi, ketidakpatuhan minum obat memunculkan masalah dengan timbulnya MTB yang resisten obat. Sampai saat ini, upaya agar pasien mendapatkan regimen OAT lengkap menjadi priotas utama untuk menyembuhkan dan mencegah masalah resistensi obat.
Referensi
- AIDS dan Infeksi HIV: Perjalanan Penyakit, Diagnosis, dan Terapi
- Bañuls A-L, Sanou A, Anh NT Van, Godreuil S. Mycobacterium tuberculosis: ecology and evolution of a human bacterium. J Med Microbiol. 2015 Nov 1;64(11):1261–9.
- Basem Abbas Al U. The Radiological Diagnosis of Pulmonary Tuberculosis (TB) in Primary Care. J Fam Med Dis Prev. 2018;4(1):1–7.
- Clemens DL. Mycobacterium tuberculosis: Bringing down the wall. Trends Microbiol. 1997;5(10):383–5.
- Ehrt S, Schnappinger D, Rhee KY. Metabolic principles of persistence and pathogenicity in Mycobacterium tuberculosis. Nat Rev Microbiol. 2018 Aug 24;16(8):496–507.
- Gagneux S. Ecology and evolution of Mycobacterium tuberculosis. Nat Rev Microbiol. 2018;16(4):202–13.
- Hegde S, Rithesh KB, Baroudi K, Umar D. Tuberculous lymphadenitis: early diagnosis and intervention. J Int oral Heal JIOH. 2014;6(6):96–8.
- Korb VC, Chuturgoon AA, Moodley D. Mycobacterium tuberculosis: Manipulator of Protective Immunity. Int J Mol Sci. 2016 Feb 25;17(3):131.
- Lee M, Lee J, Carroll MW, Choi H, Min S, Song T, et al. Linezolid for treatment of chronic extensively drug-resistant tuberculosis. N Engl J Med. 2012 Oct 18;367(16):1508–18.
- Marrakchi H, Lanéelle MA, Daffé M. Mycolic acids: Structures, biosynthesis, and beyond. Chem Biol. 2014;21(1):67–85.
- McAdam AJ, Milner DA, Sharpe AH. Infectious disease. In: Kumar V, Abbas AK, Aster JC, editors. Robbins and Cotran pathologic basis of disease. 9th ed. Philadelphia: Elsevier Saunders; 2015. p. 341–402.
- Nachiappan AC, Rahbar K, Shi X, Guy ES, Mortani Barbosa EJ, Shroff GS, et al. Pulmonary tuberculosis: Role of radiology in diagnosis and management. Radiographics. 2017;37(1):52–72.
- Nahid P, Dorman SE, Alipanah N, Barry PM, Brozek JL, Cattamanchi A, et al. Official American Thoracic Society/Centers for Disease Control and Prevention/Infectious Diseases Society of America Clinical Practice Guidelines: Treatment of Drug-Susceptible Tuberculosis. Clin Infect Dis. 2016 Oct 1;63(7):e147–95.
- Nurman J, Setyanto DB. Skrofuloderma pada Anak: Penyakit yang Terlupakan? Sari Pediatr. 2016;12(2):108.
- Park SJ, Han JK, Kim TK, Kim JS, Jung HC, Song IS, et al. Tuberculous colitis: Radiologic-colonoscopic correlation. Am J Roentgenol. 2000;175(1):121–8.
- Pedoman Nasional Pelayanan Kedokteran Kemenkes RI – Tatalaksana Tuberkulosis 2019
- Rivas-Garcia A, Sarria-Estrada S, Torrents-Odin C, Casas-Gomila L, Franquet E. Imaging findings of Pott’s disease. Eur Spine J. 2013 Jun 9;22(S4):567–78.
- Sarathy JP, Gruber G, Dick T. Re-Understanding the Mechanisms of Action of the Anti-Mycobacterial Drug Bedaquiline. Antibiotics. 2019 Dec 11;8(4):261.
- Shaw JA, Diacon AH, Koegelenberg CFN. Tuberculous pleural effusion. Respirology. 2019;24(10):962–71.
- Sterling TR, Njie G, Zenner D, Cohn DL, Reves R, Ahmed A, et al. Guidelines for the Treatment of Latent Tuberculosis Infection: Recommendations from the National Tuberculosis Controllers Association and CDC, 2020. MMWR Recomm Reports. 2020 Feb 14;69(1):1–11.
- https://pusdatin.kemkes.go.id/resources/download/pusdatin/infodatin/infodatin-tuberkulosis-2018.pdf

Seorang dokter, saat ini sedang menjalani pendidikan dokter spesialis penyakit dalam FKUI. Peminat berbagai topik sejarah dan astronomi.


Comments 3
dokter, mengapa tidak pernah upload di youtube lagi
Terima kasih dok, ilmu yang bermanfaat. Semoga tetap memberikan informasi yang up to date.
Author
Terima kasih apresianya. Jangan lupa umpan balik atau informasi jika ada bagian yang tidak tepat atau tidak up to date ya. Supaya enak bisa belajar bersama.