Fosforilasi oksidatif adalah tahapan lanjutan dari metabolisme energi secara aerob setelah glikolisis dan siklus Krebs. Tahapan ini sendiri merupakan gabungan antara rantai transpor elektron yang diikuti dengan proses kemiosmosis yang hasil akhirnya adalah ATP. Rantai transpor elektron adalah proses perubahan NADH dan FADH2 hasil dari proses sebelumnya yang dikonversi menjadi gradien atau perbedaan konsenterasi ion hidrogen antara matriks dengan ruang intermembran mitokondria. Perubahan konsenterasi ini kemudian digunakan sebagai sumber energi dalam proses kemiosmosis yang hasil akhirnya adalah ATP.
Analoginya seperti kita akan memproduksi listrik dengan menggunakan energi air. Rantai transpor elektron analoginya adalah tahap membangun bendungan sehingga terjadi perbedaan tinggi antara permukaan air di bendungan dengan sungai di bawahnya. Adapun kemiosmosis analoginya adalah perubahan energi gravitasi yang diciptakan oleh bendungan menjadi enegi listrik dengan menggunakan turbin. Adapun semua proses mulai dari membangun bendungan sampai terciptanya energi listrik dari turbin dianalogikan sebagai proses fosforilasi oksidatif. (Gambar thumbnail artikel oleh manyPictures, Pixabay)
Daftar Isi
Tahapan Kunci Fosforilisasi Oksidatif
Tahapan kunci dari proses-proses ini adalah sebagai berikut:
- Pengiriman elektron oleh NADH dan FADH2. Keduanya adalah molekul pembawa elektron hasil oksidasi proses glikolisis maupun siklus Krebs. Pada rantai transpor elektron, keduanya menyumbangkan elektron ke mekanisme rantai transpor elektron dan akan diubah kembali menjadi NADH+ dan FAD yang bisa digunakan kembali pada proses oksidasi berikutnya.
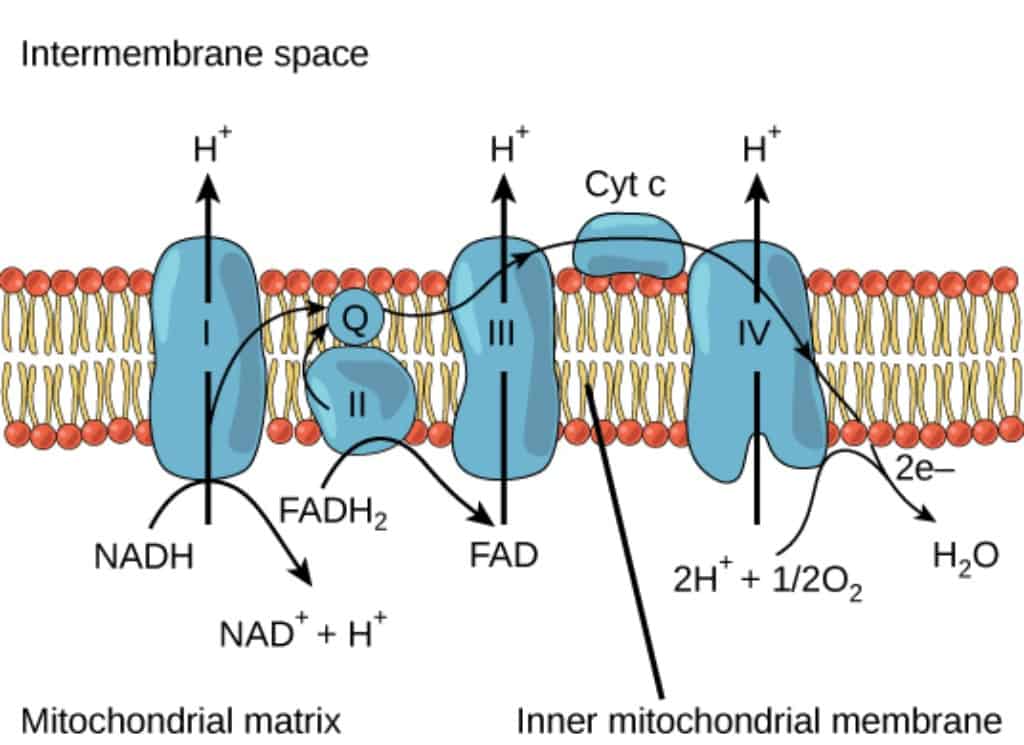
- Transfer elektron dan pompa proton. Elektron yang disumbangkan NADH dan FADH2 berupa elektron berenergi tinggi akan dipindahkan dari satu kompleks protein ke kompleks protein lain di membran dalam mitokondria. Sambil bergerak, elektron ini akan melepaskan energi. Energi yang dilepaskan digunakan untuk memompa proton atau ion hidrogen (H+) dari matriks ke ruang intermembran mitokondria. Proses ini menciptakan gradien elektrokimia.
- Pembelahan oksigen membentuk air. Setelah melewati berbagai protein, pada akhirnya elektron yang dipindahkan mengalami penuurnan tingkat energi. Di tahap akhir, elektron ini kemudian dipindahkan ke akseptor elektron terakhir yaitu berupa molekul oksigen (O2). Setelah menerima elektron, O2 terpecah menjadi dua dan masing-masing akan menghasilan molekul air (H2O).
- Sintesis ATP. Proses sebelumnya menciptakan gradien elektrokimia H+ antara matriks dengan ruang intermembran. H+ ini kemudian akan dialirkan kembali ke matriks dan proses pengaliran ini kemudian dimanfaatkan untuk mensinesis molekul ATP.
Adapun untuk secara rinci proses-proses ini akan dijelaskan lebih lanjut pada bagian artikel di bawah.
Struktur dan Fungsi Mitokondria
Untuk memahami konteks transpor elektron dan fosforilisasi oksidatif tidak bisa lepas dari pengetahuan mengenai struktur unik dari mitokondria. Mitokondria adalah organel sel yang khusus bertugas memproduksi energi. Organel ini menempati secara substansial volume sitoplasma sel eukariota. Jumlah mitokondria dalam satu sel pada tubuh manusia sangat beragam. Pada eritrosit atau sel darah merah sama sekali tidak memiliki mitokondria sehingga sepenuhnya bergantung pada proses glikolisis untuk pembentukan energi. Adapun pada sel yang aktif secara metabolisme jumlah mitokondria ini akan semakin banyak seiring tingkat aktivitas sel tersebut. Misalnya sel hati memiliki mitokondria yang menempati sekitar 20-25% volume sel atau jumahnya antara 1000-2000 mitokondria per sel. Sedangkan sel jantung yang senantiasa aktif memiliki mitokondria yang menempati 40% dari total volume sel.
Melihat dari segi jumlahnya saja jelas mitokondria penting dalam produksi energi pada eukariota. Tanpa organel ini, makhluk hidup akan hanya menggantungkan produksi energinya dari proses glikolisis secara anaerob. Namun mitokondria tidak hanya berperan dalam proses pembentukan energi. Fungsi lain seperti produksi molekul perantara yang penting dalam struktur sel serta berperan dalam proses apoptosis atau kematian sel secara terprogram.

Pada gambar di atas tampal secara skematis bentuk dasar kaitan struktur mitokondria dalam pembentukan energi di dalam sel. Secara umum bentuk mitokondria sendiri berupa silinder panjang dengan diameter 0,5 – 1 µm menyerupai bakteri. Di dalam sel, organel ini bergerak cukup aktif dan bisa berubah bentuk secara fleksibel. Di dalam sel mitokondria juga bisa bertambah atau berkurang jumlahnya sesuai dengan kebutuhan energi dari sel.
Berikut ini kita akan membahas struktur unik mitokondria, terutama yang berhubungan dengan proses pembentukan energi di dalam sel.
Struktur Membran Ganda Mitokondria
Lapisan membran ganda pada mitokondria berarti terdapat membran dalam dan membran luar. Membran luar berbatasan langsung dengan sitoplasma, ruangan antara membran luar dan membran dalam disebut ruang intermembran, sedangkan ruangan yang dilingkupi membran dalam dinamakan matriks mitokondria.

Membran luar dari mitokondria ini mengandung banyak molekul porin. Porin ini berfungsi sebagai protein transfor dengan membentuk kanal air yang besar. Molekul dengan besar 5000 Da atau kurang dapat bergerak bebas menembus membran luar ini. Sebaliknya, membran dalam memiliki sifat impermeabel. Oleh sebab itu, ruang intermembran memilki konstitusi yang mirip dengan sitoplasma.
Keberadaan membran ganda ini ternyata sangat penting dalam proses pembentukan energi di mitokondria. Dari gambar di atas, tampak bagian membran dalam yang dapat melipat yang disebut cristae. Bentuk cristae tersebut bermanfaat untuk memaksimalkan efek dari transpor elektron. Dengan adanya cristae, memungkinkan terjadi konsenterasi proton yang sangat tinggi di mitokondria. Untuk memahami proses peningkatan konsenterasi proton ini perhatikan gambar di bawah ini:

Dari gambar di atas, tampak bahwa proton (H+) dapat ditingkatkan konsenterasinya di dalam cristae. Dengan peningkatan ini, bisa didapatkan gradien kimia maupun medan listrik yang lebih kuat di dalam cristae. Hal ini akan membantu proses perubahan energi kimia dan listrik ini menjadi ATP (dijelaskan di bagian khusus di bawah).
Peran Unik Membran Dalam dan Matriks Mitokondria
Fungsi utama dari produksi energi mitokondria terutama dijalankan oleh membran dalam dan matriks dari mitokondria. Hal ini berkaitan dengan struktur membran dalam yang terspesialisasi. Membran dalam ini terdiri dari lipid bilayer yang mengandung jenis fosfolipid cardiolipin dalam proporsi besar. Kandungan ini membuat membran dalam mitokondria impermeabel atau tidak dapat ditembus terutama oleh berbagai macam ion.

Membran dalam dari mitokondria juga mengandung berbagai jenis protein yang membuat membran ini permeabel secara selektif terhadap molekul kecil yang dimetabolisme atau diperlukan oleh banyak enzim mitokondria yang terkonsenterasi di dalam matriks.
Enzim dalam matriks ini seperti enzim yang terlibat dalam proses metabolisme piruvat dan asam lemak untuk menghasilkan asetil-CoA dan juga yang dibutuhkan dalam proses oksidasi asetil-CoA pada siklus Krebs.
Seperti pada gambar di atas, membran dalam mitokondria berkelok-kelok membentuk lipatan yang dinamakan cristae. Lipatan ini menambah besar luas permukaan membran dalam mitokondria.
Materi Genetik dan Biosintesis dalam Mitokondria
Kenapa mitokondria memiliki sistem genetik terpisah? Berbeda dari organel lainnya, mitokondria adalah satu-satunya organel selain inti sel yang memiliki DNA di dalamnya. Untuk menjawab pertanyaan tersebut bukanlah hal yang mudah. Diperkirakan mitokondria dahulu adalah bakteri yang ditangkap oleh sel eukariota. Bakteri ini kemudian mengalami simbiosis mutualisma dan seiring berjalannya waktu bahkan menjadi bagian organel dari sel eukariota. Teori ini terutama berhasil menjelaskan adanya DNA di dalam mitokondria, proses pembelahan mitokondria yang berlangsung relatif independen, dan bagaimana terbentuknya membran ganda pada organel mitokondria.
Walaupun memiliki DNA tersendiri, ternyata kurang lebih 90 protein tambahan harus diimpor dari inti sel. Oleh sebab itu, untuk menjalankan fungsinya, proses biosintesis pada mitokondria memerlukan kontribusi dari dua sistem genetik yang berbeda yaitu dari inti sel dan dari mitokondria sendiri.

Protein yang diimpor ini terutama protein ribosomal, aminoacyl-tRNA synthase, DNA polimerase, RNA polimerase, dan enzim yang terlibat dalam pemrosesan dan modifikasi dari RNA. Untuk mendatangkan protein ini ternyata tidak mudah dan menyulitkan menjawab pertanyaan kenapa mitokondria memiliki DNA tersendiri.
DNA Mitokondria Manusia
Adapun DNA dari mitokondria manusia bentuk sirkuler atau lingkaran yang terdiri dari 16.569 nukleotida. Sebenarnya dibandingkan dengan DNA mitokondria makhluk hidup lain, DNA mitokondria manusia termasuk berukuran kecil. Sebagai gambaran. di bawah ini adalah skema struktur DNA mitokondria manusia serta perbandingan relatif gen DNA mitokondria manusia berbanding dengan gen mitokondria pada beberapa makhluk eukariota lainnya.


Terdapat beberapa sifat unik dari DNA mitokondria manusia dibandingkan DNA di inti sel, kloroplas, ataupun genom bakteri. Sifat unik tersebut adalah sebagai berikut:
- DNA mitokondria manusia memiliki paket gen yang padat. Tidak seperti genom di inti sel, setiap nukleotida di mitokondria manusia dikodekan dan masuk dalam sekuens gen baik untuk protein maupun satu dari rRNA atau tRNA. Dikarenakan posisi yang padat satu sama lain, hanya sedikit ruang yang dapat digunakan untuk regulasi sekuens DNA mitokondria. Hal ini berbeda dengan DNA pada inti sel yang memiliki banyak sekuens DNA yang tidak diekspresikan sebagai gen (DNA non genomik).
- Penggunaan kodon yang relatif relaks. Biasanya terdapat 30 atau lebih tRNA untuk asam amino yang spesifik namun di mitokondria hanya ada 22 tRNA yang dibutuhkan dalam sintesis protein. Oleh sebab itu di mitokondria, pasangan kodon-antikodon tidak seperti di inti sel.
- DNA pada mitokondria memiliki variasi kode genetik. Di mitokondria terdapat kode genetik yang sedikit berbeda. Empat dari 64 kodon memiliki arti yang berbeda dibandingkan pada DNA di inti sel.
NADH dan FADH2 Sebagai Molekul Sumber Elektron Berenergi Tinggi
NADH dan FADH2 yang dihasilkan oleh glikolisis dan siklus Krebs merupakan molekul sumber elektron berenergi tinggi. Elektron berenergi tinggi kemudian akan ditransfer ke membran dalam mitokondria untuk dipanen energinya dan akhirnya menghasilkan ATP. NADH dan FADH2 yang kehilangan elektron berenergi tinggi akan berubah menjadi NADH+ dan FAD yang kemudian digunakan kembali di glikolisis dan siklus Krebs untuk kembali menjadi NADH dan FADH2.

Setelah elektron berenergi tinggi dipindahkan ke membran dalam mitokondria, maka energi pada elektron ini akan diambil dan dimanfaatkan untuk memompa ion hidrogen keluar dari matriks. Ion hidrogen ini kemudian akan dialirkan kembali ke dalam matriks sambil diubah menjadi ATP.

Rangkaian Proses Rantai Transpor Elektron
Rantai transpor elektron melepas begitu banyak energi. Energi ini didapat dari proses reaksi redoks dimana secara agregat terjadi perpindahan dari elektron dari molekul dengan affinitas elektron lemah yaitu NADH sampai ke oksigen yang merupakan molekul dengan affinitias elektron tinggi. Secara umum dalam proses ini setiap perpindahan elektron melepas energi bebas (ΔG°) sebesar -26,2 kkal/mol (110 kJ/mol).
Besarnya energi ini tidak dilepas langsung melalui satu proses saja. Apabila hal ini terjadi hanya dengan satu langkah, maka proses yang terjadi akan seperti ledakan dan semua energi yang dilepas akan berupa panas. Hal ini tentu tidak menguntungkan dan malah akan sangat berbahaya. Oleh sebab itu, reaksi pelepasan energi ini dilakukan dengan proses bertahap sehingga dinamakan rantai transpor elektron. Mari kita bahas secara lebih detil mengenai molekul penting yang terlibat dan tahapan-tahapan reaksi transpor elektron ini.
Molekul Karier Elektron dalam Rantai Pernapasan
Dalam proses rantai elektron, elektron dibawa oleh molekul yang dinamakan karier elektron. Salah satu kelompok karier elektron ini berupa molekul dengan sifat dapat menyerap cahaya dan berubah warnanya ketika mengalami reduksi atau oksidasi. Oleh karena sifatnya ini, maka molekul karier elektron tersebut diberi nama sitokrom.
Dari penelitian, ternyata molekul sitokrom ini memiliki banyak jenis. Setidaknya ada tiga kelompol sitokrom yaitu sitokrom a, b, dan c. Setiap sel dalam tubuh dapat memiliki lebih dari satu jenis sitokrom.
Adapun struktur dari sitokrom ini berupa protein yang berikatan dengan grup heme. Grup heme sendiri berupa cincin forfirin yang mengelilingi atom ion besi. Besi diikat dalam cincin forfirin ini oleh empat atom hidrogen membentuk empat sudut segi empat. Ion besi di grup heme ini dapat berubah dari bentuk ferri (Fe3+) ke bentuk ferro (Fe2+) saat menerima elektron. Ion inti besi inilah yang bertugas menerima, menyimpan, serta memberikan elektron berenergi tinggi.

Selain sitokrom, terdapat molekul lain dengan inti besi sulfat yang juga berfungsi sebagai karier elektron dalam rantai oksidasi pernapasan. Di bawah ini adalah contoh karier elektron dengan inti besi sulfat:

Molekul karier elektron lainnya adalah quinone. Quinone (nama lain ubiquinone atau koenzim-Q) adalah molekul non protein dan merupakan bentuk paling sederhana dari karier elektron. Molekul ini merupakan molekul hidrofobik kecil yang bisa bergerak bebas di tengah lapisan membrann dalam lipid bilayer dari mitokondria. Quinone dapat mengambil atau memberi satu atau dua elektron dan dapat disertai mengambil satu proton untuk setiap elektron yang dibawanya. Untuk proses bagaimana quinonen menerima elektron serta proton untuk membawa energi dapat disimak di gambar di bawah ini:

Rantai Transpor Elektron Melibatkan Tiga Kompleks Enzim yang Tertanam di Dalam Membran Dalam Mitokondria
Rantai transpor elektron melibatkan tiga kompleks besar dari enzim. Kompleks enzim ini tertanam di membran dalam mitokondria dan terlibat dalam perpindahan elektron dari NADH hingga akhirnya sampai ke oksigen.

Selain memindahkan elektron, ketiga kompleks enzim ini juga memiliki kemampuan memompa proton. Di membran dalam mitokondria, tiga kompleks enzim ini berorientasi secara asimetris dan memompa ion hidrogen dari matriks ke ruangan intermembran mitokondria. Berikut adalah keterangan mengenai ketiga kompleks enzim tersebut:
- Kompleks NADH hidrogenase (secara umum dikenal sebagai kompleks I atau NADH-CoQ reductase complex). Kompleks ini merupakan kompleks terbesar yang mengandung lebih dari 40 rantai polipeptida. Kompleks ini menerima elektron dari NADH dan memindahkannya ke ubiquinone melalui flavin dan setidaknya tujuh inti besi-sulfat. Ubiquinone kemudian mengirimkan elektron ini ke kompleks yang kedua dari rantai transpor elektron yaitu kompleks sitokrom b-c1. Kompleks I ini memiliki kompleks enzim analog yaitu succinate-CoQ reductase complex atau kompleks II. Kompleks II ini menerima elektron dari FADH2 bukan dari NADH. Persamaan dan perbedaan antara kompleks I dan II ini akan dijelaskan lebih terperinci di bawah.
- Kompleks sitokrom b-c1 (dikenal sebagai kompleks III atau CoQH2—cytochrome c reductase complex). Kompleks ini mengandung setidaknya 11 rantai polipeptida dan berfungsi sebagai sebuah dimer. Tiap monomer mengandung tiga heme yang terikat ke sitokrom dan protein besi-sulfat. Kompleks ini menerima elektron dari ubiquinonen dan menyerangkannya ke sitokrom c yang membawa elektron ke kompleks sitokrom oksidase.
- Kompleks sitokrom oksidase (kompleks IV atau cytochrome c oxidase complex), berfungsi juga sebagai dimer dengan setiap monomer memiliki 13 rantai polipeptida, termasuk dua sitokrom dan dua atom tembaga. Kompleks ini menerima elektron satu per satu dari sitokrom c dan kemudian menyerahkan elektron tersebut, empat elektron sekaligus ke atom oksigen.

Sitokrom, inti besi-sulfat, dan atom tembaga hanya dapat menerima satu elektron tiap waktu namun NADH mendonasikan dua elektron dan tiap oksigen menerima empat elektron sekaligus. Oleh sebab itu terdapat sistem yang menampung elektron pada rantai transpor elektron ini yang salah satu sistem tersebut adalah sitokrom oksidase.

Oksigen Sebagai Akseptor Elektron Terakhir dan Dihasilkannya Air dalam Rantai Pernapasan
Nah, pada metabolisme pernapasan aeraob tentu kita sudah tidak asing dengan persamaan reaksi sederhana di bawah:
| C6H12O6 + 6 O2 → 6 CO2 + 6 H2O + Energi (ATP) |
Dimanakah sebenarnya oksigen (O2) ini berperan? Baik pada glikolisis maupun siklus Krebs, kita belum melihat keterlibatan oksigen ini satu kali pun. Nah ternyata, oksigen ini berperan dalam proses terakhir rantai transpor elektron yaitu sebagai penerima atau akseptor terakhir dari elektron bebas. Proses ini seperti dijelaskan di atas terjadi di kompleks IV atau kompleks sitokrom oksidase. Di dalam kompleks IV ini, empat elektron bebas akan menyebabkan empat H+ atau proton dipompa keluar. Dalam proses ini elektron tersebut akan kehilangan energinya karena ditukar dengan energi potensial dari proton. Setelah itu, empat elektron ini akan direaksikan dengan molekul oksigen ditambah empat proton sehingga menghasilkan dua molekul air (H2O). Perhatikan persamaan di bawah:
| 4 H+ + O2 → 2 H2O |
Proses terakhir dari kerja kompleks sitokrom oksidase ini dapat dihambat oleh racun seperti sianida. Seperti kita ketahui sianida menghambat kompleks IV, menyebabkan oksigen tidak bisa menjadi akseptor elektron terakhir dan menyebabkan seluruh metabolisme aerob menjadi terhenti. Akibatnya, korban yang mengonsumsi racun sianida akan mati lemas karena tidak dapat menggunakan oksigen untuk memproduksi ATP yang cukup.
Nah, untuk molekul lainnya yaitu karbondioksida (CO2) justru dihasilkan dari reaksi tahapan sebelumnya yaitu dua dari proses dekarboksilasi oksidatif dan empat molekul CO2 dari siklus Krebs.
Succinate-CoQ Reductase Complex (Kompleks II), Analog dari NADH-CoQ Reductase Complex (Kompleks I)
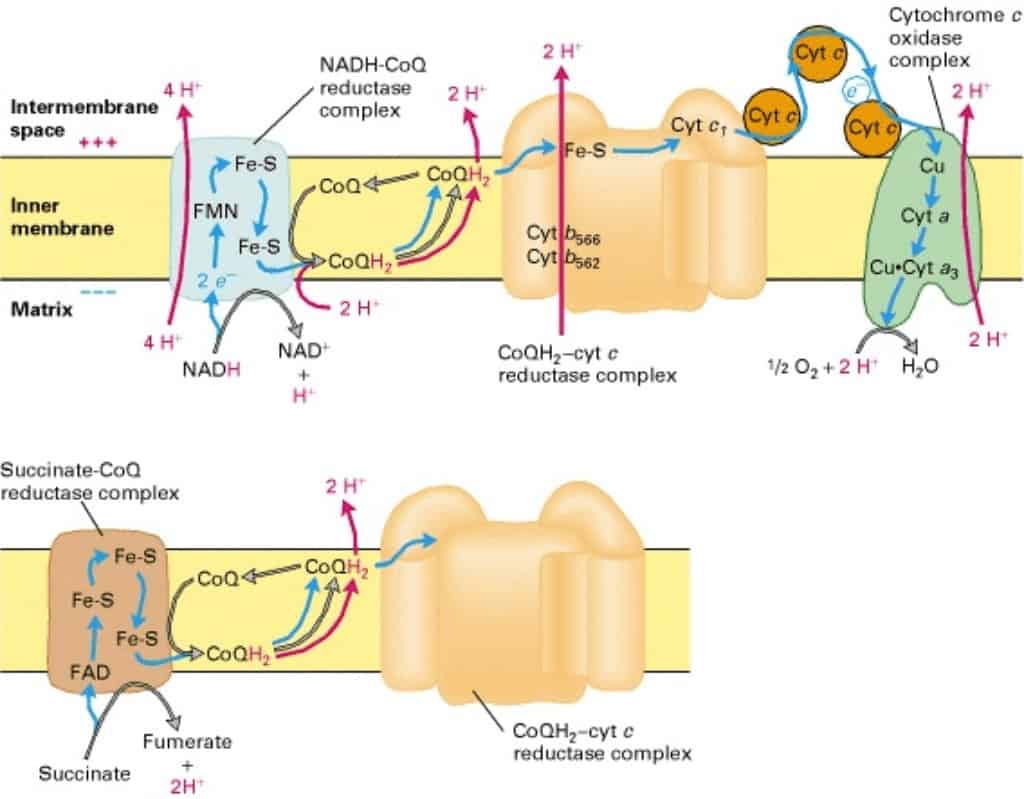
Pada siklus Krebs tahap 6 terjadi reaksi perubahan oksidasi suksinat menjadi fumarat dengan mengghasilkan FADH2. Sebenarnya enzim yang memperantarai reaksi ini merupakan komponen dari rantai transpor elektron. Enzim ini berupa kompleks II dari rantai transpor elektron atau succinate-CoQ reductase complex. Perhatikan bagan di bawah ini:
Sebenarnya kompkes enzim I dan II merupakan analog atau kemiripan dalam hal menerima elektron berenergi tinggi dari molekul pembawa energi. Perbedaan dari kompleks I adalah bahwa kompleks II menerima elektron berenergi tinggi dari FADH2 dan tidak memiliki aktivitas pompa proton. Oleh sebab itu, proses penerimaan elektron berenergi tinggi dari FADH2 menghasilkan lebih sedikit ATP dibandingkan dari NADH.
Perhatikan gambar di bawah. Pada bagan atas, memperlihatkan proses yang dimulai dari NADH yang diterima oleh kompleks enzim I kemudian berlanjut ke kompleks enzim III dan seterusnya. Adapun pada gambar di bawah, proses awal dimulai di kompleks II kemudian sama-sama dilanjutkan ke kompleks III dan seterusnya. Dikarenakan pada proses awal kompleks I memiliki pompa proton (4 H+ dipompa lebih banyak), maka NADH memberikan jumlah energi yang lebih besar dari pada FADH2.
Electron Tunneling pada Rantai Transpor Elektron
Salah satu fenomena mekanika atau fisika kuantum berupa electron tunneling pada sel dapat diobservasi pada rantai transpor elektron. Hal ini terjadi saat terjadi perpindahan elektron antara karier elektron dengan kompleks enzim.
Peristiwa perpindahan elektron ini terjadi secara kolisi atau tumbukan secara acak atau random. Pada perhitungan, dalam situasi ini terjadi tumbukan dan perpindahan elektron dalam setia 5-20 milidetik.
Hal unik dalam perpindahan elektron ini bahwa tidak hanya terjadi saat tumbukan namun dapat pula dengan aproksimasi atau kedekatan dua karier dengan celah sampai sejauh 2 nm. Bagaimana elektron dapat melompati celah ini? Jawabannya adalah dengan mekanisme quantum tunneling.
Uncoupler pada Rantai Transpor Elektron
Dalam kondisi tertentu, dapat terjadi proses rantai transpor elektron tanpa menghasilkan ATP. Peristiwa ini dinamakan uncoupling dan terjadi dengan adanya zat yang dinamakan uncoupler. Uncoupler ini dapat berupa zat sintetis seperti dinitofenol dan dapat pula berupa uncoupler alami.
Contoh peristiwa ini adalah pada jaringan lemak coklat. Jaringan ini berfungsi menjaga suhu dengan membakar lemak dan berperan penting dalam menjaga suhu terutama pada bayi tanpa perlu proses produksi panas dari menggigil.
Kita ketahui salah satu produksi panas tubuh adalah dari proses menggigil. Namun bayi belum mampu melakukan ini sehingga memerlukan proses lain. Proses produksi panas ini berlangsung di jaringan lemak coklat.
Dengan proses uncoupling, rantai transpor elektron dapat terjadi secara cepat tanpa memproduksi ATP dan gradien elektrokimia. Proses ini memungkinkan mitokondria membakar sebanyak mungkin lemak dan memproduksi panas bagi tubuh. Adapun uncoupler pada jaringan ini berupa protein yang dapat menghilangkan gradien elektrokimia.
Inhibisi Rantai Transpor Elektron
Salah satu mekanisme racun adalah menghambat rantai transpor elektron. Salah satunya adalah sianida yang menghambat kerja kompleks sitoktom okasidae dari rantai transpor elektron. Berikut adalah beberapa zat yang dapat menghambat rantai transpor elektron:

Kemiosmosis
Akibat adanya rantai transpor elektron, tercipta perbedaan konsenterasi ion hidrogen antara matriks dengan ruangan intermembran mitokondria. Perbedaan konsensterasi ini menciptakan gradien elektrokimia proton yang terdiri dua komponen. Yang pertama adalah gradien atau perbedaan energi potensial listrik membran (ΔV) dan yang kedua adalah gradien pH (ΔpH). Kedua jenis gradien ini, terutama ΔV menyumbangkan gaya utama yang nanti akan digunakan oleh mitokondria dalam memproduksi ATP pada proses kemiosmosis.

Gradien Elektrokimia Proton Mendorong Sintesis ATP
Perbedaan gradien elektrokimia yang disebutkan di atas akan menjadi sumber energi sintesis ATP. Konversi energi elektrokimia menjadi ATP ini dilakukan oleh enzim di membran dalam mitokondria yang bernama ATP sintase. Pada dasarnya enzim ini membentuk terowongan atau kanal ion hidrogen di membran dalam mitokondria. Akibat gradien elektrokimia tadi, maka ion hidrogen akan melintas kanal melewati ATP-sintase. Ketika melintas maka energi kinetik dari ion hidrogen akan dipakai untuk menggabungkan ADP dengan Pi membentuk ATP.

Struktur Kompleks Enzim ATP-Sintase
Di bawah adalah gambar struktur dari enzim ATP-sintase atau disebut juga F0F1 ATP-sintase. Enzim ini berupa kompleks multiunit protein dengan berat 500.000 dalton dan bekerja dengan mekanisme katalis rotorik. Bagian besar yang menyerupai lolipop terdiri dari enam subunit dan menonjol ke matriks mitokondria.

Terdapat bagian yang berelongasi ke kepala lolipop dengan memegang kepala lolipop dan menyambungkannya ke protein transmembran membentuk stator di dalam membran. “Stator” di membran ini berkontak dengan “rotor” di dalam membran. Bagian rotor ini terbentuk dari 10-14 subunit protein transmembran yang identik.
Saat proton melewati saluran atau kanal sempit di tempat kontak antara rotor dan stator, pergerakan ini akan menyebabkan cincin rotor berputar. Perputaran ini juga menyebabkan tangkai yang terhubung ke rotor juga berputar sehingga kepala lolipop juga akan berputar. Akibatnya, terjadi perubahan gradien elektrokimia menjadi energi mekanik di enzim.
Tiga dari enam subunit di bagian kepala lolipop mengandung situs ikat terhadap ADP dan fosfat inorganik. Subunit ini bergerak untuk membentuk ATP dengan memanfaatkan energi kinetik menjadi energi kimia dengan serangkaian perubahan bentuk konformasi saat terjadi pergerakan bagian lolipop dari ATP-sintase. Dengan cara ini, ATP-sintase dapat memproduksi 100 ATP tiap detik dengan produksi 3 molekul ATP tiap satu putaran rotor ATP-sintase. Diperkirakan dibutuhkan 3 – 5 ion hidrogen untuk menghasilkan satu ATP.
ATP Sintase dapat Berdungsi Terbalik Memompa H+ dengan Energi dari Hidrolisis ATP
ATP sintase bersifat bolak balik. Artinya selain memproduksi ATP dari pergerakan H+, enzim dapat berfungsi sebaliknya memompa H+ dengan memanfaatkan energi dari hidrolisis ATP menjadi ADP. Istilah dari sifat yang bolak balik ini dinamakan reversible coupling device.

Selain di manusia, ATP-sintase juga dimiliki banyak makhluk hidup lain seperti bakteri. Pada bakeri sifat enzim sebagai reversible coupling device dimanfaatkan dalam transisi antara metabolisme aerob ke anaerob.
Hasil ATP dari Rantai Transpor Elektron
Seperti dijelaskan di atas, bahwa produksi ATP tergantung dari banyaknya ion hidrogen yang dialirkan. Dari rantai transpor elektron, NADH akan mengeluarkan total 10 ion hidrogen sedangkan FADH2 menghasilkan 6 ion hidrogen. Apabila kita melakukan perhitungan total dari glikolisis, berikut rangkumannya untuk setiap satu molekul glukosa:
| Reaksi | Hasil NADH dan FADH2 | Jumlah proton yang dipompakan |
| Glikolisis | 2 NADH | 20 |
| Siklus Krebs | 8 NADH | 80 |
| 2 FADH2 | 12 | |
| Total | 112 |
Dari sekitar 112 proton, maka kurang lebih akan menghasilkan 22 – 37 ATP (3-5 proton per ATP). Oleh sebab itu, total ATP dari satu glukosa bisa menghasilkan 26 – 41 ATP (tambahan 2 ATP dari glikolisisi dan 2 GTP dari siklus Krebs). Oleh sebab itu jika mengatakan satu glukosa menghasilkan 36 atau 38 molekul ATP keduanya adalah benar.
Namun, apabila kita ambil nilai rerata, satu molekul NADH menghasilkan tiga ATP sedangkan satu FADH2 akan menghasilkan dua molekul ATP. Sedangkan untuk jumlah total ATP di semua proses metabolisme aerob secara sederhana dan ringkas dapat disimak di tabel di bawah ini:
| Jalur | Enzim yang terlibat | Reaksi produksi ATP | Jumlah produksi ATP |
| Glikolisis | Glyceraldehyde-3-phosphate dehydrogenase | Oksidasi rantai pernapasan 2 NADH | 6 |
| Phosphoglycerate kinase | Fosforilasi substrat | 2 | |
| Pyruvate kinase | Fosforilasi substrat | 2 | |
| Hexokinase dan phosphofructokinase | Reaksi konsumsi ATP | -2 | |
| Jumlah ATP glikolisis | 8 | ||
| Siklus Kreb | Pyruvate dehydrogenase | Oksidasi rantai pernapasan 2 NADH | 6 |
| Isocitrate dehydrogenase | Oksidasi rantai pernapasan 2 NADH | 6 | |
| α-Ketoglutarate dehydrogenase | Oksidasi rantai pernapasan 2 NADH | 6 | |
| Succinate thiokinase | Fosforilasi substrat | 2 | |
| Succinate dehydrogenase | Oksidasi rantai pernapasan 2 FADH2 | 4 | |
| Malate dehydrogenase | Oksidasi rantai pernapasan 2 NADH | 6 | |
| Jumlah ATP siklus Krebs | 30 |
Kesimpulan
Fosforilisasi oksidatif menyumbang sebagian besar energi berupa ATP dari metabolisme aerob. Proses ini terbagi dua yaitu rantai transpor elektron yang menghasilkan gradien elektrokimia yang kemudian dikonversi menjadi ATP oleh kemiosmosis oleh ATP sintase. Proses ini memiliki banyak kesamaan dengan fotosintesis dan bentuk mitokondria memegang peranan penting dalam proses fosforilisasi oksidatif ini.
Referensi
- Alberts B, Johnson A, Lewis J, Raff M, Roberts K, Walter P. Molecular biology of the cell. 5th ed. New York: Garland Science; 2008. 263–328 p.
- Frey TG, Mannella CA. The internal structure of mitochondria. Trends Biochem Sci. 2000 Jul;25(7):319–24.
- Guo R, Gu J, Zong S, Wu M, Yang M. Structure and mechanism of mitochondrial electron transport chain. Biomed J. 2018;41(1):9–20.
- Horvath SE, Daum G. Lipids of mitochondria. Prog Lipid Res. 2013;52(4):590–614.
- Lodish H, Berk A, Zipursky SL, et al. Molecular Cell Biology. 4th edition. New York: W. H. Freeman; 2000. Section 16.2, Electron Transport and Oxidative Phosphorylation.

Seorang dokter, saat ini sedang menjalani pendidikan dokter spesialis penyakit dalam FKUI. Peminat berbagai topik sejarah dan astronomi.


Comments 3
Terima kasih dok sudah buat website ini.. sangat bermanfaat dok
Pingback: Glikolisis: proses metabolisme glukosa makhluk hidup
terima kasih