Hadiah Nobel fisiologi/kedokteran 2019 diberikan kepada tiga ilmuwan yaitu William G. Kaelin Jr, Sir Peter J. Ratcliffe, dan Gregg L. Semenza. Ketiga ilmuwan tersebut dianugerahi hadiah Nobel atas penemuan mereka mengenai bagaimana sel melakukan respon terhadap hipoksia atau perubahan kadar oksigen di lingkungannya.

Daftar Isi
Perubahan Kadar Oksigen dalam Tubuh
Oksigen sangatlah penting karena merupakan sumber energi utama pada tubuh. Kadar oksigen dapat berubah-ubah terutama dengan perubahan ketinggian. Semakin tinggi, maka kadar oksigen akan menurun. Hal ini tentu memerlukan mekanisme adaptasi agar kerja tubuh tetap optimal.
Akan tetapi, kadar oksigen dalam tubuh lebih banyak berubah. Kadar oksigen antara sel otot di jantung dengan sel otot di kulit pada kaki akan berbeda. Begitu pula ketersediaan oksigen antara kondisi berbaring dengan kondisi aktivitas berat, walaupun pada tempat yang sama, namun akan berbeda. Bahkan, dalam keadaan luka misalnya, daerah sekitar luka akan mengalami kekurangan oksigen karena suplai darah terpotong oleh pembuluh darah yang pecah.
Jadi, tubuh kita sebenarnya malah lebih banyak berhadapan dengan perubahan kadar oksigen dibandingkan individu tubuh secara keseluruhan. Hal ini berarti pada tahap sel terdapat mekanisme tubuh dalam merasakan perubahan kadar oksigen agar bisa beradaptasi dengan perubahan kadar oksigen tersebut. Mekanisme seluler inilah yang diteliti oleh ketiga ilmuwan tersebut dan hasilnya memberi sumbangsih yang tidak sedikit bagi ilmu dasar maupun ilmu terapan termasuk kedokteran. Oleh sebab itu, atas dasar tersebut, ketiga ilmuwan ini kemudian dianggap pantas untuk mendapatkan hadiah Nobel fisiologi/kedokteran 2019.
Berawal dari Erythropoietin (Epo)
Walaupun telah lama diketahui bahwa tubuh dapat beradaptasi dengan kondisi hipoksia, namun baru awal tahun 1990-an kita baru mengetahui bagaimana proses ini berlangsung. Penemuan mekanisme respon terhadap hipoksia ini dimulai dari temuan terhadap hormon kunci yaitu erythropoietin atau Epo.
Epo adalah sebuah hormon yang diproduksi oleh ginjal sebagai respon terhadap kondisi hipoksia atau kekurangan oksigen. Meningkatnya kadar Epo akan mendorong produksi sel darah merah sehingga tubuh berupaya menambah pasokan oksigen dengan produksi sel darah merah yang lebih banyak. Walaupun diketahui efek tersebut, namun mekanisme apa dibalik ektivasi gen Epo tidak diketahui waktu itu namun penelitian yang berawal dari observasi terhadap gen Epo akan mulai menguak misteri dibalik mekanisme respon hipoksia ini.
Ditemukannya Hypoxic Responden Element (HRE)
Pada tahun 1990-an, penerima hadiah Nobel fisiologi/kedokteran 2019, Smenza dan Ratcliffe secara terpisah mempelajari bagaimana mekanisme dan regulasi dari gen Epo ini. Mereka menggunakan tikus yang diubah secara genetik yang dipaparkan terhadap berbagai macam kadar oksigen. Dari observasi ini mereka menemukan tempat di sekitar gen Epo yang dinamakan berfungsi meregulasi ekspresi Epo yang dinamakan hypoxic response element (HRE) (ilustrasi di bawah). HRE ini aktif di semua jaringan dan diketahui berespon atau aktif dalam kondisi hipoksia. Oleh sebab itu, disimpulkan bahwa HRE bersifat universal dan bisa menjadi mekanisme universal setiap jaringan dalam menghadapi kondisi hipoksia.
Ternyata bukan hanya gen Epo saja yang memiliki HRE. Gen-gen yang lain seperti gen yan gmengkodekan enzim glikolitik, vascular endothelial growth factor (VEGF) juga dipengaruhi ekspresinya oleh regio HRE di sekitar tersebut. VEGF adalah sinyal yang memberi perintah untuk pertumbuhan pembuluh darah. Keluarnya VEGF akan memicu pertumbuhan pembuluh darah untuk menambah oksigen di jaringan tersebut. Saat ini diketahui kurang lebih 300 gen yang diatur regulasinya oleh HRE.
Isolasi Hypoxia-Inducible Factor (HIF)
Kemudian, dengan mengetahui segmen HRE, maka Smenza akhirnya dapat mengisolasi faktor transkripsi yang kemudian disebut hypoxia-inducible factor (HIF). Smenza kemudian dapat mengidentifikasi gen HIF serta identifikasi dua tipe HIF yang kemudian dinamakan HIF-1α dan ARNT (aryl hydrocarbon receptor nuclear translocator) atau dikenal juga dengan nama HIF-1β. Cara kerja mekanisme HIF-1α dan ARNT terhadap HRE dapat disimak pada gambar di bawah ini:

Saat itu ditemukan bahwa dalam dalam keadaan normal konsenterasi HIF dalam sel rendah sedangkan dalam keadaan hipoksia, konsenterasi HIF tinggi. Kondisi ini dikarenakan pada keadaan normal, HIF akan mengalami proses ubiquitinisiasi, yaitu menempelnya gugus ubiquitin pada HIF. Setiap protein yang mengalamai ubiquinisasi kemudian akan didegradasi oleh proteasome. Penjelasan mengenai proteasome ini dapat dibaca pada artikel mengenai proteolisis.
Akan tetapi, bagaimana proses atau mekanisme ubiquitinisasi dari HIF dalam kondisi oksigen normal ini pada saat itu belum diketahui secara pasti.
Hubungan HIF dan Protein Von Hippel-Lindau (VHL)
Jawaban mengenai proses ubiquinisasi dari HIF datang dari proses yang tidak terduga. Di saat bersamaan ketika Smenza dan Ratcliffe mengeksplorasi regulasi gen Epo, penerima hadiah Nobel fisiologi/kedokteran 2019 yang ketiga William Kaelin, Jr. memberikan kontribusi yang penting. Kaelin tengah melakukan penelitian mengenai genetik kanker pada penyakit von Hippel-Lindau (penyakit VHL).
Penyakit VHL ini menyebabkan meningkatnya secara drastis kejadian kanker tertentu pada keluarga yang memiliki mutasi gen VHL. Kaelin menemukan bahwa gen VHL mengkodekan protein yang mencegah kanker. Selain itu, Kaelin juga menemukan bahwa pada sel dengan gen VHL yang mengalami mutasi mengeskpresikan gen yang meregulasi hipoksia secara tinggi. Ketika gen VHL normal diberikan, maka ekspresi gen hipoksia tersebut menjadi normal. Hal ini memberi petunjuk bahwa VHL dapat mengontrol respon terhadap hipoksia.
Petunjuk tambahan lain datang dari kelompok peneliti lainnya yang memperlihatkan bahwa VHL adalah bagian dari kompleks protein yang bertugas memberi label ubiquitin untuk menandai protein-protein yang akan didegradasi oleh proteasome. Penemuan ini semakin menunjukan bahwa degradasi HIF-1α pada keadaan oksigen normal terjadi akibat interaksi HIF-1α dengan VHL.
Pengaruh Kadar Oksigen Terhadap Hidroksilasi HIF-1α
Setelah didapatkan hubungan yang jelas antara HRE, HIF, dan VHL, maka pertanyaan selanjutnya adalah bagaimana mekanisme perubahan kadar oksigen dapat mempegaruhi HIF? Pada saat itu dicurigai bahwa HIF akan bereaksi dengan oksigen sehingga akan menyebabkan HIF dapat berinteraksi dengan VHL.
Ternyata kemudian ditemukan adanya reraksi hidroksilasi residu proline pada HIF oleh oksigen. Pada keadaan tanpa oksigen atau hipoksia, tidak ada proses hidroksilasi dari HIF-1α maupun EPAS1. Karena itu, VHL tidak bisa mengenali HIF-1α sehingga tidak terjadi ubiquinisasi dan konsenterasi HIF-1α menjadi tinggi. Hal ini kemudian menyebabkan HIF dapat bertranslokasi ke inti sel dan mengaktivasi HRE. Adapun proses ini dapat dilihat pada gambar di bawah ini:
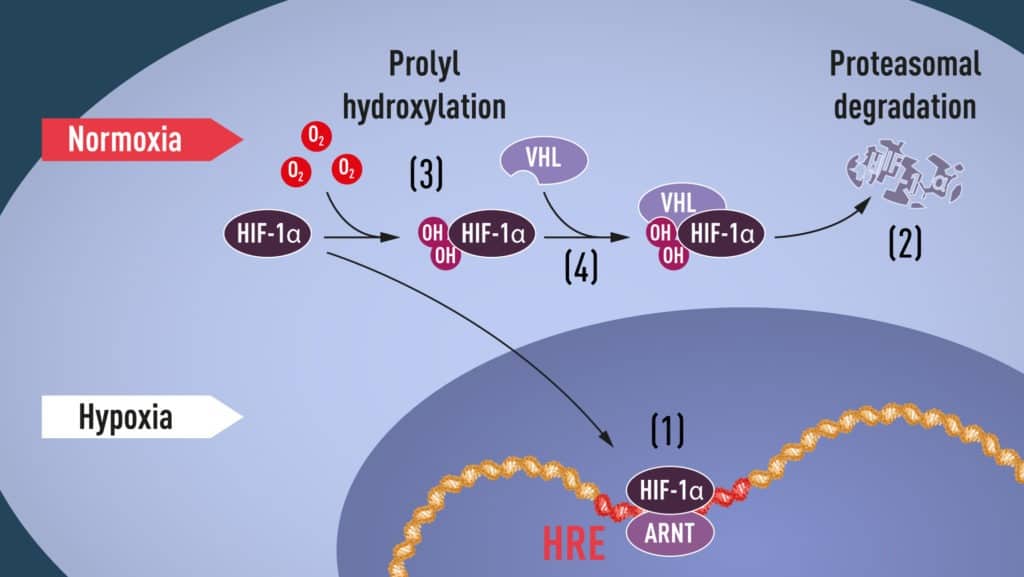
Jadi, dengan ditemukannya mekanisme bagaimana pengaruh oksigen terhadap proses hidroksilasi protein HIF, lengkap sudah gambaran proses molekuler sel mendeteksi dan berespon terhadap kondisi hipoksia.
Sekuens Proses Respon Sel Terhadap Hipoksia
1) Hidroksilasi HIF-1α oleh Oksigen
HIF-1α diproduksi secara konstan, tidak meningkat atau berkurang. Yang berpengaruh justru adalah kecepatan protein ini dipecah. Kecepatan HIF dipecah tergantung dari konsenterasi oksigen dalam sel.
Pada keadaan normal atau normoksia, oksigen akan bereaksi dengan HIF berupa hidroksilasi. Proses ini akan menambahkan gugus OH atau hidroksil pada protein HIF. Penambahan gugus hidroksil ini akan menimbulkan perubahan bentuk dari protein HIF.

2) Pengenalan HIF-1α oleh Protein VHL
Protein HIF yang berubah karena hidroksilasi kemudian akan dikenali oleh protein VHL. Protein ini kemudian akan menjalankan proses selanjutnya yaitu ubiquitinisasi atau penambahan gugus ubiquitin pada HIF. Penambahan ubiquitin ini membuat HIF dikenali oleh proteasome dan oleh proteasome HIF akan didegradasi. Proses ini berlangsung cepat sehingga dalam keadaan normoksia, kadar HIF dalam sel akan sangat kecil.
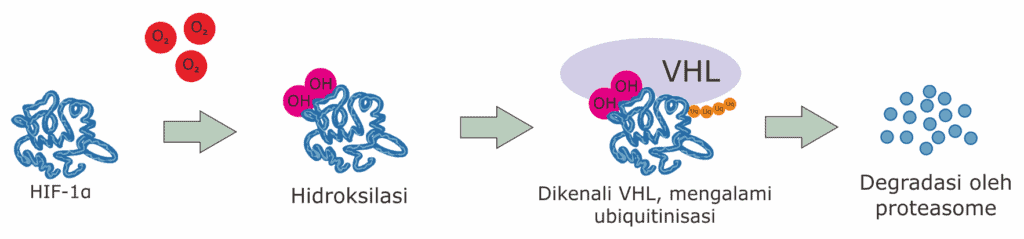
3) Peningkatan Kadar HIF-1α saat Hipoksia
Dalam kondisi hipoksia, tidak terjadi proses hidroksilasi dari HIF-1α. Akibatnya, molekul HIF-1α tidak lagi dikenali oleh protein VHL dan tidak didegradasi. Selanjutnya, jumlah atau konsentrasi HIF-1α akan meningkat sehingga HIF-1α bisa masuk ke inti sel dan kemudian berikatan dengan ARNT di HRE. Ikatan ini kemudian akan mengaktivasi gen yang berespon terhadap hipoksia seperti VGEF dan Epo. Di bawah ini adalah perbedaan keadaan antara normoksia dengan hipoksia:

Signifikansi Jalur Kontrol HIF
Alasan atau pertimbangan pemberian Nobel fisiologi/kedokteran 2019 terhadap penelitian dalam respon hipoksia ini tentu saja dikarena oksigen adalah kebutuhan vital atau penting untuk kehidupan. Tanpa oksigen, manusia tidak dapat hidup. Walaupun demikian, penemuan mekanisme adaptasi terhadap kondisi hipoksia baru diketahui tahun 1990-an. Padahal pengetahuan mengenai pentingnya oksigen sudah diketahui sejak sangat lama. Dengan ditemukannya mekanisme HIF ini, maka proses dasar respon tubuh terhadap perubahan kondisi oksigen dapat diketahui.
Pengetahuan ini penting karena mekanisme ini menjelaskan proses tubuh bertahan terhadap kerusakan akibat hipoksia. Di sisi lain, terutama untuk sel kanker, mekanisme ini digunakan untuk bertahan terhadap kondisi hipoksia relatif akibat tingginya pertumbuhan dan metabolisme dari sel tumor. Kita ketahui bahwa sel tumor aktif membelah dan membutuhkan oksigen tinggi untuk bertahan hidup. Namun, terbatasnya suplai pembuluh darah dan cepatnya pertumbuhan tumor membuat kondisi lingkungan sel tumor berada dalam keadaan hipoksia.
Kemampuan sel tumor untuk mengekspresikan HIF tentu menjadi penting karena memungkinkan sel tumor untuk bertahan dalam keadaan hipoksia. Ekspresi HIF yang tinggi juga dikaitkan dengan kemampuan sel tumor dalam resisten terhadap pengobatan seperti radioterapi. Pada beberapa jenis kanker seperti kanker buli, otak, payudara, kolon, esofagus, kepala/leher, hepatoma, pankreas, kulit, gaster, dan uters, keberadaan HIF menjadi faktor prognostik atau luaran yang buruk. Di tengah pentingnya posisi HIF pada kehidupan sel tumor atau kanker menjadi menarik apabila HIF menjadi salah satu target dalam pengobatan penyakit kanker.
HIF dan Respon Imunitas Terhadap Sel Kanker
Imunoterapi menjadi salah satu modalitas terapi yang baru dalam pengobatan kanker. Pentingnya imunoterapi ini dibuktikan dengan raihan hadiah Nobel tahun 2018 yang jatuh ke peneliti yang menjadi pionir dalam bidang imunoterapi (James P. Allison (inhibitor CTLA-4) dan Tasuko Hanjo (inhibitor PD-1) ). Ternyata kita ketahui sekarang bahwa pada keadaan hipoksia, sel tumor akan meningkatkan ekspresi dari PD-1 dan membentuk kondisi lingkungan yang imunosupresif. Hubungan proses hipoksia terhadap kondisi mikro dari tumor yang imunosupresif ini dapat dilihat di gambar di bawah ini:

Potensi dan Hambatan Terapi Anti Kanker dengan Target HIF-1α
Dari gambaran di atas, semakin jelas bahwa HIF-1α memiliki banyak peran dalam sel kanker dan apabila kita dapat menghambatnya, dapat membantu dalam terapi penyembuhan sel kanker. Namun, terapi target terhadap HIF-1α tidak mudah untuk dikembangkan.
Masalah yang dihadapi adalah selektivitas inhibitor HIF-1α. Kita ketahui bahwa HIF-1α tidak hanya dibutuhkan sel kanker namun hampir semua sel dalam tubuh kita membutuhkan HIF-1α. Saat ini telah dilakukan uji klinis obat kanker baru dengan obat yang menargetkan HIF-1α. Penelitian-penelitian ini masih berjalan dan menunggu waktu untuk melihat hasil dari obat tersebut.
Kesimpulan
Oksigen merupakan zat yang sangat penting bagi kehidupan makhluk aerob. Terlalu banyak atau terlalu sedikit oksigen akan mematikan sehingga perlu ada mekanisme dalam mengontrol kadar oksigen dan berespon secara cepat. Pengetahuan mengenai mekanisme ini menjadi berkembang berkat hasil penelitian yang dipimpin Gregg L. Semenza, William G. Kaelin, dan Peter J. Ratcliffe. Hasil penelitian mereka membuka pemahaman yang lebih besar terutama dalam bidang penelitian lain yaitu angiogenesis. Oleh sebab itu, hadiah Nobel fisiologi/kedokteran 2019 dianugerahkan kepada ketiga ilmuwan ini berkat hasil penelitian mereka mengenai mekanisme respon sel terhadap hipoksia. Selain dalam artikel ini, penjelasan mengenai hadiah Nobel Fisiologi/Kedokteran Tahun 2019 ini juga dapat disimak di video di bawah ini:
Sumber
- Jaakkola P, Mole DR, Tian YM, Wilson MI, Gielbert J, Gaskell SJ, et al. Targeting of HIF-α to the von Hippel-Lindau ubiquitylation complex by O 2 -regulated prolyl hydroxylation. Science (80- ). 2001;292(5516):468–72.
- Johnson RS. Profile of William Kaelin, Peter Ratcliffe, and Greg Semenza, 2016 Albert Lasker basic medical research awardees fire in the air, fire in the cell. Proc Natl Acad Sci U S A. 2016;113(49):13938–40.
- Maxwell PH, Wiesener MS, Chang G-W, Clifford SC, Vaux EC, Cockman ME, et al. The tumour suppressor protein VHL targets hypoxia-inducible factors for oxygen-dependent proteolysis. Nature. 1999 May;399(6733):271–5.
- Mennerich D, Kubaichuk K, Kietzmann T. DUBs, Hypoxia, and Cancer. Trends in Cancer. 2019 Oct;5(10):632–53.
- Ratcliffe PJ, O’Rourke JF, Maxwell PH, Pugh CW. Oxygen sensing, hypoxia-inducible factor-1 and the regulation of mammalian gene expression. J Exp Biol. 1998;201(8):1153–62.
- Semenza GL, Nejfelt MK, Chi SM, Antonarakis SE. Hypoxia-inducible nuclear factors bind to an enhancer element located 3′ to the human erythropoietin gene. Proc Natl Acad Sci U S A. 1991;88(13):5680–4.
- Wang GL, Jiang BH, Rue EA, Semenza GL. Hypoxia-inducible factor 1 is a basic-helix-loop-helix-PAS heterodimer regulated by cellular O 2 tension. Proc Natl Acad Sci U S A. 1995;92(12):5510–4.

Seorang dokter, saat ini sedang menjalani pendidikan dokter spesialis penyakit dalam FKUI. Peminat berbagai topik sejarah dan astronomi.

