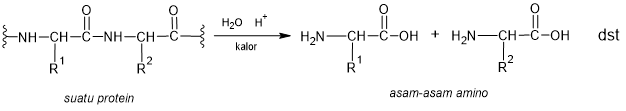
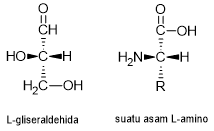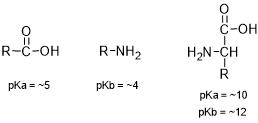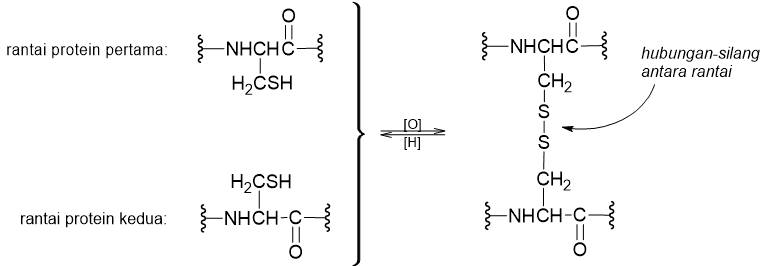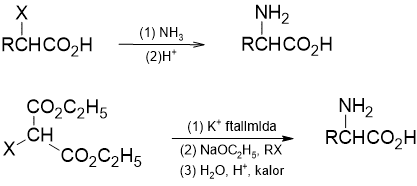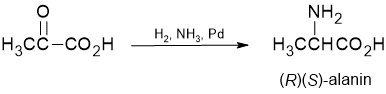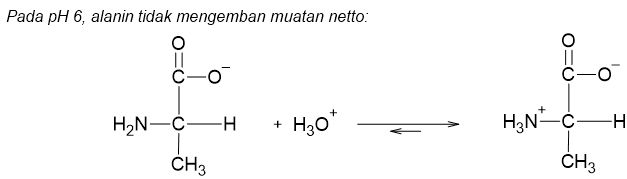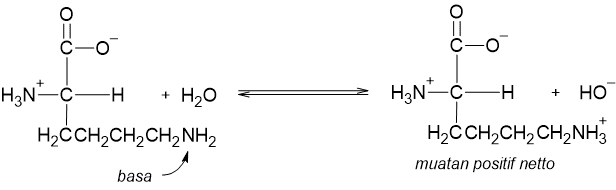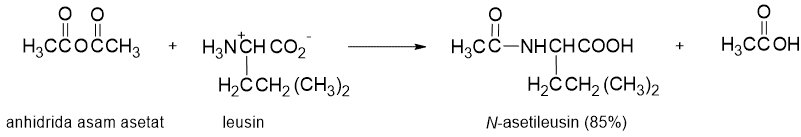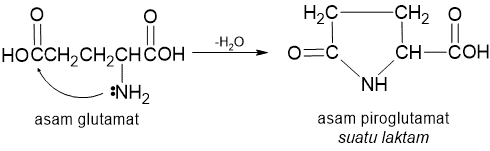Protein meruoakan kelompok senyawa yang terpenting pada makhluk hidup. Adapun istilah protein berasal dari bahas Yunani proteios, yang berarti “pertama”. Protein sendiri merupakan senyawa poliamida dimana hidrolisi dari protein akan menghasilkan pecahan berupa asam amino.
Hanya dua puluh asam amino yang lazim dijumpai dalam protein tumbuhan dan hewan, namun kedua puluh asam amino ini dapat digabungkan menurut berbagai cara membentuk otot, kulit, bulu, sutera, hemoglobin, enzim, antibodi, dan banyak hormon. Dalam kesempatan kali ini kita akan mulai membahas dari asam amino kemudian berlanjut dengan bagaimana kombinasi asam-asam amino ini menghasilkan produk senyawa yang sangat beragam.
Daftar Isi
Struktur Asam Amino
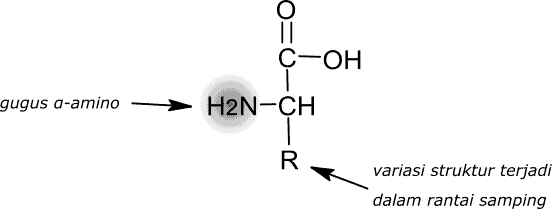
Asam amino merupakan termasuk kelompok asam α-aminokarboksilat. variasi dalam struktur monomer ini terjadi dalam keberagaman rantai atau gugus samping.
Asam amino yang paling sederhana adalah asam aminoasetat () yang disebut glisin. Glisin tidak memiliki rantai samoing dan karena itu tidak mengandung satu karbon kiral. Adapun asam amino lainnya memiliki rantai samping sehingga karbon-α-nya bersifat kiral. Asam amino yang berasal dari protein termasuk dalam deret L yang artinya gugus-gugus di sekeliling karbon α memiliki konfigurasi yang sama seperti dalam L-gliseraldehida. Adapun asam amino yang berasal dari proses non organik seperti dalam meteorit merupakan asam α-amino resemik (memiliki campuran asam amino dengan struktur deret L dan R).
Asam amino tidak selalu bersifat seperti senyawa-senyawa organik. Misalnya, titik lelehnya di atas 200°C, sedangkan kebanyakan senyawa organik dengan bobot molekul sekitar berupa cairan pada temperatur kamar. Asam amino larut dalam air dan pelarut polar lain, tetapi tidak larut dalam pelarut nonpolar seprti dietil eter dan benzena. Asam amino mempunyai momen dipol yang besar. Juga, mereka kurang bersifat asam dibandingkan sebagian besar asam karboksilat dan kurang basa dibandingkan sebagian besar amina.
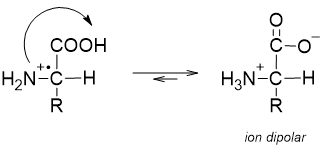
Mengapa asam amino menunjukan sifat-sifat yang tidak biasa ini? Hal ini dikarenakan asam amino mengandung gugus amino yang bersifat basa dan gugus hidroksil yang bersifat asam dalam satu molekul yang sama. Karena itu, asam amino mengalami reaksi asam-basa internal yang menghasilkan ion dipolar yang disebut zwitterion (dari bahasa Jerman zwitter yang berarti “hibrida”). Selain itu, karena bermuatan ion maka asam amino mempunyai banyak sifat garam. Tambahan pula, pKa suatu asam amino bukanlah pKa dari gugus , melainkan dari gugus . pKb juga juga bukan berasal dari gugus amino melainkan berasal dari gugus yang bersifat basa sangat lemah.
| Nama | Singkatan | Struktur |
|---|---|---|
| Alanin | ala (A) | |
| Arginin* | arg (R) | |
| Asparagin* | asn (N) | 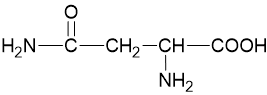 |
| Asam aspartat | asp (D) | 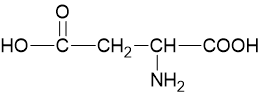 |
| Sistein (cysteine) | cys (C) | |
| Asam glutamat | glu (E) | 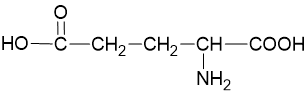 |
| Glutamin | gln (Q) | 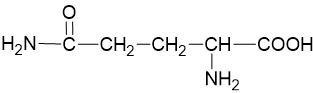 |
| Glisin | gly (G) | |
| Histidin* | his (H) | 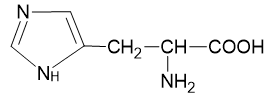 |
| Isoleusin* | ile (I) | 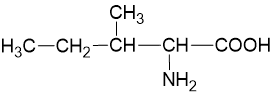 |
| Leusin* | leu (L) | 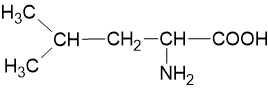 |
| Lisin* | lys (K) | |
| Metionin* | met (M) | |
| Fenilalanin | phe (F) | 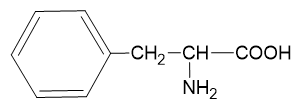 |
| Prolin | pro (P) | 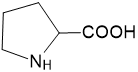 |
| Serin | ser (S) | |
| Treonin* | thr (T) | 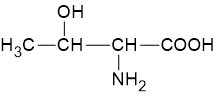 |
| Triptofan* | try (W) | 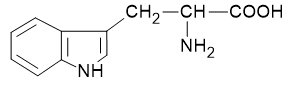 |
| Tirosin | tyr (Y) | 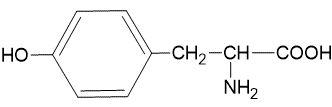 |
| Valin* | val (V) | 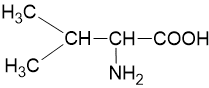 |
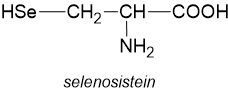
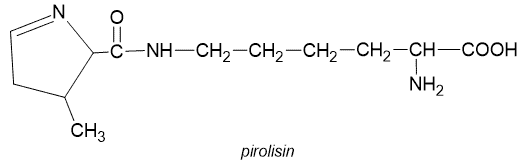
Tabel di atas menunjukan 20 asam amino standar yang terdapat pada protein. Meski asam amino biasanya berada dalam bentuk ion bipolar, struktur dalam literatur umumnya memakai bentuk non ioniknya. Walaupun demikian, saat ini diketahui juga ada 2 asam amino tambahan yaitu selenosistein (Sec atau U) dan pirolisin (Pyl atau O) dipertimbangkan masuk ke dalam daftar 22 asam amino yang ada dalam protein manusia. Alasan kenapa kedua asam amino ini tidak dimasukan ke dalam daftar asam amino standar yang berada di makhluk hidup karena keduanya tidak diinkorporasikan ke dalam protein melalui mekanisme standar kode genetik atau dalam kata lain tidak dikodekan dalam kode genetik DNA. Keduanya ada dalam struktur protein namun dimasukan ke dalam struktur melalui proses rekoding dari kodon stop (UGA untuk Sec, UAG untuk pyl) melalui mekanisme tRNA yang sangat khusus.
A. Asam Amino Esensial
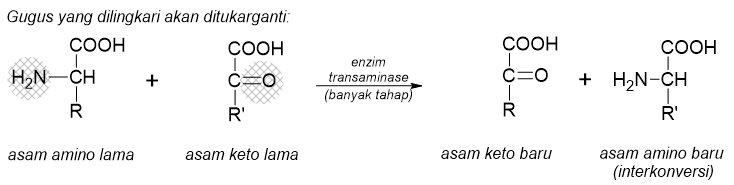
Beberapa asam amino dapat disintesis atau diproduksi oleh suatu organisme dari “persediaan” senyawa organiknya. Cara sintesis semacam ini adalah dengan mengubah satu asam amino yang berlebih ke asam amino lainnya yang diinginkan melalui reaksi transaminasi.
Tidak semua asam amino dapat diperoleh dengan mekanisme interkonversi dari asam amino lainnya atau dengan sintesis dari senyawa lain pada binatang. Asam amino seperti ini tidak disintesis sendiri dan didapat melalui asupan dari makanan. Asam amino yang seperti ini dinamakan asam amino esensial. Asam amino pada satu spesies mungkin akan berbeda dengan spesies lainnya dan bahkan ada perbedaan dari satu individu ke individu lainnya.
Pada tabel di atas, asam amino yang dianggap esensial bagi mansia ditandai dengan tanda bintang. Dari asam amino tersebut, triptofan, fenilalanin, metionin, dan histidin dapat diubah secara enzimatik dari (R) ke (S) sehingga suatu campuran rasemik asam-asam amino ini dapat dimanfaatkan seluruhnya. Adapun asam amino lain harus disediakan dalam makanan dalam konfigurasi (S) agar dapat dimanfaatkan dalam sintesis protein.
Suatu contoh perbedaan asam amino esensial antarindividu adalah tirosin. Asam amino ini tidak dianggap esensial karena karena pada kebanyakan orang, tirosin dapat disintesis dari fenilalannin. Namun pada orang yang memiliki penyakit genetik fenilketonuria (PKU), orang tersebut tidak memiliki tidak memiliki enzim fenilalanin hidroksilasi yang diperlukan dalam proses perubahan tersebut. Fenilalanin malah diubah menjadi fenilpiruvat. Oleh sebab itu, pada penderita PKU, tirosin menjadi asam amino esensial dan konsumsi fenilalanin harus dibatasi. Jika tidak, penumpukan fenilpiruvat di otak dapat menyebabkan keterbelakangan mental.
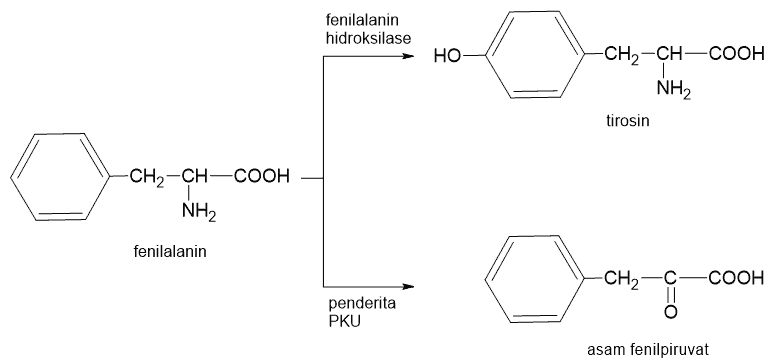
Kondisi tersebut dikenal dengan istilah asam amino esensial bersyarat (conditional essential) dimana dalam keadaan normal asam amino ini bukan merupakan asam amino esensial namun dalam kondisi tertentu misalnya dalam keadaan sakit, asam amino ini menjadi esensial. Contoh dari asam amino esensial bersyarat ini adalah arginin, sistein, glutamin, tirosin, glisin, prolin, dan serin.
B. Pentingnya Struktur Rantai Samping Asam Amino
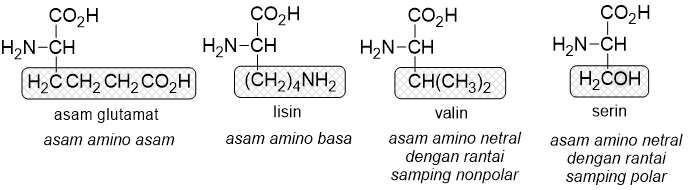
Dikarenakan adanya perbedaan sifat struktur asam amino, maka polimer yang tersusun dari ke-20 asam amino ini dapat memiliki sifat yang sangat beragam. Perhatikan pada tabel ke-20 asam amino di atas. Sebagian asam amino memiliki gugus samping yang memiliki gugus karboksil yang memiliki sifat asam sehingga dikelompokan ke dalam kelompok asam amino asam. Adapun asam amino yang memiki rantai samping gugus amino dikelompokan ke dalam kelompok asam amino basa. Rantai samping asam dan basa ini bisa mempengaruhi struktur dan reaktivitas protein yang disusun oleh asam amino tersebut. Adapun asam amino yang lain selain asam atau basa dikelompokan ke dalam kelompok asam amino netral. Gugus samping yang netral juga penting. Misalnya, asam amino dengan gugus samping yang mengandung atau gugus polar lainnya yang dapat membentuk ikatan hidrogen akan berperan penting dalam menentukan struktur suatu protein.
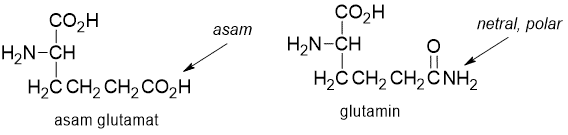
Karakteristik suatu protein akan berubah jika suatu gugus asam karboksilat dalam suatu rantai diubah menjadi amida. Perhatikan perbedaan dalam rantai samping glutamin dan asam glutamat di bawah.
Rantai samping tiol dalam sitein memainkan peranan yang unik dalam struktur protein. Tiol dapat bereaksi kopling oksidatif untuk menghasilkan disulfida. Kopling antara dua satuan sistein ini menghasilkan asam amino baru yang disebut sistin dan memberikan cara hubungan silang rantai-rantai protein. Pengeriting rambut melibatkan pemutusan beberapa hubungan silang lama dengan cara reduksi dan kemudian membentuk hubungan yang baru di posisi lain dari rantai protein.
Urutan asam amino dalam suatu rantai molekul protein menentukan hubungan rantai samping satu sama lain sehingga menentukan bagaimana protein itu berinteraksi dengan dirinya sendiri maupun lingkungannya. Sebagai contoh, suatu hormon atau protein lain yang larut dalam air mengandung banyak asam amono dengan rantai samping polar sedangkan protein otot yang yang tidak larut dalam air mengandung lebih banyak asam amino dengan gugus samping non polar.
Suatu kasus mengenai pentingnya gugus samping asam amino yakni pada penyakit anemia sel sabit (sickle-cell anemia). Hemoglobin memiliki rantai protein yang tediri dari dari 146 satuan asam amino. Yang menjadi pembeda pada hemoglobin normal dengan hemoglobin sel sabit adalah perbedaan satu asam amino dari asam glutamat (sam amino asam) menjadi valin (asam amino non polar). Mutasi ini menjadikan hemoglobin sel sabit kurang larut dan kurang mampu menjalankan tugas mengangkut oksigen ke sel-sel tubuh sebagaimana mestinya.
Sintesis Asam Amino
Asam amino biasa merupakan senyawa yang agak sederhana dan sintesis campuran rasemik dari asam amino dapat dibuat melalui teknik-teknik standar. Campuran rasemik kemudian dapat dipisahkan untuk menghasilkan asam amino enantiomer murni.
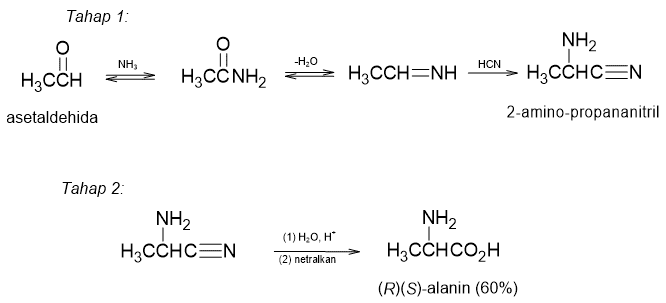
Sintesis Strecker dari aasam amino dikembangkan tahun 1850 yang terdiri dari dua tahap reaksi. Tahap pertama adalah reaksi antara suatu aldehida dengan campuran amonia dan HCN untuk menghasilkan aminonitril. Hidrolisis aminonitril ini kemudian akan menghasilkan asam amino.
Sintesis ftalimida Gabriel merupakan jalur sintesis yang lebih baik. Keuntungan sintesis ini terhadap aminasi langsung adalah tidak terjadinya alkilasi yang berlebihan.
Aminasi reduktif suatu asam α-keto juga merupakan prosedur lain untuk memperoleh asam amino rasemat (ingat, gugus karboksil tidak mudah direduksi).
Reaksi Asam Amino
A. Keamfoteran Asam Amino
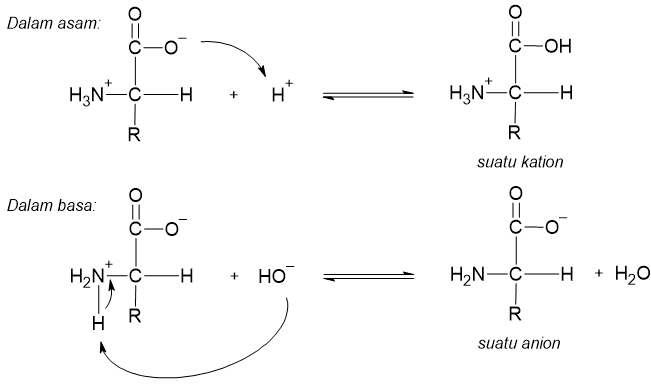
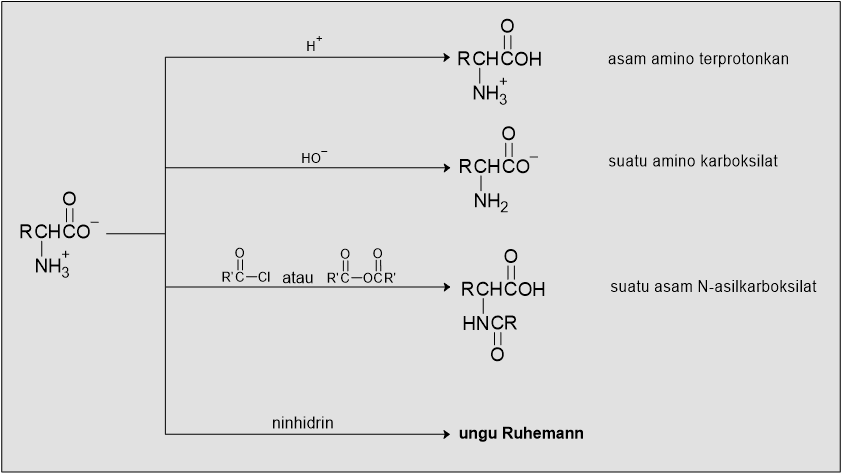
Molekul asam amino mengandung baik ion karboksilat () maupun ion amonium () dalam satu molekul. Oleh karena itu asam amino disebut bersifat amfoter. Dengan sifat amfoter ini asam amino dapat bereaksi dengan asam ataupun basa dan masing-masing menghasilkan suatu kation atau anion.
Titik isoelektrik. Walaupun bersifat amfoter, larutan dari asam amino tidak bersifat benar-benar. Larutan asam amino sebenarnya berifat agak asam (karena itu namanya asam amino). Keasaman ini disebabkan karena keasaman gugus lebih kuat dari pada kebasaan . Perbedaan ini menyebabkan larutan asam amino alanin mengandung lebih banyak anion asam amini dari pada bentuk kationnya. Dengan demikian kita dapat katakan bahwa larutan asam amino alanin mengemban muatan negatif netto.
Jika kita tambahkan HCl atau asam lain sedikit demi sedikit ke dalam larutan alanin, maka kesetimbangan asam-basa akan bergeser ke satu titik dimana muatan netto pada larutan asam amino menjadi nol. Pada pH dimana suatu larutan asam amino tidak mengemban muatan ion netto didefinisikan sebagai titik isoelektrik dari asam amino tersebut. titik isoelektrik dari larutan alanin adalah pH 6,0.
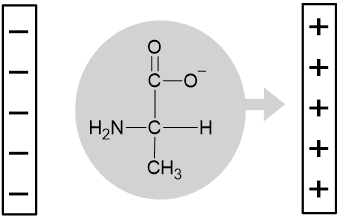
Titik isoelektrik juga dapat ditentukan dengan elektroforesis, suatu proses yang mengukur migrasi ion dalam suatu medan listrik. Dalam proses elektroforesis, larutan suatu asam amino ditaruh pada media adsorben diantara sepasang elektroda. Dalam kondisi ini, anion akan bermigrasi ke arah elektrod apositif dan kation ke arah elektroda nehatif. Jika alanin atau asam amino netral lainnya dilarutkan dalam air biasa, ternyata terdapat migrasi netto ion asam amino ke arah elektroda positif. Pada titik isoelektriknya, suatu asam amino tidak menunjukan migrasi netto ke arah elektroda manapun dalam suatu elektroforesis.
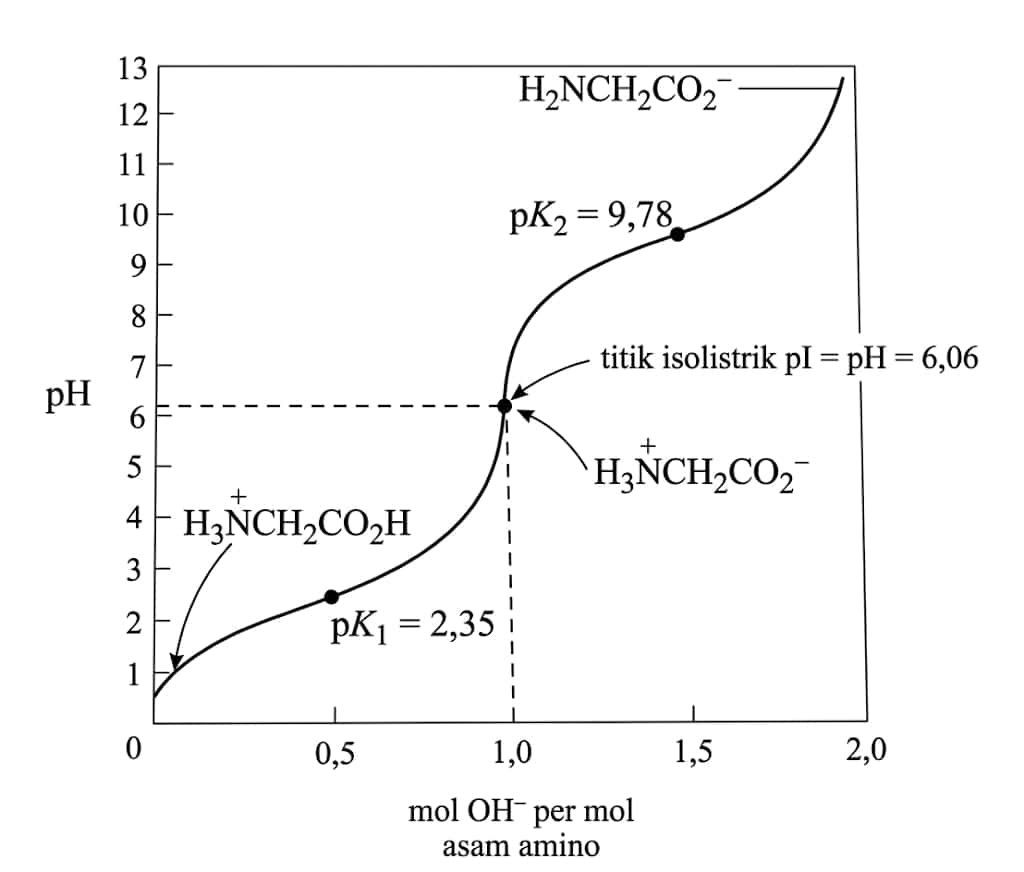
Titi isoelektrik dapat juga diteteapkan dengan titrasi. Gambar di bawah menunjukan kurva titrasi untuk titrasi kation dari glisin, , dengan basa. Pada saat basa ditambahkan, ion yang terprotonkan sempurna diubah menjadi ion dipolar yang netral, . Bila separuh bentuk kation telah dinetralkan, pH akan sama dengan pK1 untuk reaksi tersebut.
Bila , , dengan demikian
Ketika lebih banyak basa ditambahkan, semua bentuk kation diubah menjadi ion dipolar yang netral. pH pada saat terjadinya hal ini disebut titik isoelektrik. Dengan penambahan basa yang lebih banyak lagi, ion dipolar diubah menjadi anion. Pada titik tengah, akan sama dengan .
Bila , dengan demikian
Titik isoelektrik bisa ditunjukan pada kurva titrasi namun juga bisa dihitung sebagai rata-rata pK1 dan pK2.
Titik isoelektrik dari suatu larutan asam amino adalah suatu ketetapan fisis, Nilainya bermacam-macam tetapi berada dalam salah satu dari tiga kisaran umum. Untuk suatu asam amino netral, dimana titik isoelektriknya tergantung dari nilai pKa dan pKb dari gugus dan , maka nilai pI berkisar antara 5,5 – 6,0.
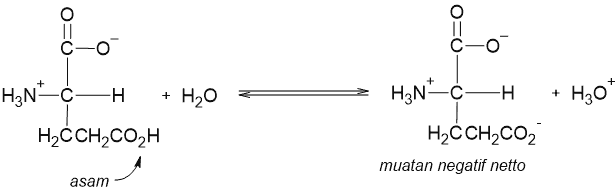
Dengan adanya gugus karboksi kedua pada rantai samping asam amino asam berarti terdapat gugus lain yang dapat berinteraksi dengan air. Berarti, larutan asam amino asam jelas bersifat asam dan ion asam aminonya mengemban muatan negatif netto.
Diperlukan konsentrasi lebih tinggi untuk memungkinkan asam amino asam sampai ke tiotik isoelektriknya daripada yang diperlukan asam amino netral. Titik isoelektrik asam amino asam berkisar pH=3.
Suatu asam amino basa mempunyai gugus amino kedua yang berinteraksi dengan air membentuk ion positif. Diperlukan ion=ion hidroksida untuk menetralkan asam amino basa dan membawanya sampai ke titik isoelektrik. Untuk asam amino basa, titik isoelektriknya terletak di atas pH=7. Titik isoelektrik ini berkisar antara 9-10.
B. Asilasi
Gugus amino dari suatu asam amino dapat dengan mudah diasilasi dengan suatu halida asam ataupun anhidrida asam untuk menghasilkan amida. Karena nitrogen amida tidak bersifat basa, suatu asam amino terasilasi tidak membentuk ion dipolar. Karena alasan ini, asam amino terasilasi menunjukan sifat-sifat fisis yang khas dari senyawa organik bukannya sifat fisis dari garam. Dalam sintesis peptida (protein pendek), gugus N-asil digunakan sebagai suatu gugus blokade.
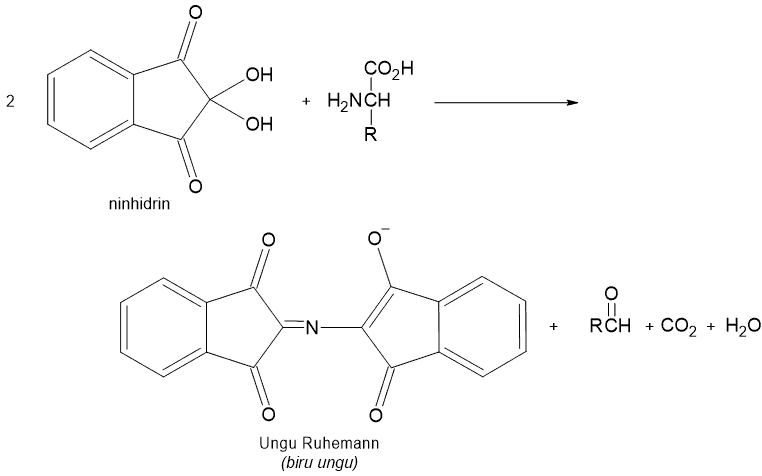
C. Reaksi dengan Ninhidrin
Asam amino bereaksi dengan ninhidrin untuk membentuk produk yang disebut ungu Ruhemann. Reaksi ini biasa digunakan sebagai uji bercak untuk mendeteksi hadirnya asam amino pada kertas kromatografi. Karena reaksi ini bersifat kuantitatif, reaksi ini digunakan sebagai penganalisi asam amino yang diotomasi serta instrumen-instrumen yang menetapkan presentase asam amino yang ada dalam suatu sampel.
Peptida
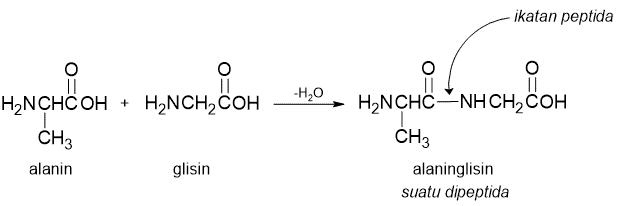
Peptida adalah suatu asam amida yang dibentuk dari dua asam amino atau lebih. Ikatan peptida adalah ikatan amida antara suatu gugus α-amino dari satu asam amino dan gugus karboksil dari asam amino lainnya. Contoh peptida berikut adalah yang dibentuk dari alanin dan glisin yang disebut alanilglisin sebagai contoh pembentukan ikatan peptida.
Untuk mempermudah, nama asam amino dalam peptida sering dipisah. Dengan menggunakan nama singkatan, alaniltirosilglisin menjadi ala-tyr-gly.
Ikatan dalam Peptida
Ikatan amida memiliki karakter rangkap yang disebabkan oleh tumpang tindih parsial orbital p dari gugus karbonil dengan pasangan elektron menyendiri dari nitrogen.
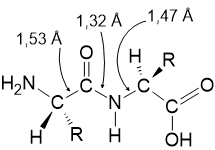
Bukti mengenai karakter ikatang rangkap suatu ikatan peptida terdapat dalam panjang ikatan. Panjang ikatan dari ikatan peptida lebih pendek dari pada panjang ikatan dari ikatan tunggal yang lazim: 1,32 Å dalam ikatan peptida dibandingkan dengan 1,47 Å untuk ikatan tunggal yang khas dalam suatu amina.
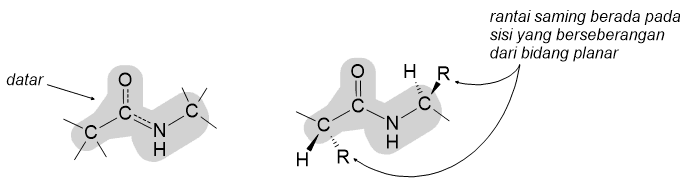
Karena karakter ikatan rangkap dari ikatan peptida, rotasi gugus mengelilingi ikatan ini agak terhambat, dan atom-atom yang terikat pada gugus karbonil dan pada N semuanya terletak dalam satu bidang. Analisis sinar-X menunjukan bahwa rantai samping asam amino di sekitar bidang ikatan peptida berada dalam hubungan tipe trans. Stereokimia ini meminimalkan halangan sterik antara rantai samping.
Beberapa Peptida yang Menarik
Meskipun kebanyakan protein berupa molekul yang besar, suatu peptida tidak perlu mengandung ribuan residu asam amino untuk memiliki aktivitas biologis. Perhatikan tripeptida berikut:
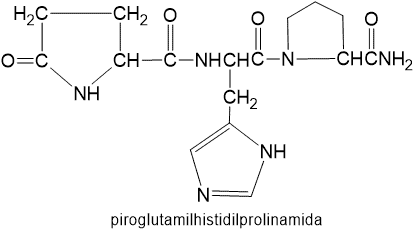
Tripeptida ini adalah faktor pelepasan hormon tirotropik (TRF) yang diisolasi dari kelenjar hipotalamus babi dan sapi. Bila dimasukan ke dalam tubuh manusia, peptid aini merangsang pengeluaran tirotropin yang selanjutnya merangsang pelepasan hormon-hormon tiroid yang mengatur metabolisme dalam tubuh.
Struktur TRF memaparkan contoh dari variasi struktur yang biasa dijumpai dalam peptida dan protein. Asam amini N-ujung merupakan derivat dari asam glutamat: gugus karboksil rantai samping telah berikatan dengan gugus asam amino bebas dan membentuk suatu laktam (amida siklik).
Residu C-ujung dari TRF adalah suatu amida dari prolin. Amida dari gugus karboksil bebas tidaklah sama sekali asing dalam struktur protein alamiah. Biasanya ini dinyatakan dengan menambahkan pada C-ujung dalam struktur singkatan. Misalnya, gly berarti , tetapi gly- berarti .
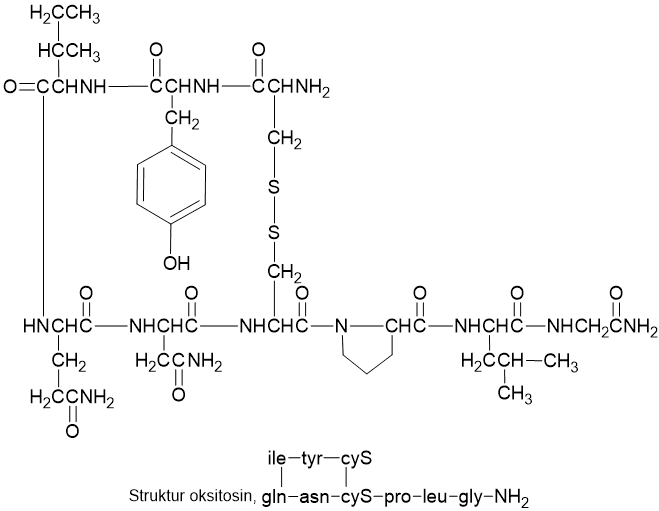
Oksitosin, suatu hormon, berasal dari kelenjar pituitari yang menyebabkan kontraksi uterus selama proses persalinan. Hormon ini adalah peptida yang penting. Struktur oksitosin berupa peptid asiklik yang digabung oleh hubungan sistin .
Enkefalin adalah zat-zat penghilang nyeri yang dihasilkan oleh tubu. Enkefalin berupa peptida-peptida otak yang mengandung hanya lima residu asam amino. Diduga opiat bertindak sebagai analgesik dengan meniru bentuk dan polaritas enkefalin dan meletakan diri pada situs reseptor penghilang nyeri di otak. Dilontarkan teori bahwa “jogger’s high” (perasaan sehat dan segar yang timbul saat jogging) disebabkan oleh pelepasan enkefalin dalam otak.
Penetapan Struktur Peptida
Untuk mendapatkan struktur peptida kita perlu mengurai atau menghidrolisis asam amino dari peptida tersebut satu per satu dan dianalisa melalui teknik kromatografi atau elektroforesis. Dengan cara ini, ahli kimia dapat mengetahui banyaknya residu asam amino, identitas residu asam amino, dan banyaknya residu masing-masing asam amino dalam peptida aslinya. Tetapi informasi ini tidak memberikan informasi mengenai urutan untaian asam amino penyusun peptida tersebut. Nah, untuk menentukan atau mengurai informasi mengenai untaian asam amino penyusun peptida, telah dikembangkan suatu teknis dan yang pertama adalah analisa residu-ujung.
A. Analisa Residu Ujung
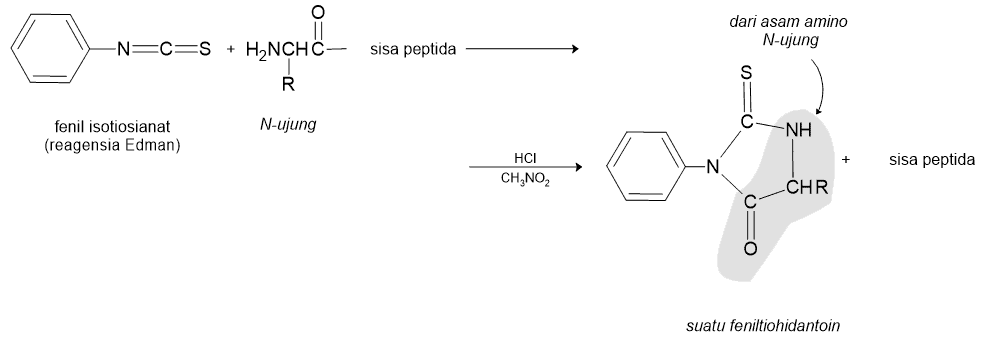
Reagensia Edman. Analisa dari N-terminal dapat diperoleh dengan mengolah peptida dengan fenil isotiosoanat (regensia Edman, diambil dari nama ahli biokimia Swedia P. Edman yang mengembangkan teknik ini). Isotiosianat akan menjalani reaksi dengan gugus asam amino bebas dalam sederat tahap yang akhirnya menghasilkan pemaksapisahan asam amino N-ujung dari dalam peptidanya dan membentuk feniltiohidantoin (PTH), suatu dervat asam amino yang dapat diisolasi dan ditentukan cirinya. Reaksi pemaksapisahan ini dilakukan dengan memanaskan zat-antara adisi (adduk) dengan asam dalam suatu pelarut bebas-air seperti nitrometana (seandainya ada air, peptida keseluruhan akan terhidrolisis).
Mengapa kemudian kita tidak apat meneruskan pengolahan peptida itus ecara bertahap dengan fenil isotiosianat? Dalam tiap residu N-ujung dapat dipatahkan sampai seluruh peptida itu terdegradasi dan urutan asam amino itu ditetapkan. Sampai batas tertentu hal itu dapat dilakukan. Tetapi, tiap siklus pembentukan tiourea dan hidrolisis akan mengakibatkan suatu hdirolisis-dalam pada sisa peptida itu. Setelah sektiar 20-30 siklus, hidrolisis peptida itu telah cukup untuk menghasilkan banyak peptida yang lebih kecil, yang masing-masing memiliki suatu residu N-ujung. jadi, feniltiohidantoin tidak lagi berasal dari suatu gugus ujung tunggal, tetapi merupakan campuran yang berasal dari keanekaragaman gugus ujung. Akhir-akhir ini, penganalisis peptida terotomasi yang disebut sequenator telah digunakan untuk mendegradasi dan menganalisa peptida dengan 20 – 60 residu asam amino.
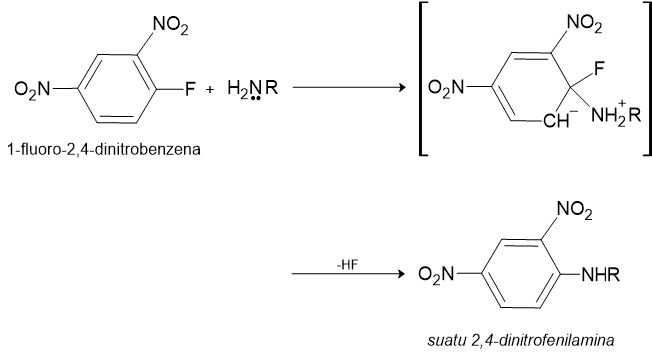
Reagensia Sanger. Suatu reagensia lain yang berguna untuk menetapkan residu N-ujung adalah regensia Sanger, 1-fluoro-2,4-dinitrobenzena. Gugus fluoro dari regensia Sanger dapat mengalami substitusi nukleofilik aromatik dengan amina. Substitusi itu mudah karena zat-antara-karbanion distabilkan oleh gugus nitro.
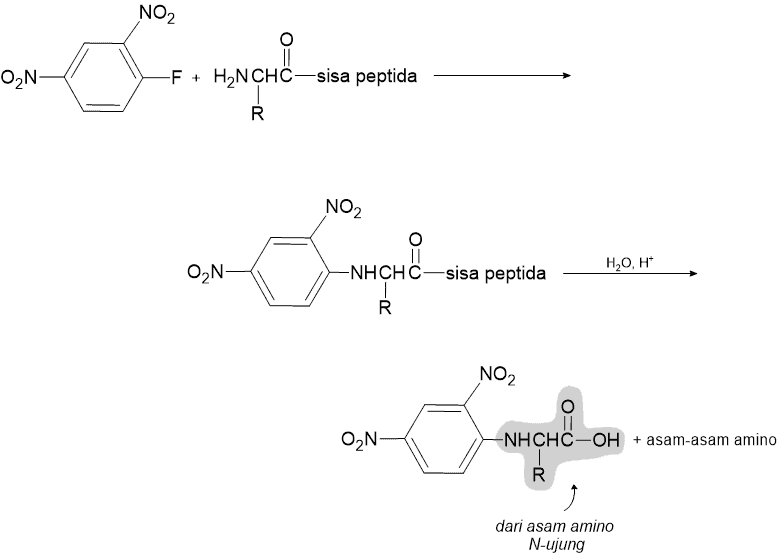
Reagensia Sanger mudah bereaksi dengan asam amino N-ujung dari suatu peptida dan mengubah asam amino itu menjadi gugus arilamino. Setelah peptida yang ditangani itu dihidrolisis lengkap, asam amino N-ujung tetap terikat pada gugus 2,4-dinitrofenil dan karena itu dapat dipisahkan dari asam-sam amino lain dan diidentifikasi. Kekurangan utama penggunaan reagensia Sanger adalah bahwa suatu peptida tidak dapat didegradasi menjadi asam amino tiap kali, seperti halnya dalam degradasi Edman.
Reagensia Sanger dikembangkan oleh Sir Frederick Sanger, yang memenangkan hadiah Nobel tahun 1958 karena pertama kali menetapkan rentetan asam amino secara lengkap dari protein insulin.
Kesimpulan
Asam amino adalah molekul organik kecil yang berfungsi sebagai bahan penyusun dasar protein, masing‑masing tersusun atas satu atom karbon pusat yang terikat pada gugus amino, gugus karboksil, satu atom hidrogen, dan rantai samping yang bervariasi yang memberikan sifat khas pada setiap asam amino. Protein merupakan molekul besar dan kompleks yang terbentuk ketika asam‑asam amino saling terhubung dalam rantai panjang melalui ikatan peptida dan kemudian melipat membentuk struktur tiga dimensi tertentu. Struktur ini menentukan fungsi protein, sehingga protein dapat berperan sebagai enzim yang mempercepat reaksi kimia, komponen struktural yang menyokong sel dan jaringan, molekul pensinyalan seperti hormon, atau sistem pertahanan seperti antibodi. Secara umum, protein sangat penting bagi hampir seluruh proses biologis, memungkinkan pertumbuhan, perbaikan, metabolisme, dan pemeliharaan kehidupan secara keseluruhan.
Referensi
- Fessenden RJ, Fessenden JS. Organic chemistry. 3rd ed. Belmont: Wadsworth; 1986.

Seorang dokter, saat ini sedang menjalani pendidikan dokter spesialis penyakit dalam FKUI. Peminat berbagai topik sejarah dan astronomi.