Awalnya pembahasan antara transkripsi DNA dengan sintesis protein digabungkan dalam satu artikel. Namun, karena tidak semua transkripsi DNA diteruskan ke proses translasi RNA, maka akhirnya pembahasan kedua proses ini dipisahkan ke dalam dua artikel yang berbeda. Untuk artikel ini, di dalamnya akan membahas mengenai proses sintesis protein. Sebagai gambaran, proses ini dimulai dari translasi mRNA menjadi protein, kemudian protein tersebut akan lebih lanjut dimodifikasi sehingga akhirnya menghasilkan protein yang matur.
Daftar Isi
Translasi RNA: Sintesis Protein dari RNA
Beberapa gen menghasilkan produk akhir berupa molekul RNA (contohnya snRNP dan rRNA) tanpa dilanjutkan ke sintesis protein. Namun, sebagian besar gen akan menghasilkan mRNA yang merupakan molekul intermediet dalam produksi atau sintesis protein. Kita akan membahas bagaimana informasi yang dibawah oleh mRNA diproses dan ditranslasikan menjadi molekul protein.
Kode Genetik pada mRNA Berupa Satu Set Tiga Nukleotida
Proses perubahan satu untaian mRNA menjadi satu untaian protein mendapat perhatian para ilmuwan terutama pada tahun 1950-an. Terdapat pertanyaan besar saat itu mengenai bagaimana sekuens nukleotida dari mRNA diubah menjadi protein. Hal ini dikarenakan struktur mRNA berupa asam nukleat sedangkan protein berupa asam amino.
Hal pertama adalah terdapat perbedaan jumlah kode antara mRNA dengan protein. Masalah ini terjadi karena pada RNA hanya terdiri dari empat basa nukleotida (A, U, C, dan G) sedangkan protein mengandung 20 asam amino. Hal ini berarti proses translasi tidak memasangkan satu nukleotida ke satu asam amino. Berarti, terdapat “kode genetik” yang terdiri dari lebih dari satu nukleotida untuk diterjemahkan menjadi satu asam amino.
Kode genetik ini berhasil dipecahkan pada awal 1960-an. Sekuens nukleotida dari mRNA dibaca secara konsekutif dan terdiri dari satu grup beranggotakan tiga nukleotida. Dikarenakan pada RNA terdapat empat nukleotida, maka akan menghasilkan 64 kode genetik (4 x 4 x 4). Kode gentik ini dinamakan codon.
Di satu sisi terdapat 64 kode genetik sedangkan di sisi lain ada 20 asam amino. Berarti, asam amino dikodekan lebih dari satu kode genetik. Selain itu, kode genetik codon ini juga mengkodekan tanda berhenti translasi. Oleh sebab itu, codon mengkodekan asam amino atau kode stop translasi. Adapun codon yang sekarang kita ketahui adalah sebagai berikut:


Reading Frame mRNA
Reading frame artinya cara membagi sekuens nukleotida secara berurutan/konsekutif, tanpa pengulangan, dan tanpa tumpang tindih dari mRNA menjadi susunan blok yang terdiri dari tiga nukleotida (satu codon) untuk setiap blok. Reading frame ini menentukan jenis asam amino yang akan dihasilkan oleh setiap mRNA.
Dikarenakan codon tediri dari tiga nukleotida, maka satu sekuens RNA dapat menghasilkan tiga reading frame yang berbeda. Hal ini tergantung dari di mana proses pembacaan dimulai. Namun, hanya ada satu reading frame yang menghasilkan protein yang benar. Nanti akan dibahas bagaimana mekanisme sel mengenali reading frame yang sesuai dan mencegah kesalahan translasi. Perhatikan contoh gambar di bawah ini:

Pada Sintesis Protein, tRNA Memasangkan Asam Amino dengan Codon pada mRNA
Codon pada mRNA tidak secara langsung mengenali asam amino yang dikodekannya. Codon tidak berkontak atau berikatan langsung dengan asam amino yang dikodekan. Codon mengenali asam amino melalui perantara molekul lain atau molekul adaptor dimana di satu sisi dapat berikatan dengan codon dan di sisi yang lain mengikat asam amino. Adaptor ini merupakan molekul yang tersusun atas RNA kecil yang terikat dengan asam amino. Adapun nama dari molekul adaptor ini adalah transfer RNA (tRNA). Nukleotida pada tRNA memiliki panjang kurang lebih 80 nukleotida.
Kita singgung dalam artikel lain bahwa RNA dapat melipat membentuk struktur khusus. tRNA adalah contoh dalam pelipatan tersebut. Molekul ini memiliki empat segmen yang terlipat akibat double helix pendek. Struktur ini secara dua dimensi membentuk struktur mirip daun semanggi. Struktur daun semanggi ini kemudian melipat lebih jauh lagi sehingga membentuk struktur tiga dimensi seperti huruf “L”. Struktur tiga dimensi ini dipertahankan dengan bantuan interaksi ikatan hidrogen antara region molekul dalam tRNA.
Terdapat dua region dimana nukleotida tidak berpasangan. Keduanya berada di kedua ujung bentuk “L” . Region tersebut berperan sangat penting menjalankan fungsi tRNA dalam sintesis protein. Salah satu dari region ini membentuk anti-codon, set tiga nukleotida yang merupakan pasangan komplementer dari codon di mRNA. Adapun satu region lain berikatan dengan asam amino. Regio ini berupa untaian single strand di ujung 3′ dari tRNA.
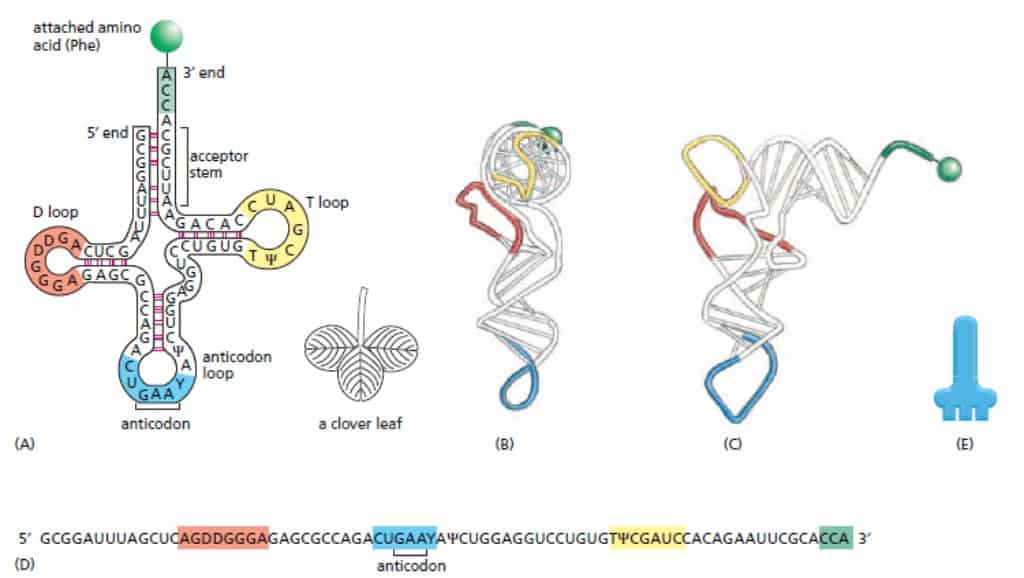
Wobble Position pada Codon dan Anti-Codon
Kita telah melihat bahwa jumlah codon banyak yang bersifat redundat yakni satu asam amino dikodekan lebih dari satu kodon. Dalam arti lain, satu tRNA bisa berpasangan dengan lebih dari satu kodon. Hal terjadi karena beberapa tRNA dapat membentuk pasangan hanya dengan kecocokan dua basa nukleotida pertama saja.
Codon-codon tersebut memang memiliki kesamaan di basa nukleotida pertama dan kedua. Adapun basa ketiga bisa terjadi mismatch atau ketidakcocokan sehingga basa ketiga ini disebut wobble position. Wobble position ini menjelaskan kenapa codon-codon alternatif hanya memiliki perbedaan di basa nukleotida ketiga.
Pada bakteri, wobble position memungkinkan mencocokan 20 jenis asam amino dengan 61 codon dan 31 jenis tRNA. Jumlah jenis tRNA ini berbeda dari satu spesies ke spesies lain. Adapun manusia memiliki hampir 500 gen tRNA namun semuanya hanya memproduksi 48 anti-codon yang berbeda.

Molekul tRNA Dimodifikasi Sebelum Meninggalkan Nukleus
Molekul tRNA mengalami modifikasi sebelum meninggalkan nukleus. Seperti dijelaskan pada artikel mengenai transkripsi DNA, tRNA disintesis dalam bentuk RNA prekursor yang kemudian dipotong dan diolah menjadi tRNA yang matur. Seperti pada mRNA, prekursor tRNA juga memiliki intron. Namun, pada tRNA pemotongan intron dilakukan oleh protein (tRNA-splicing endonuclease). Proses pemotongan dan splicing dari intron tRNA hanya terjadi apabila tRNA melipat dalam bentuk daun semanggi.

Semua molekul nukleotida tRNA juga dimodifikasi secara kimia. Satu dari sepuluh nukleotida pada tRNA yang matur mengalami perubahan dari standar G, U, A, atau C. Diketahui terdapat sekitar 50 jenis modifikasi tRNA yang berbeda.

Beberapa modifikasi nukleotida dari tRNA terutama inosine diproduksi melalui reaksi deaminasi dari adenosine. Perubahan ini mempengaruhi konformasi dan pemasangan dengan anti-codon sehingga memfasilitasi pengenalan dan pemasangan codon mRNA dengan molekul tRNA. Efek lain dari modifikasi ini adalah menambah akurasi penempelan tRNA dengan asam amino yang tepat.
Enzim Spesifik Memasangkan Setiap Asam Amino ke Masing-masing Molekul tRNA yang Sesuai
tRNA berfungsi membawa asam amino dan kemudian mencocokannya dengan codon yang ada di mRNA. Namun, bagaimana produksi tRNA sendiri? Apakah proses yang mencocokan anti-codon dengan asam amino yang dibawanya?
Ternyata proses mencocokan ini dijalankan oleh enzim aminoacyl-tRNA synthetase. Enzim ini memasangkan asam amino dan menggabungkannya secara kovalen dengan tRNA. Kebanyakan sel memiliki enzim aminoacyl-tRNA synthetase yang khusus untuk tiap asam amino (20 jenis enzim). Namun, beberapa bakteri memiliki kurang dari 20 synthetase. Dalam kasus ini, satu synthetase memasangkan satu jenis asam amino ke dua tipe tRNA yang berbeda.

Terdapat enzim kedua yang mengkoreksi kesalahan yang dilakukan oleh synthetase. Sistem ini menjaga agar tRNA yang diproduksi sesuai dengan pasangan asam amino yang dibawanya.
Synthetase mengkatalisasi reaksi kimia dengan menggunakan energi ATP. Reaksi ini menghasilkan ikatan berenergi tinggi. Energi ini kemudian akan digunakan kembali saat proses translasi di ribosom.

Dengan reaksi pembentukan tRNA ini kita dapat mengetahui bahwa proses dekoding dari kode mRNA dilakukan secara dua tahap secara simultan. Tahap pertama adalah dekoding codon dengan anti-codon dan tahap kedua adalah dekoding asam amino dengan tRNA oleh enzim aminoacyl-tRNA synthetase.

Akurasi Produksi tRNA Dijalankan oleh Proses Editing dari tRNA Synthetase
Terdapat mekanisme untuk memastikan tRNA synthetase memproduksi tRNA yang tepat. Pertama, dengan menjaga agar tRNA synthetase memilih asam amino yang tepat.
Proses pemilihan ini terjadi karena pertama, asam amino yang tepat memiliki afinitas yang paling tinggi dengan situs aktif synthetase yang sesuai. Namun, untuk asam amino yang mirip seperti valine dengan isoleucone proses ini tidak cukup.
Mekanisme kedua terjadi pada setelah asam amino diikat dengan AMP. Saat asam amino akan digabungkan ke tRNA, molekul asam amino akan dipaksa dimasukan ke tempat situs kedua. Dimensi molekul yang sesuai diperlukan untuk proses ini.
Ketika asam amino yang salah dimasukan, maka asam amino ini tidak bisa masuk ke situs aktif yang kedua ini. Akhirnya asam amino akan dialihkan ke situs aktif lain yang berfungsi sebagai editing. Di sini, asam amino yang salah akan dilepas dari tRNA. Proses ini mengurangi tingkat kesalahan sehingga menjadi satu kesalahan untuk 40.000 proses pemasangan.
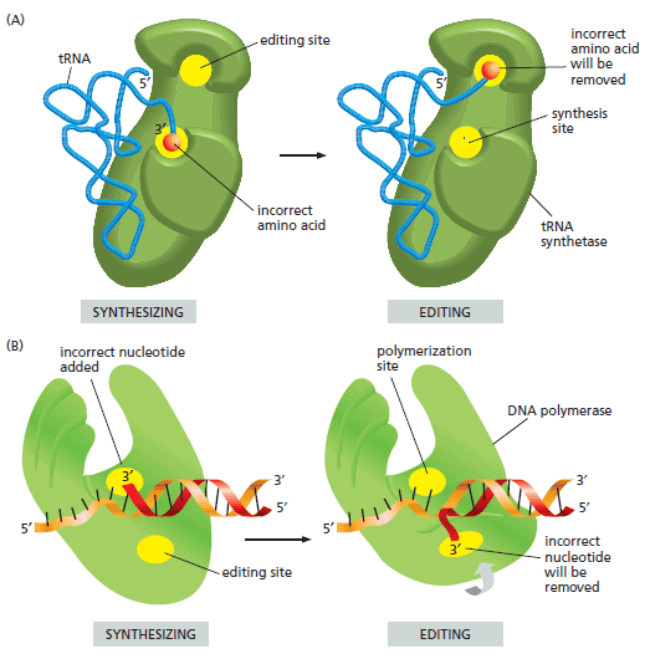
tRNA synthetase juga harus mengenali sekuens tRNA yang tepat. Kebanyakan tRNA-synthetase akan mengenali anti-codon yang dibawa tRNA. Di enzim ini terdapat tiga kantung yang cocok dengan anti-codon spesifik yang terdapat pada tRNA. Terdapat pula proses pengenalan lain dimana enzim mengenali struktur segmen lain dari tRNA.

Asam Amino Ditambahkan ke Ujung C-Terminal dari Rantai Polipeptida yang Sedang Disintesis
Sekarang mari kita lihat bagaimana asam amino dirangkai menjadi protein. Reaksi utama pada proses ini adalah pembentukan ikatan kovalen peptida antara gugus karboksil di ujung rantai asam amino yang sedang dibuat dan gugus amino pada asam amino bebas. Dengan demikian, sintesis protein berjalan dari ujung N-terminal ke ujung C-terminal.
Sepanjang proses ini, ujung karboksil dari peptida yang sedang disintesis terus dalam keadaan teraktivasi. Aktivasi ini dikarenakan adanya ikatan kovalen dengan molekul tRNA melalui ikatan peptidil-tRNA.

Pesan di RNA Dikodekan di Ribosom
Sintesis protein dipandu oleh informasi di mRNA dan dikerjakan di kompleks protein yaitu ribosom. Ribosom merupakan kompleks katalitik besar yang terbentuk dari lebih dari 50 protein yang berbeda (protein ribsomal) dan beberapa molekul RNA (rRNA). Sintesis protein yang dijalankan ribosom cukup akurat dengan hanya satu kesalahan untuk tiap 10.000 asam amino.
Ribosom sangat penting dalam metabolisme sel. Protein adalah makromekul yang sangat penting bagi sel. Karena itu, sel eukariota pada umumnya memiliki jutaan ribosom di sitoplasma.

Subunit ribosom di eukariota dirakit di nukleolus. Molekul rRNA yang baru terbentuk di nukleolus akan dirakit dengan protein ribosomal di sini. Adapun protein ribosomal disintesis di sitoplasma dan dikirim dari sitoplasma ke inti sel. Ketika proses perakitan selesai, maka dua subunit dari ribosom akan dikirim keluar dari inti sel.

Adapun secara desain, ribosom eukariota dan prokariota memilki struktur yang mirip. Keduanya memilki dua subunit yaitu subunir besar dan subunit kecil. Subunit kecil memberi gugus kerja dimana tRNA dapat secara akurat mencocokan diri dengan codon dari mRNA. Adapun subunit besar mengkatalisasi proses pembentukan ikatan peptida.

Proses Sintesis Protein oleh Ribosom
Saat tidak aktif dalam sintesis protein, kedua subunit ribosom berada dalam kondisi terpisah. Keduanya bergabung ketika ada molekul mRNA, diujung 5′ dari mRNA. Ketika sintesis protein berakhir, maka kedua subunit ini akan terpisah kembali.
Ribosom bekerja secara efisien dimana dalam satu detik ribosom sel eukariota dapat menambah dua asam amino ke rantai polipeptida. Ribosom bakteri bahkan berjalan lebih cepat dengan kecepatan 20 asam amino per detik.

Bagaimana ribosom bekerja dengan efisiensi yang tinggi? Diketahui bahwa ribosom memilki empat binding sites terhadap molekul RNA. Satu untuk mRNA dan tiga (situs A, P, dan E) untuk tRNA. Molekul tRNA ditahan di situs A dan P hanya jika antikodon di tRNA membentuk pasangan komplementer dengan codong di mRNA. Situs A dan P berdekatan sehingga membuat dua molekul tRNA dapat berpasangan dengan codon di molekul mRNA.

Ketika proses sintesis protein diinisiasi, setiap asam amino akan ditambahkan ke rantai peptida dengan siklus reaksi yang terdiri dari empat tahap:
- Pengikatan tRNA. Molekul tRNA yang membawa asam amino akan mengikat ke situs A membentuk pasangan basa dengan codon di mRNA.
- Pembentukan ikatan formasi. Saat tRNA bebas berada di situs A, di situs P sudah terdapat tRNA yang terikat ke peptida (ikatan peptidil-tRNA). Ujung karboksil di peptida dilepaskan dari tRNA di situs P dan kemudian digabungkan ke gugus amino di tRNA di situs A membentuk ikatan peptida baru. Proses ini dikatalisasi oleh enzim peptidyl transferase yang terdapat di subunit besar ribosom.
- Translokasi subunit besar. Subunit besar bergeser relatif terhadap posisi subunit kecil yang memegang mRNA. Hal ini menyebabkan tRNA bergerak dari situs A ke situs P dan dari situs P ke situs E.
- Translokasi subunit kecil. Subunit kecil kemudian juga bergerak sejauh tiga nukleotida mereset posisi ribosom agar bersiap menerima tRNA yang baru di situs A.

Sebagai hasil dari tahap satu dan dua, seluruh kompleks ribosom bergerak sejauh tiga nukleotida sepanjang mRNA dan bersiap untuk memulai siklus selanjutnya.
Faktor Elongasi Mendorong dan Memperbaiki Akurasi Proses Translasi mRNA
Selain langkah dasar di atas, terdapat faktor tambahan yang menambah efisiensi dan keakuratan proses translasi. Dua faktor elongasi masuk dan keluar ribosom saat proses translasi dan tiap faktor menghidrolisis GTP menjadi GDP.
Kedua faktor ini adalah EF-Tu dan EF-G pada bakteri dan EF1 dan EF2 pada eukariota. Sebenarnya tanpa kedua faktor ini, ribosom dapat menjalankan proses translasi. Namun prosesnya menjadi sangat lambat, tidak efisien, dan rentan kesalahan. Walaupun proses detilnya masih belum diketahui, namun kedua faktor diyakini terlibat dalam mengatur posisi RNA di ribosom.
EF-Tu atau EF1 akan secara simultan mengikat GTP dan aminoasil-tRNA. Faktor ini membantu akurasi translasi dengan beberapa cara. Pertama, mengantar aminoasil-tRNA ke ribosom. EF-Tu mengecek apakah pasangan tRNA-asam amino sudah tepat. Proses ini tidak diketahui dengan pasti namun diperkirakan pasangan tRNA-asam amino yang tepat memiliki afinitas yang tepat dengan EF-Tu.
Kedua, EF-Tu memonitor interaksi awal antara anti-codon dengan aminoasil-tRNA yang datang dan codon dari mRNA di A-site. Aminoasil-tRNA akan sedikit bengkok ketika berinteraksi dengan EF-Tu. Bentuk ini memungkinkan pemasangan codon namun mencegah memasukan asam amino ke peptida yang sedang diproduksi.
Apabila pasangan codon-anticodon tepat, ribosom akan menghidrolisis GTP dan EF-Tu kemudian akan melepas aminoasil-tRNA dan asam amino di aminoasil-tRNA kemudian dapat digabungkan ke peptida yang sedang diproduksi. Proses ini membantu menambah akurasi proses translasi.
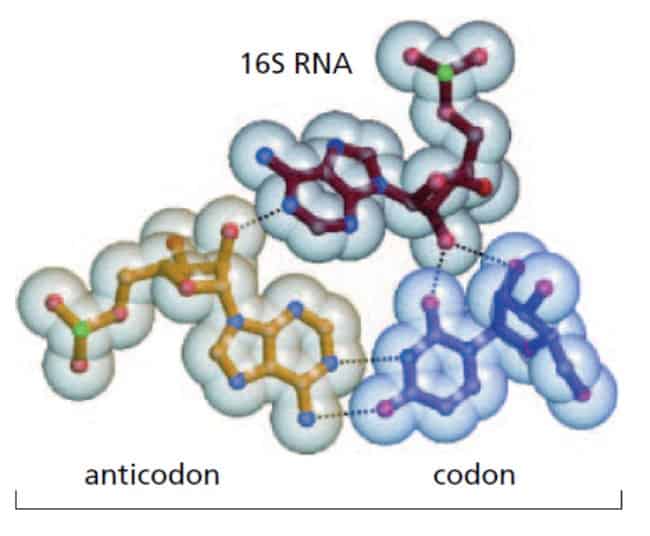
Adapun faktor EF-G membantu dalam proses pemindahan ribosom. Misalnya saat ribosom selesai melepas tRNA, faktor ini akan membantu pergeseran ribosom subunit besar sehingga site-A menjadi kosong dan diikuti dengan pergeseran subunit kecil ribosom.

Ribosom Merupakan Sebuah Ribozim
Telah diterangkan sebelumnya bahwa ribosom terdiri dari kompleks molekul RNA dan protein. Molekul protein hanya meliputi sepertiga bagian dan sebagian besar sisanya berupa RNA. Adapun dari studi molekuler, diketahui bahwa struktur dan fungsi utama ribosom dijalankan atau diperankan oleh RNA bukan oleh protein.

Adapun protein dari ribosom biasanya menempati bagian permukaan dan mengisi sela-sela di ribosom. Beberapa protein ini ada yang memiliki bagian polipeptida yang masuk mendekati inti ribosom. Tampaknya fungsi utama dari protein ribosomal ini adalah untuk menstabilisasi inti RNA. Selain itu, protein di ribosom juga membantu perakitan awal dari rRNA yang membentuk inti dari ribosom.

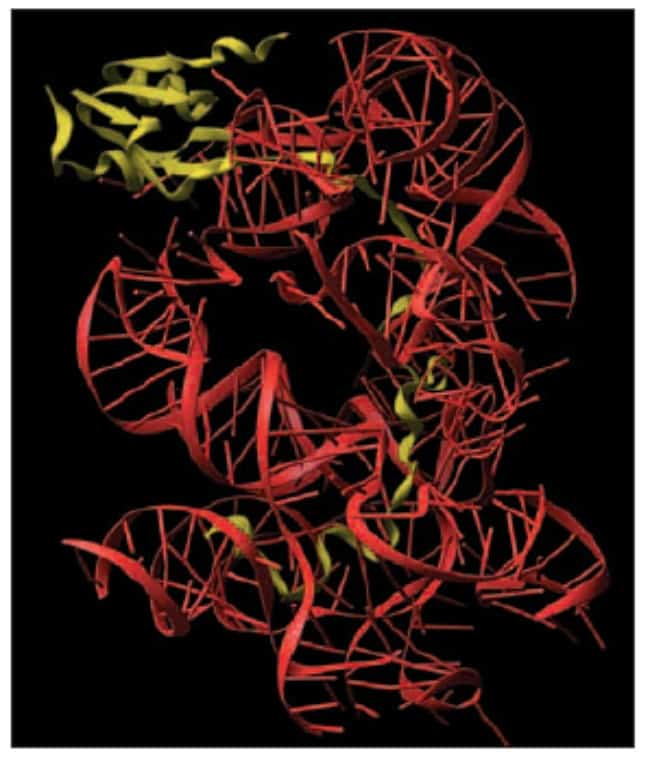
Selain dari situs ikat (binding site) dari ribosom, tRNA juga berperan dalam mengkatalis reaksi di ribosom. Fakta ini cukup mengejutkan peneliti karena sebelumnya biasanya reaksi katalis diperankan oleh protein. Apalagi RNA umumnya tidak memiliki gugus molekul yang dapat mudah terionisasi. Selain itu, di inti ribosom juga tidak terdapat ion metal yang sering kali digunakan molekul RNA untuk mengkatalisasi reaksi kimia.
Ternyata, kemudian diketahui bagwa rRNA 23S membentuk serupa kantung yang sangat terstruktur. Kantung ini berupa jaringan ikatan hidorgen yang mengorientasikan secara tepat reaktan sehingga bisa membantu terciptanya ikatan kovalen. Selain itu, RNA pada P-site berkontribusi dengan menyuplai gugus fungsional OH dalam reaksi katalis.
Molekul RNA yang memilki aktivitas proses katalitik dinamakan ribozim. Kita dapat menyimak reaksi ribozim lainnya yaitu pada proses splicing RNA. Begitu pula pada proses translasi atau sintesis protein, karena ribosom pada dasarnya merupakan RNA dengan aktivitas katalitik, maka ribosom juga termasuk ribozim.
Sekuens Nukleotida di mRNA Sebagai Sinyal Dimulainya Sintesis Protein
Untuk memulai sintesis protein, terdapat tanda atau sinyal khusus yang dibawa oleh mRNA. Sinyal ini penting karena menentukan reading frame yang tepat. Kita pelajari sebelumnya bahwa kesalahan memulai membaca mRNA pada tempat nukleotida yang salah akan menghasilkan peptida yang salah.
Adapun sinyal pada mRNA dalam memulai sintesis protein atau translasi RNA adalah codon AUG. Pasangan dari codon ini adalah tRNA khusus yang dikenal sebagai tRNA inisiator. tRNA inisiator ini selalu membawa asam amino methionine (pada bakteri, asam amino methionine yang dimodifikasi, formylmethionine). Tentu saja hasilnya nanti adalah protein yang memiliki gugus pertama terminus-N methionine. Mehionine ini kemudian akan dibuang oleh protease spesifik.
Pada eukariota, tRNA-methionine ini membentuk tRNA-methionine complex (Met-tRNAi). Selain itu, terdapat protein tambahan lain yang dikenal sebagai eucaryotic initiation factors (eIF).
Dari semua jenis aminoasil-tRNA, hanya tRNA-methionine yang dapat berikatan secara kuat dengan subunit kecil ribosom tanpa perlunya subunit ribosom lainnya lengkap. tRNA-methionine ini juga langsung berikatan di P-site. Selanjutnya, subunit kecil ribosom akan berikatan dengan ujung 5′ mRNA berkat adanya cap dan dua faktor inisiator eIF4E (berikatan ke cap 5′ mRNA) dan eIF4G. Kemudian subunit kecil ribosom bergerak dari 5′ ke arah 3′ mRNA mencari sinyal AUG pertama.
Terdapat faktor inisiasi tambahan lain yang bertindak sebagai helikase dan memfasilitasi pergerakan ribosom melalui struktur sekunder dari mRNA. Ingat, mRNA juga dapat membentuk struktur sekunder seperti heliks.
Pada 90% mRNA, translasi dimulai di AUG pertama yang ditemui. Di titik ini, faktor inisiator akan terdisosiasi dan diikuti dirakitnya subunit besar ribosom sehingga ribosom menjadi lengkap. Adapun tRNA inisiator tetap berada di P-site dan A-site masih kosong. Pada kondisi ini, proses sintesis protein siap untuk dimulai.


Fenomena Leaky Scanning pada Sintesis Protein
Nukleotida yang berada disekitar tempat codon mulai translai dimuai mempengaruhi efisiensi dari pengenalan codon AUG. Nukleotida konsensus pengenalan ini adalah 5′-ACCAUGG-33. Jika pola ini berbeda, biasanya codon AUG pertama tidak dipindai dan dilompat ke AUG kedua atau ketiga.
Fenomena dilompatinya codon AUG pertama ini dinamai leaky scanning. Sel menggunakan fenomena ini untuk menghasilkan dua atau lebih jenis protein yang berbeda dari segi N-terminus dari protein-protein tersebut. Hal ini memungkinkan gen untuk menghasilkan protein yang sama dengan atau tanpa sekuens sinyal di N-terminus.
Contoh manfaat dari fenomena ini misalnya jika protein yang dihasilkan akan dikirim ke dua kompartemen yang berbeda di dalam sel. Perbedaan sekuens sinyal menentukan ke arah kompartemen mana protein akan dikirim.
Pada bakteri, mekanisme pemilihan start codon berbeda. mRNA bakteri tidak memiliki 5′ cap untuk menandai ujung mulai sintesis protein. Dalam kondisi ini, bakteri mempunyai sinyal khusus di ujung 5′ mRNA berupa sekuens spesifik yang dinakan sekuens Shine-Dalgarno. Sekuens konsensus ini adalah 5′-AGGAGGU-3′ yang membentuk pasangan basa dengan 16S rRNA di subunit kecil dari ribosom. Faktor inisiator translasi lainnya membantu interaksi ini dan juga menuntun penyusunan subunit besar ribosom untuk melengkapi mesin translasi pada bakteri.
Dengan mekanisme ini, ribosom bakteri dapat langsung terakit di awal codon yang terletak di interior dari mRNA. Sifat ini dikenal dengan nama polycistronic sehingga mRNA dapat mengkodekan langsung beberapa jenis protein. Hal ini berbeda dari mRNA eukariota yang hanya mengkodekan satu protein.

Codon Stop Menandai Berakhirnya Sintesis Protein
Akhir dari translasi ditandai dengan codon stop yaitu salah satu dari UAA< UAG, atau UGA. Codon stop ini tidak dikenal oleh tRNA dan tidak mengkodekan asam amino tertentu. Namun, codon tersebut menandai berakhirnya translasi.
Terdapat protein yang dikenal sebagai release factor berikatan dengan ribosom dengan codon stop yang berposisi di A-site. Konfigurasi ini akan memaksa peptidyl transferase mengkatalisasi tambahan molekul air ke peptidil-tRNA.
Reaksi tadi akan melepaskan ujung kaborksil dari peptida dari ikatannya dengan molekul tRNA dan peptida lalu dilepas dari ribosom. Ribosom kemudian akan melepas mRNA dan subunit besar dan kecil dari ribosom akan terpisah.
Release factor ini adalah contoh dari molecular mimicry dimana satu jenis makromolekul menyerupai makromolekul lainnya. Pada kasus ini, struktur tiga dimensi dari protein release factor menyerupai struktur dan distribusi muatan dari molekul tRNA. Kemiripan ini membantu protein masuk ke A-site dari ribosom dan menyebabkan terminasi dart proses translasi.

Saat translasi, peptida yang baru dibentuk akan bergerak sepanjang saluran air (kira-kira 10 nm x 1,5 nm) di subunit besar ribosom. Dinding dari saluran ini terbuat terutama dari 23S rRNA yang permukaanya banyak ditempeli gugus yang bersifat hidrofobik.
Struktur tersebut berfungsi seperti “teflon” agar peptida dapat bergerak dengan mudah di dalam saluran ribosom ini. Di dalam struktur saluran ini, struktur protein tidak berubah namun beberapa bentuk struktur sekunder seperti α-heliks dapat mulai terbentuk di saluran ini. Agar dapat berfungsi dengan baik, setelah peptida melewati saluran ribosom, harus melipat membentuk konformasi tiga dimensi agar bisa berfungsi dengan baik.

Poliribosom, Tempat Sintesis Protein
Lamanya waktu proses sintesis protein bervariasi dari 20 detik sampai beberapa menit. Saat waktu yang pendek ini, satu mRNA dapat mengalami proses berkali-kali. Ketika ribsom telah mentranslasikan cukup ruang nukleotida di ujung 5′, maka ribosom lain akan memulai proses translasi yang baru. Oleh sebab itu, mRNA sering kali ditemukan dalam bentuk poliribosom atau polisom.
Poliribosom adalah mesin perakitan di sitoplasma berukuran besar yang terbentuk dari beberapa ribosom berjejer dengan jarak sedekat 80 nukleotida sepanjang satu molekul mRNA. Inisisi multipel ini memungkinkan sel untuk dapat membuat banyak protein sekaligus.

Baik bakteri maupun eukariota menggunakan poliribosom dan menggunakan strategi tambahan untuk menambah kecepatan sintesis protein. Dikarenakan mRNA bakteri tidak diproses dan langsung dapat ditranlasikan sewaktu disintesis, maka sering didapat RNA polimerase di satu ujung diikuti oleh ribosom setelahnya.
Variasi Minor dari Kode Genetik Standar
Kode genetik dari codon berlaku secara universal untuk semua tiga kingdom makhluk hidup (prokariota, eukariota, dan archaea). Namun, terdapat beberapa pengecualian yang jarang dari kode ini. Misalnya Candida albicans memiliki kode codon CUG untuk serine sedangkan makhluk hidup lainnya mengkodekan CUG untuk leucne.
Mitokondria sering kali memiliki kode tersendiri. Sebagai contoh pada mitokondria mamalia, AUA ditranslasikan sebagai methionine sedangkan disitosol ditranslasikan sebagai isoleucine.
Tipe variasi lain yang disebut translation recoding muncul di banyak sel. Pada kasus ini, informasi sekuens nukleotida yang ada di mRNA dapat merubah arti dari kode genetik di tempat khusus dari mRNA. Kode genetik standar memberikan kode untuk 20 asam amino namun pada makhluk hidup terdapat asam amini ke-21 yang dapat dimasukan ke protein. Selenocystein merupakan asam amino esensial untuk banyak enzim agar dapat berfungsi. Asam amino ini memiliki atom selenium sebagai ganti dari atom sulfur.
Selenocystein diproduksi secara enzimatik dari serine yang terikat pada tRNA khusus yang berpasangan dengan codon UGA dimana pada kondisi biasa merupakan codon stop. Molekul mRNA yang dimana protein yang dihasilkan harus mengandung selenocystein mengandung sekuens nukleotida tambahan yang memungkinkan insersi selenocystein terjadi.

Bentuk lain dari rekoding adalah translational frameshifting dimana memungkinkan lebih dari satu protein disintesis dari saru mRNA. Retrovirus umumnya menggunakan translational frameshifting untuk membuat protein capsid (protein Gag), enzim reverse transcriptase, dan integrase (protein Pol) dari transkrip RNA yang sama.
Virus membutuhkan lebih banyak protein Gag dibandingkan protein Pol. Penyesuaian jumlah ini dicapai dengan mengkodekan gen Pol setelah gen Gag namun dengan reading frame yang berbeda.
Protein Pol diproduksi dalam jumlah yang kecil karena sering kali translational frameshift menyebabkan codon stop dari protein Gag dilewati. Proses ini terjadi di codon tertentu dari mRNA dan membutuhkan sinyal rekoding khusus.

Inhibitor Sintesis Protein Prokariota Bermanfaat Sebagai Antibiotik
Banyak antibiotik diperoleh dari jamur yang berfungsi menghambat sintesis protein pada bakteri. Jamur dan bakteri saling bersaing di lingkungan untuk hidup. Salah satu mekanisme agar jamur dapat menyaingi bakteri adalah dengan memproduksi zat yang menghambat bakteri.
Zat-zat inhibitor ini memanfaatkan perbedaan struktur dan fungsi ribosom antara prokariota dan eukariota sehingga spesifik menghambat ribosom bakteri namun tidak menghambat ribosom jamur (jamur termasuk eukariota). Dengan demikian, zat ini dalam jumlah besar juga tidak atau sedikit berpengaruh pada jamur maupun manusia.

Banyak antibiotik bersarang di kantung ribosom bakteri dan dengan demikian, menghambat kerja dari ribosom. Tabel di bawah ini berisi daftar antibiotik dan mekanismenya dalam menghambatan sintesis protein pada bakteri.
| Inhibitor | Efek Spesifik |
|---|---|
| Pengaruh hanya pada bakteri | |
| Tetrasiklin | Menghambat ikatan aminoasil-tRNA ke site-A ribosom |
| Streptomisin | Menghambat transisi dari inisiasi ke elongasi dan juga menyebabkan kesalahan koding |
| Kloramfenikol | Menghambat reaksi peptidil transferasi dari ribosom |
| Eritromisin | Berikatan ke saluran keluar dari ribosom sehingga menghambat elongasi rantai peptida |
| Rifamisin | Menghambat inisiasi rantai RNA dengan berikatan pada RNA polimerase (menghambat sintesis RNA) |
| Pengaruh pada bakteri dan eukariota | |
| Puromycin | Menyebabkan pelepasan prematur rantai polipeptida karena zat ini ditambahkan ke rantai peptida yang sedang disintesis |
| Actinomycin D | Berikatan dengan DNA dan menghambat pergerakan RNA polimerase (menghambat sintesis RNA) |
| Pengaruh hanya pada eukariota | |
| Cycloheximide | Menghambat reaksi translokasi di ribosom (langkah 3) |
| Anisomycin | Menghambat reaksi peptidil-transferase dari ribosom |
| α-Amanitin | Menghambat sintesis mRNA dengan berikatan secara khusus dengan RNA polimerase II |
Akan tetapi, dikarenakan ada persamaan mekanisme sintesis protein bakteri dengan mitokondira, beberapa obat seperti kloramfenikol dapat menghambat sintesis protein di mitokondria. Namun, ada juga obat seperti puromycin menghambat sintesis protein baik di eukariota maupun prokariota. Hal ini disebabkan mekanisme puromycin inhibitor analog molekul tRNA yang memiliki kesamaan struktur baik di prokariota maupun eukariota.

Proses Menjaga Akurasi Sintesis Protein Membutuhkan Energi
Ribosom dalam sel memiliki keseimbangan antara kecepatan translasi dengan ketepatan translasi. Kedua sisi terebut saling berkebalikan. Semakin cepat ranslasi maka tingkat akurasi akan berkurang begitu juga sebaliknya, semakin akurat maka sintesis protein akan semakin lambat. Memang di laboratorium dapat kita saksikan jenis mutasi pada ribosom bakteri yang dapat meningkatkan keakurasian translasi namun kecepatan sintesis menjadi sangat berkurang sehingga bahkan tidak fit untuk bertahan.
Hubungan terbalik ini disebabkan oleh meningkatnya energi yang dibutuhkan untuk proses perbaikan translasi. Sintesis protein sendiri membutuhkan banyak energi. Dibuuthkan setidaknya empat ATP untuk setiap pembentukan ikatan peptida. Dua untuk pembentukan aminosil-tRNA dan dua digunakan dalam proses langkah translasi oleh ribosom.
Sebagai tambahan, makin banyak ATP digunakan tiap kali ada asam amino yang salah dimasukan dalam translasi. Begitu juga pada sistem proofreading, juga membutuhkan energi. Oleh sebab itu, semakin akurat, energi yang dibutuhkan menjadi lebih banyak dan kecepatan sintesis protein menjadi semakin lambat.
Mekanisme Kontrol Kualitas Mencegah Translasi Molekul mRNA yang Rusak
Di eukariota, RNA hasil transkripsi akan diolah, dimodifikasi, dan kemudian ditranspor dari inti sel ke sitoplasma. Namun, dapat terjadi kerusakan atau kesalahan dari mRNA yang dihasilkan. Terdapat bahaya apabila mRNA yang salah atau rusak ini kemudian ditranslasikan oleh sel.
Untuk mencegah hal tersebut terdapat mekanisme tersendiri. Ujung cap 5′ dan ekor poli-A pertama kali dikenali oleh sistem translasi sebelum proses sintesis protein dimulai. Untuk memastikan bahwa proses splicing intron dilakukan dengan benar, maka sel dapat memeriksanya dengan melihat exon junction compex (EJC). Untuk membaca proses-proses ini, dapat disimak di artikel mengenai transkripsi DNA di tautan ini.
Namun, sistem survailans paling kuat dalam pengenalan mRNA yang rusak adalah nonsense-mediated mRNA decay. Sistem ini menghancurkan mRNA defektif sebelum ditranslasikan menjadi protein. Mekanisme ini aktif ketika mRNA tidak memiliki codon stop (UAA, UAG, atau UGA) atau berada di tempat yang salah.


Proses survailans ini dimulai segera saat mRNA ditranspor ke sitosol. Saat ujung 5′ masuk ke nuclear pore, mRNA akan bertemu dengan ribosom dan mulai ditranslasikan. Saat translasi berlangsung, EJC yang berikatan pada mRNA akan terlepas karena kerja ribosom. Codon stop biasanya berada di ekson terakhir sehingga saat ribosom masuk ke ekson terakhir maka setelahnya sudah tidak ada lagi EJC. Jika hal ini terjadi maka ribosom akan masuk dalam mode inspeksi dan kemudian melepaskan mRNA.
Namun, apabila posisi codon tidak tepat, misalkan berada tempat yang lebih awal, maka setelah ribosom mengenal codon stop, masih ada EJC setelahnya. Jika ribosom mengenali ini, maka ribosom akan memberi sinyal untuk sel kemudian menghancurkan mRNA tersebut.
Bakteri juga memiliki sistem kontrol kualitas dalam proses translasi. Jika terdapat translasi mRNA yang rusak atau tidak lengkap, maka proses translasi terhenti dan ribosom terkunci dengan mRNA. Agar dapat terlepas, terdapat RNA khsusu yaitu tmRNA.
Molekul tmRNA akan masuk ke A-site dari ribosom dan translasi akan berlanjut kembali. Proses ini akan membuat protein yang disintesis memiliki tambahan 11 asam amino khusus di ujung C-terminus. Asam amino khusus ini menjadi sinyal bagi protease untuk menghancurkan protein yang tidak lengkap atau rusak tersebut.

Modifikasi Protein Pascatranslasi (Modifikasi Postranslasional)
Proses sintesis protein tidak selesai di translasi oleh ribosom. Setelah proses translasi, protein harus melakukan serangkaian proses untuk memperoleh bentuk yang matur. Kita ketahui bahwa protein harus memiliki bentuk tiga dimensi spesifik agar bisa berfungsi dengan semestinya. Proses ini berarti protein akan dimodifikasi lebih lanjut setelah proses translasi untuk mencapai bentuknya yang matur.
Beberapa Protein Mulai Melipat Saat Proses Sintesis Sedang Berlangsung
Eskpresi gen tidak selesai saat kode genetik memproduksi protein. Agar dapat berfungsi, maka polipeptida ini harus melalui banyak modifikasi. Pertama, polipeptida melipat untuk membentuk konformasi tiga dimensi yang unik. Kemudian, polipeptida juga perlu mengikat molekul kecil berupa kofaktor untuk memperoleh aktivitas enzimatik. Selain itu, perlu dimodifikasi dengan benar oleh protein kinase atau jenis modifikasi lain, serta dirakit dengan subunit protein lain untuk memperoleh fungsi yang sebenarnya.

Informasi semua proses di atas terdapat di sekuens asam amino yang diproduksi ribosom. Saat peptida melipat membentuk struktur yang kompak, polipeptida akan mengubur residu hidrofobik di bagian dalam. Selain itu, terjadi interaksi dan ikatan nonkovalen antara bagian molekul protein. Semua pembentukan struktur ini mengikuti arah energi dan struktur yang paling stabil dari protein.
Untuk beberapa protein, proses pelipatan ini terjadi segera bahkan saat proses translasi masih berjalan. Pada keadaan ini, beberapa detik setelah domain protein keluar dari ribosom, langsung membentuk struktur kompak. Struktur ini mengandung mayoritas bentuk sekunder (α-helix dan β-sheet) dan tersusun dalam konformasi yang benar.

Kondisi dinamis dan fleksibel ini pada kebanyakan protein disebut molten globule. Keadaan ini adalah titik awal proses panjang dimana nantinya banyak rantai samping disesuaikan agar dapat membentuk struktur tersier yang diharapkan. Bagi kebanyakan protein, diperlukan waktu beberapa menit untuk proses penyesuaian ini.

Proses Pelipatan Protein Dibantu Molekul Pendamping (Chaperone)
Kebanyakan protein tidak melipat secara langsung sewaktu ditranslasikan. Protein ini di ribosom akan bertemu dengan molekul khusus yakni protein pendamping (molecular chaperone). Molekul pendamping sangat penting bagi sel karena banyak bentuk yang dapat diambil protein saat melipat namun hanya satu cara pelipatan yang benar. Tanpa molekul pendamping, banyak protein akan gagal mencapai bentuk yang matur.

Mayoritas dari molekul pendamping ini berupa kelompok heat-shock protein (Hsp). Dinamai Hsp karena saat sel dipaparkan pada peningkatan suhu lingkungan, produksi Hsp akan meningkat secara dramatis. Hal ini juga petanda adanya sistem respon dari sel untuk antisipasi kondisi yang meningkatkan terjadinya kesalahan pelipatan protein.
Hsp memiliki beberapa famili besar di eukariota yaitu Hsp60 dan Hsp70. Tiap famili bekerja di organel yang berbeda. Mitokondria memiliki molekul Hsp60 dan Hsp70 tersendiri yang berbeda dari sitosol. Satu Hsp70 spesial disebut BIP membantu pelipatan protein di retikulum endoplasma.
Protein Hsp60 dan Hsp70 juga bekerja dengan protein kecil lain yang berkaitan saat membantu proses pelipatan protein. Semua jenis Hsp memiliki afinitas yang sama terhadap bagian protein yang hidrofobik. Dalam kerjanya, Hsp dapat menghidrolisis ATP untuk mengikat dan melepas susbtrat protein masing-masing.
Adapun perbedaan antara jenis Hsp adalah sebagai berikut. Hsp70 bekerja sejak awal protein terbentuk, mengikat ke serangkaian tujuh asam amino hidrofobik sebelum protein meninggalkan ribosom.

Adapun Hsp60 membentuk struktur seperti tong atau barel yang bekerja setelah protein secara penuh disintesis. Tipe chaperone ini disebut chaperonin membentuk ruangan isolasi untuk protein yang mengalami kesalahan pelipatan. Hal ini untuk mencegah protein tersebut beragregasi dengan protein lain dan memberikan lingkungan yang mendukung protein untuk kembali melipat ulang.
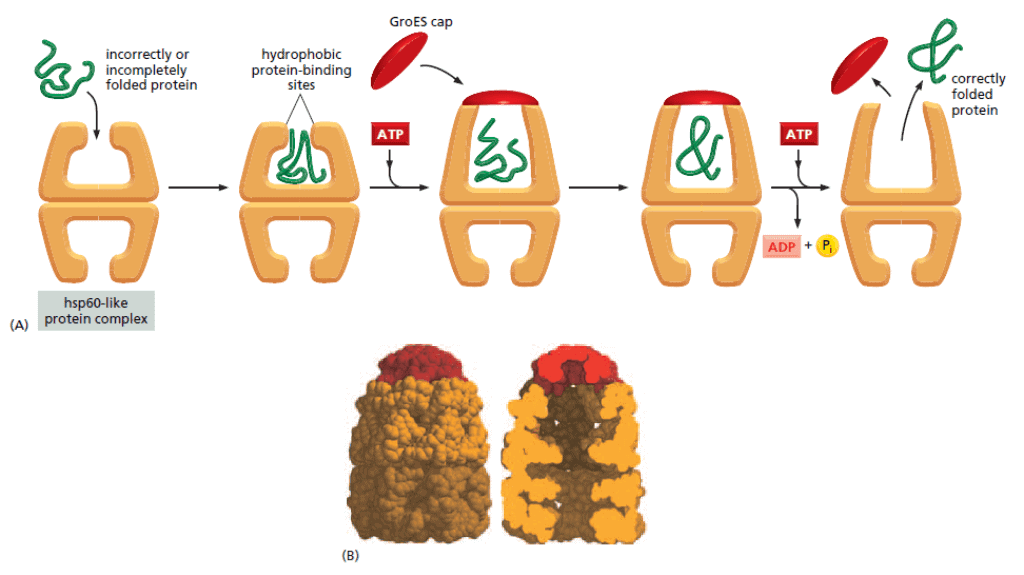
Walaupun telah di sini hanya disebut dua jenis molekul pendamping saja, pada kenyataannya sel mempunyai lebih banyak lagi keluarga chaperone. Banyak protein yang disintesis membutuhkan banyak jenis molekul pendamping dengan mekanisme pendampingan dan kerja yang juga berbeda-beda.
Regio Hidrofobik Protein Menjadi Sinyal Penting untuk Kontrol Kualitas Protein
Seperti dijelaskan sebelumnya bahwa pada proses pelipatan protein, umunya bagian atau regio hidrofobik akan terkubur di bagian dalam protein. Oleh sebab itu, secara umum apabila banyak regio hidrofobik berada di permukaan protein, berarti protein tidak melipat secara benar. Protein yang demikian tidak hanya tidak bermanfaat namun dapat berbahaya bagi sel.
Dari penjelasan di atas, maka salah satu cara sel untuk mengenali protein yang gagal melipat adalah dengan mengenali regio hidrofobik ini. Mekanisme ini melibatkan molekul pendamping yang kita bahas sebelumnya. Chaperone akan menempel ke regio hidrofobik, mencoba memperbaiki protein tersebut, sekaligus melindungi protein lain agar tidak terjadi agregasi.

Dari bagan di atas, tampak bahwa ketika protein yang salah melipat gagal diperbaiki, maka protein tersebut akan dihancurkan. Proses pengenalan protein yang akan dihancurkan juga dengan cara mengenali protein yang memiliki banyak regio hidrofobik di permukaan protein.
Proteasome
Mekanisme proteolitik dan chaperone saling berkompetisi untuk mengenali protein yang salah melipat. Hanya sebagian kecil dari protein baru yang cepat melipat akan didegradasi. Sebaliknya, protein yang proses pelipatannya lama akan lebih terancam proses penghancuran. Apabila terdapat mutasi, biasanya protein tidak akan berhasil melipat dengan benar sehingga biasanya protein yang dihasilkan akan dihancurkan.
Aparatus sel yang berperan dalam penghancuran protein ini adalah proteasome. Protein ini merupakan protease yang memerlukan ATP. Keberadaannya dalam sel cukup banyak, meliputi 1% dari semua protein sel. Selain itu, proteasome juga tersebar merata di sitosol dan inti sel. Sistem di retikulum endoplasma mengawasi pelipatan protein dan apabila protein salah melipat akan mengirim protein tersebut ke sitosol untuk dihancurkan oleh proteasome.
Proteasome sendiri terdiri dari silinder pusat (inti 20S proteasome) yang terbentuk dari beberapa subunit yang tersusun sebagai quasi-silinder dari empat cincin heptamerik. Beberapa subunit ini merupakan protease dengan situs katalitik berada di dinding bagian dalam dari silinder. Struktur ini mencegah protease untuk bekerja sembarangan menghancurkan protein yang normal.

Kedua ujung dari silinder inti proteasome ini berikatan dengan kompleks protein besar (cap 19S) yang mengandung enam subunit protein cincin dimana protein target akan diantar masuk ke inti protrasome untuk dihancurkan.

Proses pemasukan protein ke proteasome ini membutuhkan energi ATP. Energi ini digunakan untuk membongkar lipatan protein dan menggerakan protein masuk ke proteasome. Adapun protein di cap dari proteasome merupakan bagian dari keluarga protein “unfoldase” yang diberi nama protein AAA. Struktur protein AAA ini memiliki kemiripan dengan helikase DNA.

Saat proteasome menghancurkan protein, protein akan tetap terikat dengan proteasome sampai seluruh protein dihancurkan. Cap pada proteasome juga berfungsi sebagai gerbang dan mengenali target protein yang akan dihancurkan.
Proses pengenalan protein yang akan dihancurkan diperankan oleh ubiquitin. Ubiquitin merupakan molekul kecil yang dipergunakan untuk menandai protein yang akan dihancurkan. Protein yang akan dihancurkan ini diikat dengan ubiquitin melalui ikatan kovalen. Cap pada proteasome kemudian mengenali tanda ubiquitin di protein dan kemudian menangkap dan memasukan protein tersebut ke inti proteasome.
Sistem Konjugasi Ubiquitin sebagai Penanda Destruksi Protein
Proses penyiapan ubiquitin dikerjakan oleh ubiquitin-activating enzyme (E1) yang kerjanya membutuhkan ATP. Ubiquitin yang diaktivasi berupa E1-bound ubiquitin akan ditransfer ke salah satu set dari ubiquitin-conjugating enzyme (E2). E2 bekerja dengan berasosiasi dengan protein aksesoris E3. Kompleks E2-E3 ini disebut ubiquitin ligase. Komponen E3 sendiri mengikat ke sinyal degradasi spesifik yang disebut degron di protein substrat.
Ubiquitin ligase ini membentuk rantai poliubiquitin di protein substrat. Di rantai ini, masing-masing ubiquitin disambungkan melalui penyambungan residu C-terminal setiap ubiquitin ke residu asam amino lysine spesifik ubiquitin yang lainnya.

Terdapat sekitar 20 jenis protein E2 yang berbeda dan ratusan jenis protein E3 di mamalia. Oleh sebab itu, sistem ubiquitin-proteasome terdiri dari banyak jalur proteolitik dengan kesamaan enzim E1 di awal dan proteasome di akhir dari jalur proteolitik tersebut. Perbedaan dari setiap jalur adalah komposisi E2-E3 dan protein atau faktor aksesoris tambahan lainnya.
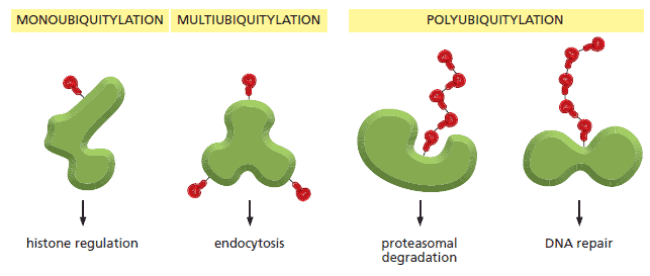
Kontrol Protein Melalui Proteolisis
Selain berfungsi untuk menghancurkan protein yang malfungsi, sistem proteolisis melalui proteasome juga berfungsi untuk meregulasi protein. Beberapa kondisi harus direspon oleh sel untuk merubah konsenterasi protein tertentu dan salah satu caranya adalah dengan proteolisis.
Struktur E3 pada sistem ubiquitinisasi dapat diaktivasi melalui fosforilasi sehingga berubah bentuk dan dapat berikatan dengan protein tertentu. Contohnya adalah anaphase-promoting complex (APC) yang merupakan multisubunit ubiquitin ligase yang diaktivasi oleh siklus sel saat mitosis. APC yang teraktivasi akan menyebabkan degradasi dari siklin dan regulator lainnya.
Mekanisme lainnya adalah perubahan pada protein yang diregulasi. Misalnya dengan perubahan situasi, menyebabkan perubahan struktur protein baik akibat fosforilasi ataupun cara lain yang menyebabkan sinyal ubiquitinisasi yang tadinya terkubur dalam protein menjadi muncul di permukaan protein. Salah satu proses kontrol dengan proteolisis adalah protein HIF dalam proses sensing oksigen di dalam sel.
Proses pengenalan terakhir adalah munculnya sinyal degradasi yang terbentuk dengan membelah satu iaktan peptida. Pembelahan ini menciptakan N-terminus baru yang dikenali oleh E3 spesifik sebagai destabilizing N-terminal residue.
Destabilizing N-terminal residue muncul karena adanya “N-end rule” dimana terdapat kaitan antara identitas residu N-terminal dengan waktu paruh protein. Terdapat 12 destabilizing N-terminal residue pada N-end rule di S. cerevisiae yaitu Arg, Lys, His, Phe, Leu, Tyr, Trp, Ile, Asp, Glu, Asn, dan Gln.

Protein yang Melipat Abnormal Beragregasi dan Menyebabkan Penyakit pada Manusia
Banyak penyakit yang diturunkan seperti sickle cell anemia dan defisiensi α-1-antitripsin disebabkan oleh protein mutan yang lolos dari mekanisme degradasi, melipat secara abnormal, dan membentuk agregat. Dengan mengikat makromolekul penting lainnya, agregat protein ini menyebabkan kerusakan bahkan kematian sel.
Pada individu normal, dengan bertambahnya usia, terjadi penurunan fungsi kontrol kualitas protein. Akibatnya, terdapat peningkatan risiko terjadinya agregasi protein abnormal seiring bertambahnya usia.
Dalam kondisi tertentu, agregat protein ini dilepaskan oleh sel yang mati dan berkumpul di matriks ekstraseluler di sekitar jaringan. Hal ini juga dapat menyebabkan kerusakan jaringan. Otak adalah salah satu organ yang rentan terhadap agregasi protein ini. Beberapa penyakit neurodegeneratif seperti Alzheimer dan penyakit Huntington disebabkan oleh agregat protein abnormal.
Agar agregat protein abnormal dapat menyebabkan kerusakan, maka agregat ini harus tahan terhadap proteolisis baik di dalam maupun di luar sel. Banyak agragat protein yang merusak membentuk fibril yang terbentuk dari serangkaian rantai polipeptida yang membentuk lapisan β-sheet satu sama lain dan dinamai cross-beta filament. Struktur tersebut memiliki sifat tahan terhadap proteolisis dan memiliki sifat khusus dalam pewarnaan. Di dalam observasi mikroskop agregat tersebut dikenal sebagai deposit amiloid.

Satu jenis agregat protein yang mendapat perhatian khusus adalah penyakit prion. Kekhususan dari penyakit prion ini adalah dapat ditularkan dari individu yang sakit ke individu yang sehat. Caranya adalah saat individu yang sehat mengonsumsi bagian dari individu yang sakit. Contohnya adalah scrapie pada domba, Creutzfeldt-Jacob disease (CJD) pada manusia, dan bovine spongiform encephalopathy (BSE) pada sapi.

Penyakit-penyakit tersebut disebabkan oleh agragat protein abnormal yang dinamakan prion protein (PrP). Dalam kondisi normal PrP berada di permukaan membran sel terutama di neuron. Fungsi normal dari protein ini tidak diketahui namun PrP memiliki sifat buruk yaitu dapat berubah ke bentuk konformasi abnormal. Konformasi ini tidak hanya membenuk cross-beta filament yang tahan proteolisis namun juga dapat mengubah protein PrP lain menjadi bentuk abnormal.
Sifat ini membentuk sinyal positif dimana jika terdapat satu PrP abnormal akan menyebabkan protein PrP lain menjadi abnormal (PrP menjadi PrP*). Akibat dari proses ini adalah agregat protein yang semakin banyak dan menyebar dari satu sel ke sel lain di otak. Semakin banyak agregat ini meluas menyebabkan kerusakan dan kematian jaringan dan mengakibatkan munculnya gejala dan kematian pada individu yang sakit.
Sintesis Protein, Kontrol Kualitas Protein, serta Hubungannya dengan Proses Penuaan
Penuaan ditandai dengan penurunan fungsi organ dan akumulasi kerusakan jaringan. Hal ini juga berkaitan dengan kemampuan individu dalam produksi protein serta kontrol kualitas protein di setiap sel. Hal yang mencolok dari proses penuaan adalah menurunnya fungsi penjagaan kualitas pelipatan protein. Seiring bertambahnya usia, kemungkinan kesalahan pelipatan protein semakin besar. Selain itu, kemampuan degradasi protein yang salah ini juga semakin menurun.

Kesimpulan
Sampai tahap ini kita membahas bagaimana susunan reaksi harus dilalui agar informasi dari DNA diartikan oleh sel menjadi protein. Mulai dari transkripsi DNA menjadi RNA dan dilanjutkan translasi sampai proses maturasi protein. Di setiap proses ini pula dapat dilakukan pengaturan sehingga pada akhirnya sel dapat berfungsi dan melakukan adaptasi terhadap perubahan lingkungan demi kelangsungan hidup sel dan kelestarian spesies dari sel tersebut.

Referensi
- Alberts B, Johnson A, Lewis J, Raff M, Roberts K, Walter P. Molecular biology of the cell. 5th ed. New York: Garland Science; 2008. 263–328 p.
- Anisimova AS, Alexandrov AI, Makarova NE, Gladyshev VN, Dmitriev SE. Protein synthesis and quality control in aging. Aging (Albany NY). 2018 Dec 18;10(12):4269–88.
- Arenz S, Wilson DN. Bacterial protein synthesis as a target for antibiotic inhibition. Cold Spring Harb Perspect Med. 2016;6(9):1–14.
- Guo H. Specialized ribosomes and the control of translation. Biochem Soc Trans. 2018;46(4):855–69.
- Karousis ED, Mühlemann O. Nonsense-mediated mRNA decay begins where translation ends. Cold Spring Harb Perspect Biol. 2019;11(2).
- Merrick WC, Pavitt GD. Protein synthesis initiation in eukaryotic cells. Cold Spring Harb Perspect Biol. 2018;10(12).

Seorang dokter, saat ini sedang menjalani pendidikan dokter spesialis penyakit dalam FKUI. Peminat berbagai topik sejarah dan astronomi.


Comments 2
Terimakasih pak, penjelasan nya sangat bagus dan rinci selain itu juga dilengkapi dengan gambar yang menarik dan jelas, saya sangat senang menemukan artikel ini dan juga sangat membantu saya dalam mengerjakan tugas biomol🙏
Terima kasih. Tulisannya sangat membantu.