Pada artikel kali ini kita akan mempelajari bidang kimia organik yang merupakan ilmu dasar bidang kedokteran. Adapun tema kimia organik yang pertama kali kita bahas adalah mengenai karbohidrat. Karbohidrat merupakan senyawa karbon, hidrogen, dan oksigen yang terdapat di alam. Banyak karbohidrat memiliki rumus empiris CH2O seperti glukosa yakni C6H12O6 (enam kali CH2O). Senyawa karbohidrat ini pernah disangka “hidrat dari karbon” sehingga diberi nama atau disebut karbohidrat. Namun, pada tahun 1880-an kemudian disadari bahwa gagasan “hidrat dari karbon” merupakan gagasan yang salah. Karbohidrat sebenarnya adalah polihidroksi aldehida dan keton atau turunannya.
Daftar Isi
Pembagian Karbohidrat: Monosakarida, Oligosakarida, dan Polisakarida
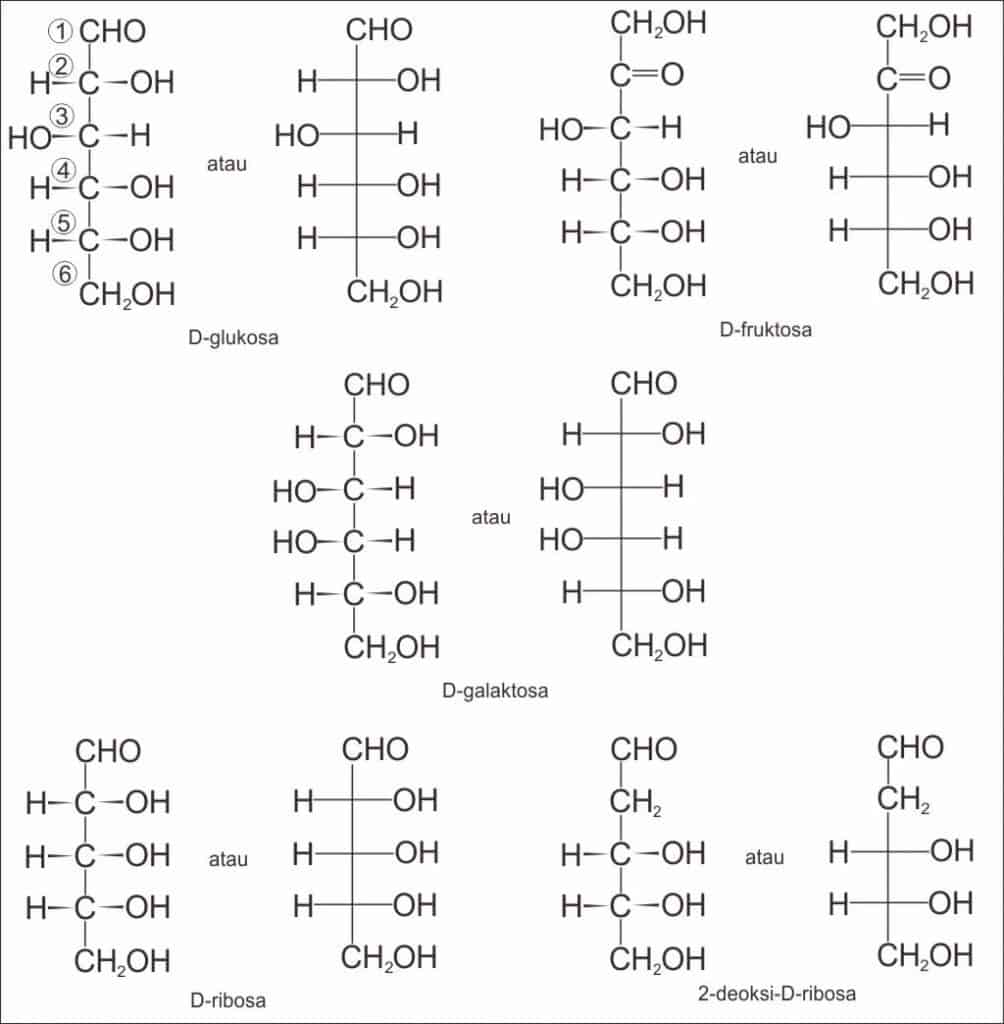
Karbohidrat memiliki sifat yang sangat beraneka ragam. Contohnya adalah sukrosa (gula pasir) dibandingkan dengan kapas. Keduanya adalah karbohidrat namun memiliki sifat yang sangat berbeda. Salah satu perbedaan utama dari berbagai tipe karbohidrat adalah besar molekulnya. Monosakarida (sering disebut pula gula sederhana) adalah satuan karbohidrat yang paling sederhana. Monosakarida ini tidak dapat dihidrolisis menjadi molekul karbohidrat yang lebih kecil lagi. Gambar di bawah ini menunjukan rumus-rumus dimensi dan proyeksi Fischer untuk lima monosakarida yang paling penting.
Monosakarida dapat diikat secara bersama-sama untuk membentuk dimer, trimer, dan sebagainya dan akhirnya polimer. Dimer-dimer disebut disakarida. Sukrosa adalah suatu disakarida yang dapat dihidrolisis menjadi satu satuan glukosa dan satu satuan fruktosa. Monosakarida dan disakarida larut dalam air dan umumnya terasa manis.
\scriptsize{\text{1 sukrosa} \atop \text{\it suatu disakarida}} \xrightarrow[\text{kalor}]{\text{H$_2$O},\text{ H$^+$}} \text{1 glukosa} + \text{1 fruktosa}
Karbohidrat yang tersusun dari dua sampai delapan satuan monosakarida dirujuk sebagai oligosakarida (Yunani, oligo-, = beberapa). Jika lebih dari delapan satuan monosakarida diperoleh dari hidrolisis, maka karbohidrat itu disebut polisakarida. Contoh polisakarida adalah pati yang dijumpai dalam gandum dan tepung jagung serta selulosa, penyusun dari batang serat tanaman dan penyusun utama kapas.
\scriptsize {{\text{pati atau selulosa} \atop \text{\it polisakarida}} \xrightarrow[\text{kalor}]{\text{H$_2$O},\text{ H$^+$}} \text{banyak satuan glukosa}}Beberapa Monosakarida yang Lazim Dijumpai
Glukosa merupakan salah satu monosakarida yang terpenting. Glukosa juga sering kali disebut gula darah (karena dijumpai di dalam darah), gula anggur (karena dijumpai dalam buah anggur), atau dekstrosa (karena memutar bidang polarisasi ke kanan). Hewan mamalia dapat mengubah sukrosa, laktosa (gula susu), maltosa, dan pati menjadi glukosa, yang kemudian dapat digunakan sebagai sumber energi atau disimpan sebagai glikogen (suatu polisakarida). Bila kemudian energi dibutuhkan, glikogen akan diubah kembali menjadi glukosa. Adapun sebagian dari karbohidrat yang berlebih akan diubah menjadi lemak untuk disimpan. Oleh sebab itu, orang bisa menjadi gemuk walaupun mengonsumsi sedikit lemak. Selain menjadi sumber energi, karbohidrat juga merupakan bahan dari steroid (seperti kolesterol) serta secara terbatas dapat diubah menjadi protein (untuk menjadi protein dibutuhkan sumber nitrogen). Adapun sebaliknya, organisme juga dapat mengubah protein dan lemak menjadi karbohidrat.
Fruktosa, disebut juga levulosa karena memutar bidang polarisasi ke kiri, adalah gula yang termanis. Terdapat dalam buah-buahan dan madu, maupun dalam sukrosa. Galaktosa terdapat dalam disakarida laktosa, dalam keadaan terikat dengan glukosa. Ribosa dan deoksiribosa membentuk sebagian kerangka polimer dari asam nukleat (RNA dan DNA). Awalan deoksiribosa berarti “minus atom oksigen”, dimana struktur ribosa dan deoksiribosa adalah sama kecuali deoksiribosa tidak mempunyai atom oksigen di atom karbon posisi kedua.
Klasifikasi Monosakarida
Akhiran -os digunakan dalam tata nama karbohidrat sistematik dalam menyatakan suatu gula pereduksi, yaitu suatu gula yang mengandung gugus aldehida atau suatu gugus α-hidroksiaseton. Banyak oligosakarida dan polisakarida yang bukan gula pereduksi juga memiliki nama trivial yang berakhiran -osa (misalnya sukrosa dan selulosa). Pada bagian ini, baik nama sistematik maupun trivial digunakan terutama ditekankan untuk nama-nama yang lazim digunakan.
Monosakarida yang mengandung gugus aldehida dirujuk sebagai aldosa (aldehida plus -osa). Glukosa, galaktosa, ribosa, dan deoksiribosa semuanya adalah aldosa. Monosakarida seperti fruktosa, memiliki gugus keton dan disebut ketosa (keton plus -osa).
Banyaknya atom karbon dalam suatu monosakarida (biasanya tiga sampai tujuh) dapat dinyatakan dengan tri-, tetr-, dan seterusnya. Misalnya, suatu triosa adalah monosakarida tiga karbon sedangkan suatu heksosa adalah monosakarida enam karbon. Glukosa merupakan golongan heksosa. Istilah-istilah ini dapat digabung sehingga glukosa yang juga merupakan aldosa dapat disebut monosakarida aldoheksosa (aldosa dengan enam karbon). Adapun ribosa adalah suatu aldopentosa (aldosa lima karbon). Ketosa sering diberi nama dengan akhiran -ulosa. Fruktosa merupakan contoh dari suatu heksulosa (ketosa enam karbon).
Konfigurasi Monosakarida
Seperti pada Gambar 1, struktur monosakarida mirip satu dengan lainnya. Beberapa memiliki struktur yang berbeda seperti glukosa yang merupakan suatu aldehida dengan fruktosa yang merupakan suatu keton. Monosakarida yang lain ternyata adalah diastereomer (stereoisomer yang tidak enantiomerik) satu sama lainnya. Contohnya adalah glukosa dan galaktosa adalah epimer satu terhadap yang lainnya. Epimer adalah diastereomer yang konfigurasinya berbeda hanya pada satu dari atom-atom karbon kiralnya.
a. Sistem D dan L
Di akhir abad ke-19, ditetapkan bahwa konfigurasi atom kiral yang terakhir di setiap monosakarida yang terdapat di alam, sama dengan konfigurasi (+)-gliseraldehida. Sekarang, konfigurasi tersebut dinamakan konfigurasi-(R). Pada saat itu, ahli kimia belum dapat menentukan konfigurasi mutlak di sekitar suatu atom karbon kiral dari monosakarida. Sebagai gantinya, para ahli mereka-reka sistem D dan L untuk menandai konfigurasi relatif. Sistem D dan L ini berbeda dengan d dan l yang digunakan untuk merujuk arah pemutaran bidang polarisasi cahaya oleh suatu larutan zat kimia.
Pada sistem D dan L, (+)-gliseraldehida dapat secara sebarang diberi konfigurasi dengan OH-nya pada karbon 2 berada di sebelah kanan dalam proyeksi Fischer (suatu pengandaian yang kelak terbukti benar). Suatu monosakarida merupakan anggota deret-D jika gugus hidroksil pada karon kiral yang terjauh dari karbon 1 juga terletak di sebelah kanan dalam proyeksi Fischer. Hampir semua karbohidrat alami merupakan anggota deret-D. Disamping itu, setiap monosakarida diber nama sendiri. Misalnya dua aldopentosa diastereomerik berikut ini diberi nama D-liksosa dan D-ribosa (lyxose; ribose). Adapun perbandingan struktur molekul keduanya dapat dilihat di Gambar 5 di bawah ini:
Jika OH pada karbon kiral terakhir diproyeksikan ke kiri, maka senyawa itu merupakan anggota deret-L. Dua contoh berikut ini adalah enantiomer D-liksosa dan D-ribosa:
b. Konfigurasi yang Berhubungan
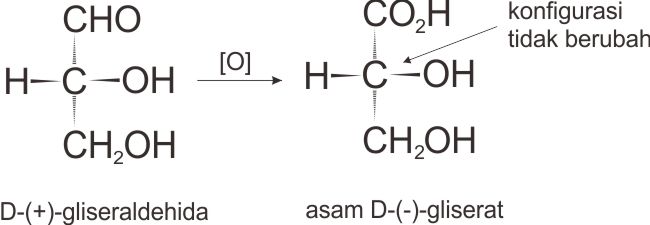
Telah disebutkan sebelumnya bahwa dahulu para ahli belum bisa menentukan konfigurasi mutlak dari karbon-karbon kiral. Sebagai gantinya ditetapkan konfigurasi yang realtif terhadap konfigurasi (+)-gliseraldehida. Bagaimana senyawa-senyawa lain dihubungkan dengan gliseraldehida? Berikut ini adalah contoh penetapan suatu konfigurasi relatif. Jika gugus aldehida dari D-gliseraldehida dioksidasi menjadi suatu asam karboksilat, maka produknya, asam gliserat, haruslah sama konfigurasinya di sekitar atom karbon kiral dari konfigurasi dalam D-gliseraldehida. Produk itu, meskipun memutar ke kiri, masih merupakan anggota deret-D.
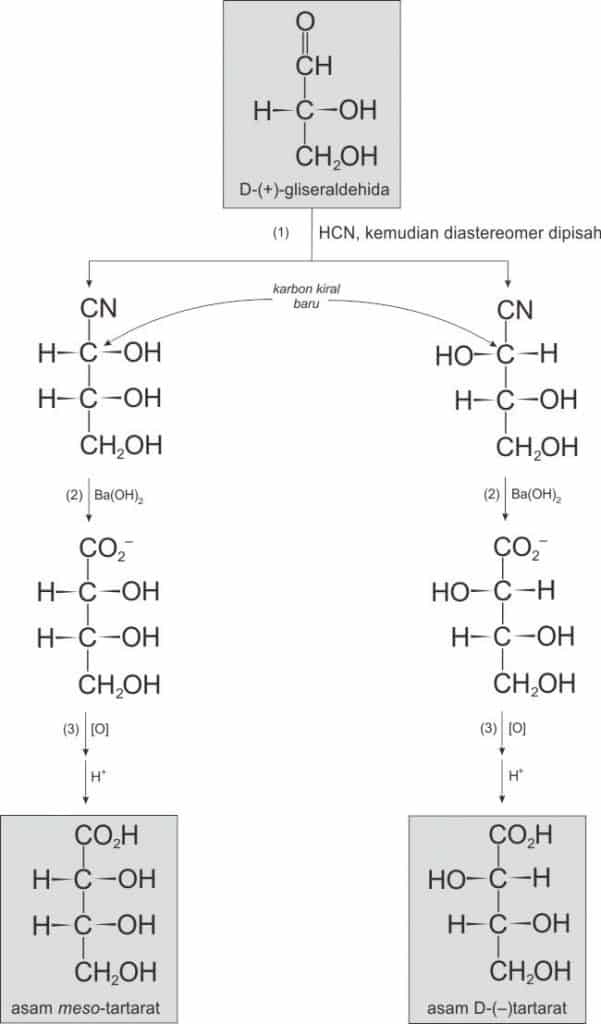
Konfigurasi asam-asam tartarat relatif terhadap D-gliseraldehida ditetapkan pada tahun 1917 dengan rentetan yang ditunjukan di Gambar 8. Dari gambar tersebut tampak dihasilkan dua dari tiga isomer asam tartarat. Dalam tahap pertama dari rentetan tersebut, D-gliseraldehida diolah dengan HCN menghasilkan suatu campuran sianohidrin. Letak kiralitas baru dibentuk dalam tahap ini dan terbentuklah dua diastereomer. Diastereomer ini dipisahkan kemudian di tahap kedua tiap diastereomerik itu dihidrolisis.
Dalam tahap ketiga, gugus CH2OH di ujung dioksidasi untuk menghasilkan dua asam tartarat. Karbon ke-3 dari masing-masing asam tartarat itu mempunyai konfigurasi yang sama dengan karbon 2 dari D-gliseraldehida karena rangkaian tersebut tidak mempengaruhi konfigurasi sekitar karbon itu. Tetapi konfigurasi sekitar karbon 2 dalam asam tartarat berbeda. Salah satu asam tartarat yang diperoleh dari sintesis ini tidak memutar bidang polarisasi cahaya. Ini adalah isomer meso, yakni isomer dengan suatu bidang simetri dalam. Asam tartarat yang lain yang diperoleh dari sintetsis itu memutar bidang polarisasi cahaya ke kiri; asam ini pasti memiliki struktur kedua sebagai berikut:
c. Konfigurasi Aldoheksosa
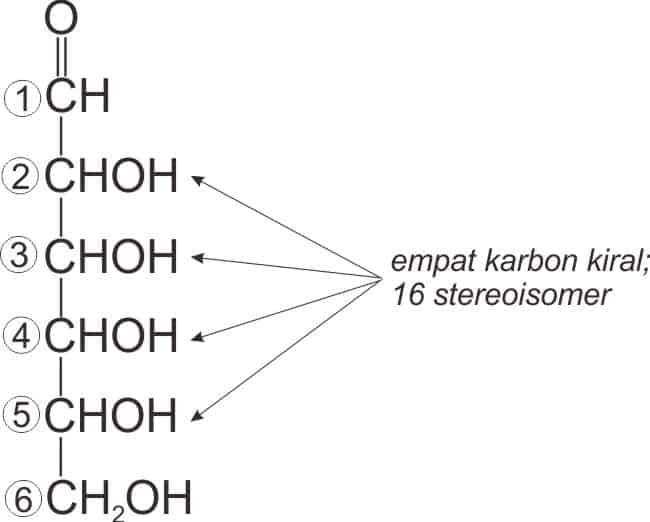
Glukosa mempunyai enam atom karbon, empat diantaranya bersifat kiral (karbon 2, 3, 4, dan 5) seperti tampak pada Gambar 10 di bawah. Karena atom karbon ujung dari glukosa memiliki fungsionalitas yang berlainan, maka tidak dapat diperoleh bidang simetri dalam. Oleh karena itu, senyawa ini memiliki 24 atau 16 stereoisomer. Hanya separuh dari enam belas stereoisomer tersebut termasuk ke dalam deret-D dan dijumpai di alam. Dari delapan ini, hanya D-glukosa, D-galaktosa, dan D-manosa yang dijumpai dalam jumlah melimpah.
Proyeksi Fischer dari semua semua D-aldosa ini, dari D-glsieraldehida sampai dengan D-aldoheksosa, dipaparkan pada Gambar 11 di bawah. Mulai dari triosa, yaitu D-gliseraldehidam ke tetrosa, satu karbon ditambahkan ke “puncak” molekul dalam proyeksi Fischer. Penambahan satu karbon lagi menciptakan satu karbon kiral yang baru. Oleh sebab itu, D-gliseraldehida menghasilkan sepasang tetrosa lalu tiap tetrosa menghasilkan sepasang pentosa, dan tiap pentosa akan menghasilkan sepasang heksosa.
Siklisasi Monosakarida
Glukosa mempunyai suatu gugus aldehida pada karbon 1 dan gugus hidroksil pada karbon 4 dan 5 (seperti juga pada karbon 2, 3, dan 6). Suatu reaksi umum antara alkohol dan aldehida adalah pembentukan hemiasetal. Reaksi pembentukan hemiasetal ini dapat dilihat di bagan persamaan di bawah ini:
Dalam larutan air, glukosa dapat bereaksi intramolekul untuk menghasilkan hemiasetal siklik. Baik hemiasetal cincin lima anggota (digunakan gugus hidroksil pada karbon 4) atau hemiasetal cincin enam-anggota (digunakan gugus hidroksil pada karbon 5) dapat terbentuk (perhatikan gambar di bawah).
Meskipun proyeksi Fischer berguna dalam pembahasan karbohidrat rantai terbuka tetapi untuk senyawa siklik proyeksi ini janggal. Untuk itu rumus glukosa ini ditulis ulang untuk menunjukan rumus yang lebih penting dari reaksi siklisasi yakni reaksi yang menghasilkan cincin enam anggota.
Dalam proyeksi Fischer untuk hemiasetal siklik, perhatikan bahwa karbon 1 (karbon aldehida), yang tidak bersifat kiral dalam struktur rantai terbuka menjadi kiral dalam siklisasi. Oleh karena itu, dihasilkan sepasang diastereomer dari siklisasi tersebut. Karena semua struktur hemiasetal berada dalam kesetimbangan dengan aldehida dalam larutan air, maka mereka juga berada dalam kesetimbangan satu dengan yang lainnya.
\scriptsize {\text{hemiasetal siklik 5 anggota} \atop \text{\it dua diastereomer}} \leftrightarrows {\text{glukosa} \atop \text{\it rantai terbuka}} \leftrightarrows {\text{hemiasetal siklik 6 anggota} \atop \text{\it dua diastereomer}}a. Cincin Furanosa dan Piranosa
Suatu karbohidrat sederhana atau monosakarida dalam bentuk hemiasetal cincin lima anggota disebut furanosa, Furan- diambil dari kata furan, senyawa heterosikel oksigen lima anggota. Serupa pula dengan piranosa yaitu monosakarida dalam bentuk cincin enam anggota, diambil dari kata piran. Istilah puranosa dan piranosa seringkali digabung dengan nama monosakaridanya, misalnya D-glukopiranosa untuk cincin enam anggota dari D-glukosa atau D-fruktofuranosa untuk cincin lima anggota dari fruktosa.
Dari dua sistem cincin untuk glukosa, yang disukai adalah hemiasetal siklik enam anggota atau glukopiranosa. Untuk ukuran cincin ini akan ditekankan dalam pembahasan nanti. Sebagian sebab mengapa glukosa memilih membentuk cincin enam anggota dalam larutan adalah karena sudut-sudut ikatan dan dapat bergoyangnya gugus-gugus yang terlekat. Meskipun cincin piranosa dari suatu monisakarida mungkin melimpah dalam suatu kesetimbangan dalam air, namun mungkin cincin furanosalah yang dipersatukan ke dalam hasil alam secara enzimatik. misalnya, dalam suatu asam ribunukleat, ribosa dijumpai sebagai suatu furanosa dan bukan sebagai piranosa.
b. Rumus Haworth dan Rumus Konformasi Karbohidrat
Untuk memaparkan struktur siklik karbohidrat sederhana dengan lebih baik, dikembangkan rumus perspektif Haworth. Menurut perjanjian, suatu rumus Haworth digambarkan dengan oksigen berada di sisi terjauh dari cincin dan karbon 1 berada di sebelah kanan. Gugus CH2OH ujung ditempatkan di atas bidang cincin untuk deret-D dan di bawah cincin untuk deret-L. Atom-atom hidrogen pada karbon cincin biasanya tidak ditampakan dalam proyeksi Haworth.
Dengan menggunakan rumus Fischer maupun Haworth dapatlah kita tulis ulang persamaan-persamaan yang menunjukan siklisasi glukosa. Perhatikan bahwa gugus apa saja yang berada di sebelah kanan dalam proteksi Fischer berada di sebelah bawah dalam proyeksi Haworth dan gugus apa saja yang berada di sebelah kiri dalam proyeksi Fischer berada di sebelah atas dalam rumus Haworth.
Rumus Haworth yang datar bukan merupakan pemaparan yang seluruhnya tepat dari cincin piranosa (meskipun cukup tepat untuk cincin furanosa yang lebih datar). Suatu piranosa, seperti sikloheksana, terutama berada dalam bentuk kursi, seperti ditunjukan oleh rumus konformasi di bawah ini.
Jika suatu OH berada di sebelah bawah dalam suatu rumus Haworth, maka gugus ini juga berada di sebelah bawah (di bawah bidang cincin) dalam rumus konformasi. Serupa pula jika suatu OH berada di sebelah atas dalam rumus Haworth, maka OH tersebut juga berada di sebelah atas dalam rumus konformasi. Sebagaimana untuk setiap cincin enam anggota tersubstitusi, cincin mengambil konformasi dalam mana sebagian besar gugusnya bersikap ekuatorial.
c. Anomer
Untuk menghasilkan suatu piranosa, gugus hidroksil pada karbon 5 dari glukosa menyerang karbon aldehida, yaitu karbon 1. Hasilnya adalah terbentuknya gugus hemiasetal. Kemudian akibat terpenting setelahnya adalah terbentuk suatu karbon kiral baru (karbon 1) sehingga bisa dihasilkan sepasang diastereomer. Diastereomer ini yaitu monosakarida yang berbeda hanya pada konfigurasi pada karbon 1 disebut anomer satu terhadap lainnya. Karbon karbonil dalam monosakarida apa saja adalah karbon anomerik. Karbon ini ialah karbon yang menjadi kiral dalam reaksi siklisasi.
Dalam rumus Haworth untuk suatu D-gula, struktur dalam mana OH anomerik diproyeksikan ke bawah (trans terhadap CH2OH ujung) disebut α-anomer, sedangkan struktur dalam mana OH anomerik diproyeksikan ke atas (cis terhadap CH2OH ujung) disebut β-anomer.
Jadi, kedua D-glukosa anomerik dapat disebut α-D-glukopiranosa (atau cukup α-D-glukosa) dan β-D-glukopiranosa (atau β-D-glukosa).
d. Mutarotasi
Glukosa murni berada dalam dua bentuk kristalin: α-D-glukosa dan β-D-glukosa. α-D-glukosa murni memiliki titik leleh 146℃. Rotasi jenis larutan yang baru saja dibuat adalah +112º. β-D-glukosa murni mempunyai titik leleh 150℃ dan rotasi +18,7º. Sudut putar spesifik larutan baik rotasi jenis larutan α- maupun β-D-glukosa berubah perlahan-lahan sampai mencapai nilai kesetimbangan sebesar +52,6º. Perubahan serta-merta yang lambat dari rotasi optis ini pertama kali dijumpai tahun 1846 dan disebut mutarotasi.
Mutarotasi terjadi karena (dalam larutan) baik α-maupun β-D-glukosa mengalami suatu proses penyetimbangan lambat dengan bentuk rantai terbuka dan dengan anomer lainnya. Tak perduli anomer mana yang dilarutkan, hasilnya ialah suatu campuran kesetimbangan yang terdiri dari 64% β-D-glukosa, 36% α-D-glukosa, dan 0,02% bentuk aldehida dari D-glukosa. Rotasi jenis akhir adalah rotasi jenis dari campuran kesetimbangan.
Perhatikan bahwa campuran kesetimbangan dari anomer-anomer D-glukosa mengandung lebih banyak β-anomer dari pada α-anomer. Sebabnya adalah lebih stabilnya β-anomer dari pada α-anomer. Dari analisis konformasi, gugus hidroksil pada karbon 1 bersikap ekuatorial dalam β-anomer tetapi aksial dalam α-anomer. Kita ketahui bahwa posisi ekuatorial lebih stabil sehingga lebih disukai.
Monosakarida lain juga menunjukan mutarotasi. Dalam larutan air, aldosa-aldosa lain (jika memiliki gugus 5-hidroksil) juga berada terutama bentuk piranosa. Namun presentase berbagai spesimen yang terlibat dalam kesetimbangan dapat beraneka ragam. Misalnya, campuran kesetimbangan D-ribosa dalam air terdiri dari 56% β-piranosa, 20% α-piranosa, 18% β-furanosa, dan 16% α-furanosa (plus kelumit bentuk aldehida rantai terbuka).
Meskipun β-anomer cincin-cincin piranosa umumnya merupakan anomer yang lebih stabil, tetapi tidak selalu demikian. Misalnya, α-D-manosa lebih stabil dari pada β-anomernya dan melimpah dalam suatu campuran kesetimbangan. Anomali seperti ini disebut efek anomerik dan diakibatkan oleh interaksi antara substituen-subtituen polar pada cincin.
Karena mudahnya perubahan dalam air antara gugus OH hemiasetal α dan β, sering kali tidak mungkin untuk menentukan konfigurasi pada karbon ini. Karena itu, kadang-kadang ikatan OH hemiasetal dinyatakan dengan garis berombak yang berarti struktur itu α dan β atau suatu campuran.

Glikosida
Bila suatu hemiasetal diolah dengan suatu alkohol, akan terbentuk suatu asetal. Asetal monosakarida disebut glikosida dan memperoleh nama yang berakhir dengan -osida.
Karbon glikosida (karbon 1 dalam aldosa) mudah dikenali karena mempunyai dua gugus OR yang terikat pada karbon 1 itu.
Meskipun suatu hemiasetal dari suatu monisakarida berada dalam kesetimbangan dengan bentuk rantai terbuka dan denan anomernya dalam air, suatu asetal bersifat stabil dalam larutan netral atau basa. Oleh karena itu suatu glikosida tidak membentuk kesetimbangan dengan aldehidanya atau anomernya dalam larutan air. Namun glikosida dapat dihidrolisis menjadi bentuk-bentuk hemiasetal (dan aldehida) bila diolah dengan asam berair. Reaksi ini sekedar kebalikan pembentukan glikosida.
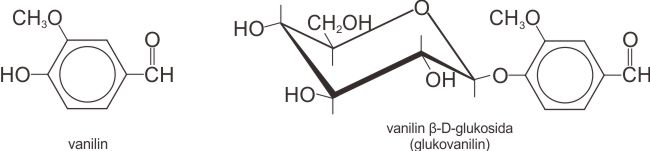
Disakarida dan polisakarida adalah glikosida. Tipe lain dari glukosida biasa dijumpai dalam tumbuhan dan hewan. Amygdalin dan laetrile merupakan glikosida yang dijumpai dalam biji buah aprikot dan almond pahit. Vanilin (esens vanila) adalah suatu contoh lain dari glikosida alamiah, dalam hal ini sebagai β-D-glukosida. Dalam tipe glikosida ini, bagian bukan gulanya disebut aglikon (aglycone). Dalam contoh di bawah ini, vanilin adalah sebuah aglikon.
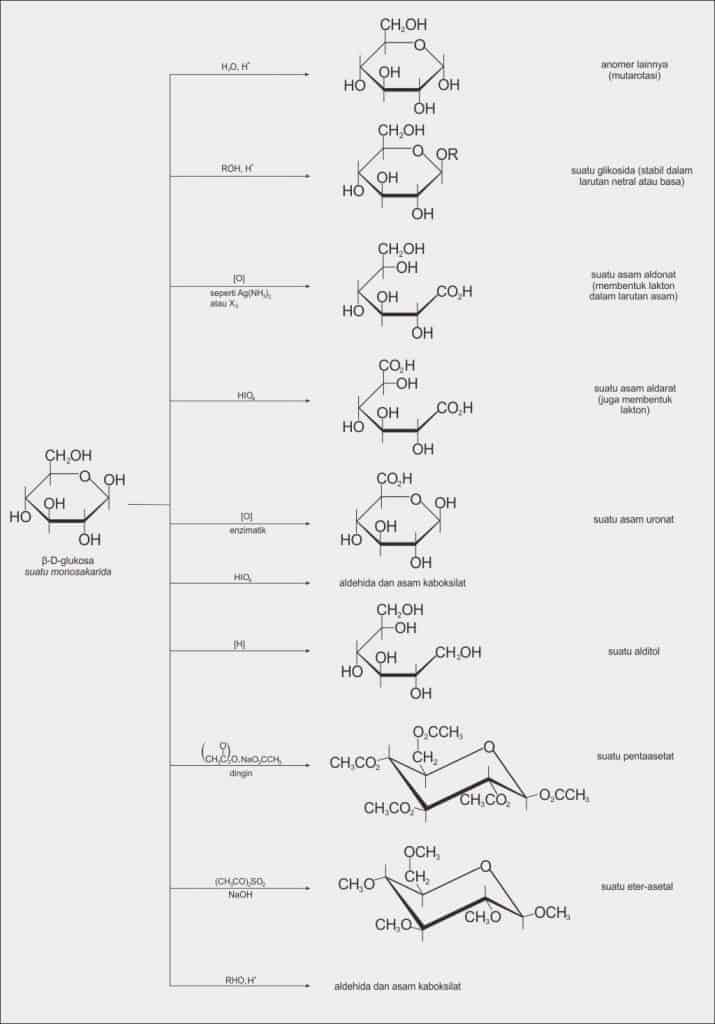
Oksidasi Monosakarida
Suatu gugus aldehida sangat mudah dioksidasi menjadi suatu gugus karboksil. Uji kimiawi suatu aldehida tergantung pada mudahnya oksidasi ini. Gula yang dapat dioksidasi oleh zat pengoksidasi lembut seperti reagensia Tollens, suatu larutan basa dari Ag(NH3)2+, disebut gula pereduksi (karena zat pengoksidasi anorganik direduksi dalam reaksi tersebut). Bentuk-bentuk hemiasetal siklik dari semua aldosa mudah dioksidasi karena mereka berada dalam kesetimbangan dengan bentuk aldehida rantai terbukanya.
Meskipun berupa suatu keton, fruktosa juga merupakan gula pereduksi.
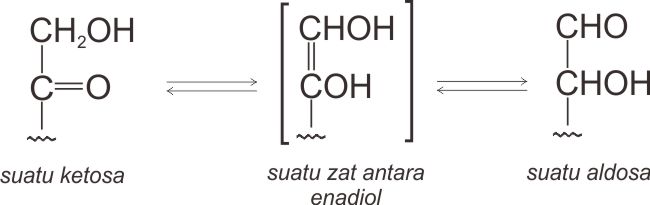
Alasan mengapa fruktosa begitu mudah teroksidasi adalah karena dalam larutan basa, fruktosa berada dalam kesetimbangan dengan dua aldehida diastereomerik serta penggunaan suatu zat antara tautomerik enadiol.
Glikosida bukan merupakan gula pereduksi. Hal ini dikarenakan dalam glikosida, gugus karbonil terblokade sehingga tidak terjadi reaksi.
a. Asam Aldonat
Produk oksidasi dari gugus aldehida suatu aldosa adalah suatu asam polihidroksi karboksilat, yang disebut asam aldonat (aldonic acid). Meskipun reagensia Tollens dapat mengakibatkan perubahan ini, reagensia lain yang lebih mudah dan murah untuk reaksi sintetik asam aldonat ini adalah dengan menggunakan larutan bufer brom (disangga).
Dalam larutan basa, asam aldonat berada sebagai ion karboksilat rantai terbuka. Dengan pengasaman, asam aldonat akan cepat berubah menjadi lakton (ester siklik), tepat seperti asam γ- atau δ-hidroksi. Kebanyakan asam aldonat memiliki gugus hidroksil γ maupun δ dan dapat terbentuk cincin lima anggota maupun enam anggota. Cincin lima anggota (γ-lakton) lebih disukai/stabil.
b. Asam Aldarat
Zat pengoksidasi kuat mengoksidasi gugus aldehida dan juga gugus hidroksil ujung (suatu alkohol primer) dari monosakarida. Produknya adalah asam polihidroksi dikarboksilat yang disebut asam aldarat (aldaric acid). Asam aldarat dapat pula dengan mudah membentuk lakton.
Asam aldarat ini memainkan peranan penting dalam penetapan struktur gula atau karbohidrat.
c. Asam Uronat
Meskipun tidak mudah dilakukan di laboratorium, dalam sintesis biologis gugus CH2OH ujung dapat dioksidasi dengan enzim tanpa teroksidasinya gugus aldehida. Produknya disebut asam uronat (uronic acid).
Asam glukuronat penting dalam sel hewan karena banyak zat toksik yang dibuang lewat air seni berupa bentuk glukuronida, derivat dari asam glukuronat. Pada sel hewan dan tumbuhan juga, asam D-glukuronat dapat diubah menjadi asam L-glukonat yang digunakan untuk biosintesis asam L-askorbat (vitamin C). Konversi terakhir ini tidak terjadi pada tubuh hewan primata termasuk manusia, kera, dan babi guinea (guinea pig). Oleh sebab itu, hewan-hewan ini memerlukan asupan vitamin C dari luar (makanan). Fakta bahwa suatu senyawa deret-D menjadi suatu senyawa deret-L tidak disebabkan oleh perubahan biokimia pada konfigurasinya melainkan lebih disebabkan oleh berubahnya cara penomoran karbon, tampak dalam persamaan berikut ini:
d. Oksidasi Asam Periodat
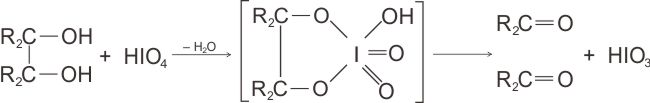
Oksidasi asam periodat merupakan uji untuk 1,2-diol dan untuk 1,2- atau α-hidroksi dari aldehida maupun keton. Suatu senyawa yang mengandung gugusan semacam itu dioksidasi dan dipaksa pisah oleh asam periodat (HIO4). Dalam hal 1,2-diol sederhana, produknya adalah dua aldehida atau keton.
Reaksi asam periodat berlangsung lewat suatu zat antara siklik, suatu fakta yang menjelaskan mengapa gugus hidroksil yang terisolasi tidak mengalami oksidasi.
Dalam hal α-hidroksi aldehida atau keton, gugus karbonil dioksidasi menjadi gugus karboksil, sedangkan gugus hidroksil dioksidasi lagi menjadi suatu aldehida atau keton.

Oksidasi asam periodat digunakan dalam analisis karbohidrat. Dalam karbohidrat, oksidasi gugus hidroksil-dalam berlangsung lebih lanjut dibandingkan oksidasi dengan 1,2-diol sederhana. Misalnya, produk oksidasi asam periodat dari eritrosa adalah formaldehida dan asam format dengan perbandingan molar 1 : 3.
Osidasi gugus-gugus CHOC dalam eritrosa menjadi asam format ini dapat dinalarkan dengan memperhatikan reaksi tersebut secara bertahap.
Reduksi Monosakarida
Baik aldosa maupun ketosa dapat direduksi oleh zat pereduksi karbonil, seperti hidrogen dan katalis atau suatu hidrida logam, menjadi polialkohol yang disebut alditol. Akhiran untuk nama dari salah satu polialkohol ini ialah -itol. Produk reduksi D-glukosa disebut D-glukositol (D-glucitol) atau sorbitol.
D-glusitol alamiah telah diisolasi dari banyak buah (misalnya buah ceri, prem, apel, peer, dan beri), lumut, serta rumput laut. D-glusitol sintetik digunakan sebagai pemanis sintetik.
Reaksi pada Gugus Hidroksil dari Karbohidrat
Gugus-gugus hidroksil dalam karbohidrat bertabiat serupa dengan dalam gugus-gugus alkohol lain. Gugus ini dapat diesterifikasi oleh asam karboksilat atau oleh suatu asam anorganik dan dapat digunakan untuk membentuk eter. Karbohidrat dapat juga bertindak sebagai diol dan membentuk asetal atau ketal siklik dengan aldehida atau keton.
a. Pembentukan Asetat
Suatu reagensia yang lazim digunakan untuk esterifikasi alkohol adalah anhidrida asam asetat, dengan antrium asetat atau piridina sebagai suatu katalis basa. Jika reaksi itu dilakukan di bawah 0℃, reaksi asilasi akan lebih cepat dari pada antar-pengubahan anomerik α-β. Pada kondisi ini baik α- atau pun β-D-glukosa menghasilkan pentaasetat padanannya. Pada temperatur yang lebih tinggi diperoleh suatu campuran α- dan β-pentaasetat, dengan Suatu reagensia yang lazim digunakan untuk esterifikasi alkohol adalah anhidrida asam asetat, dengan antrium asetat atau piridina sebagai suatu katalis basa. Jika reaksi itu dilakukan di bawah 0℃, reaksi asilasi akan lebih cepat dari pada antar-pengubahan anomerik α-β. Pada kondisi ini baik α- atau pun β-D-glukosa menghasilkan pentaasetat padanannya. Pada temperatur yang lebih tinggi diperoleh suatu campuran α- dan β-pentaasetat, dengan β-pentaasetat yang lebih melimpah.
b. Pembentukan Eter
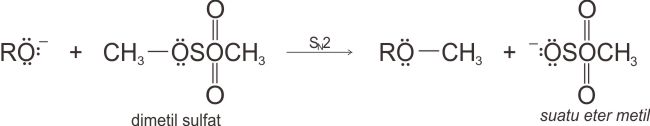
Dimetil sulfat adalah suatu ester anorganik dengan gugus pergi yang sangat baik. Senyawa ini digunakan untuk membentuk eter metil.
Bila suatu monosakarida diolah dengan dimetil sulfat yang berlebih dan NaOH, semua gugus hidroksil (termasuk gugus OH hemoasetal dan hemiketal) diubah menjadi gugus metoksil.
Dalam suatu sintesis eter Williamson yang lazim (RO– + RX → ROR + X–), alkoksida itu harus dibuat dengan suatu basa yang lebih kuat dari pada NaOH. Dalam hal karbohidrat, NaOH merupakan basa yang cukup kuat untuk menghasilkan ion alkoksida. Efek induktif dari oksigen-oksigen yang elektronegatif pada karbon-karbon yang berdekatan membuat tiap gugus hidroksil lebih asam dari pada suatu gugus hidroksil dalam suatu alkohol biasa. Karena ikatan asetal stabil dalam basa, konfigurasi pada karbon anomerik dari suatu glikosida tidak berubah dalam reaksi metilasi ini.
c. Pembentukan Asetal dan Ketal Siklik
Karena karbohidrat mengandung banyak gugus OH, kadang-kadang diinginkan untuk memblokade beberapa diantaranya sehingga dapat dilaksanakan reaksi selektif pada gugus-gugus hidroksil yang lain. Asetal dan ketal merupakan dua gugus blokade yang lazim. Misalnya, suatu aldehida, seperti benzaldehida, bereaksi dengan gugus 1,3-dial dalam molekul gula. Aldehida dan keton lain dapat bereaksi secara pilih-pilij oada gugus diol yang berlainan. Dalam beberapa hal, produknya adalah cincin furanosa, bukannya piranosa. Produk-produk yang berbeda-beda timbul karena adanya efek elektronik dan sterik yang hampir tidak bisa dibedakan (dan umumnya tidak dapat teramalkan).
Dalam pengubahan L-sorbosa secara komersial menjadi vitamin C, digunakan aseton untuk memblokade empat gugus hidroksi sehingga dapat dioksidasi hanya satu gugus CH2OH. Konversi ini diringkas pada Gambar 48.
Ringkasan Reaksi-reaksi Penting dari Monosakarida atau Karbohidrat Sederhana
Berikut ini adalah bagan ringkasan mengenai reaksi-reaksi yang penting dari monosakarida:
Penentuan Struktur Glukosa
Pada tahun 1888, diketahui bahwa glukosa adalah suatu aldoheksosa. Pertanyaannya adalah ada 16 aldoheksosa stereoisomerik yang mungkin, stereoisomer mana yang glukosa? Kemudian tahun 1891, seorang ahli kimia Jerman, Emil Fischer melaporkan struktur dari aldehida berbentuk rantai terbuka dari D-glukosa. Atas karya ini ia memperoleh hadiah Nobel Kimia tahun 1902.

Asumsi Fischer
Penentuan konfigurasi suatu senyawa dengan empat karbon kiral kelihatannya suatu pekerjaan yang luar biasa beratnya. Tetapi Fischer berhasil menyelesaikan persoalan ini dengan serangkaian reaksi sederhana. Menurut datanya, hanya mungkin ditetapkan konfigurasi relatif glukosa, bukan konfigurasi mutlaknya, yang akhirnya ditentukan dengan menggunakan difraksi sinar X 50 tahun kemudian. Oleh karena itu, Fischer membuat pengandaian (asumsi) bahwa OH pada karbon 2 dalam D-(+)-gliseraldehida dan dengan demikian OH pada karbon 5 dalam D-(+)-glukosa diproyeksikan ke kanan dalam proyeksi Fischer. Di kemudian hari ternyata bahwa pengandaian ini terbukti benar. Pengandaian tersebut menyusutkan pilihan untuk konfigurasi glukosa menjadi delapan D-aldoheksosa seperti ditunjukan pada Gambar 11 di atas.
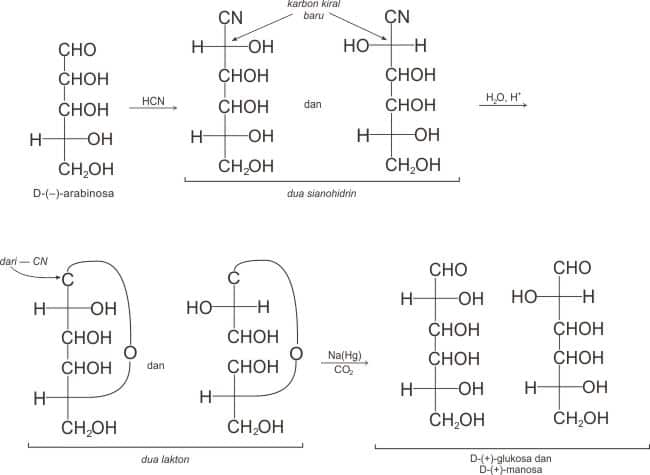
Sintesis Kiliani-Fischer
Fakta I: Diketahui bahwa aldopentosa (–)-arabinosa dapat diubah menjadi aldoheksosa (+)-glukosa dan (+)-manosa. Heinrich Kiliani menemukan tahap pemanjangan rantai pada tahun 1886, dan pada tahun 1890 Fischer melengkapi sintesisnya dengan mereduksi lakton yang dihasilkan untuk memperoleh aldoheksosa-aldoheksosa. Rentetan reaksi berikut dikenal sebagai sintesis Kiliani-Fischer. Di sini ditunjukan lakton zat-antara itu sebagai proyeksi Fischer agar persamaan-persamaan ini taat asas.
Karena (–)-arabinosa menghasilkan (+)-glukosa dan (+)-manosa, maka ketiga gula ini memiliki konfigurasi yang sama pada ketiga karbon kiral terakhir. Baik (+)-glukosa maupun (+)-manosa pasti berbeda hanya dari konfigurasi pada karbon 2. Kesimpulan-kesimpulan ini dipaparkan pada Gambar 53 di bawah.

Sifat Optis Aktif Asam Aldarat Hasil Oksidasi (–)-Arabinosa
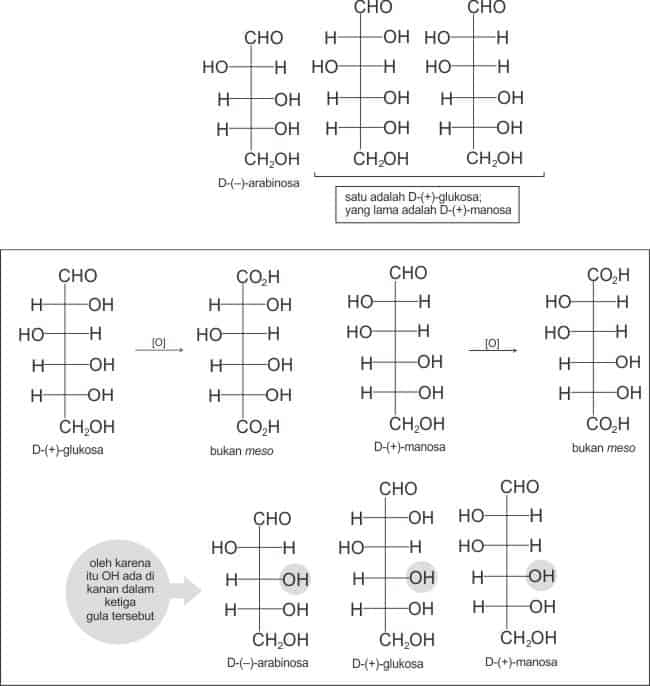
Fakta 2: Fischer menjumpai bahwa oksidasidari kedua gugus ujung dari (–)-arabinosa menghasilkan suatu dwiasam yang aktif optis dan bukan dwiasam-meso.
Oleh karena itu Fischer menyimpulkan bahwa karbon 2 dalam (–)-arabinosa pasti memiliki OH di kiri dari proyeksi Fischer. Seandainya di kanan, akan diperoleh dwiasam meso.

Dari data yang kita dapatkan sejauh ini, kita bisa menulis struktur yang hampir lengkap untuk (–)-arabinosa, (+)-glukosa, dan (+)-manosa. Struktur yang kita dapatkan sementara ini adalah sebagai berikut:

Hasil Oksidasi (+)-Glukosa Maupun (+)-Manosa Bersifat Optis Aktif
Fakta 3: Fischer menjumpai bahwa baik (+)-glukosa maupun (+)-manosa dioksidasi menjadi dwiasam aktif optis. Ini berarti bahwa OH pada karbon 4 dari kedua monosakarida ada di kanan. Seandainya berada di kiri, salah satu dari kedua gula ini akan menghasilkan suatu dwiasam-meso. Gambar berikut menunjukan reaksi ini dengan struktur-struktur yang diketahui:
Sekarang dapatlah ditulis suatu struktur lengkap untuk (–)-arabinosa dimana yang diperlukan sekarang adalah hanyalah membedakan antara (+)-glukosa dan (+)-manosa.
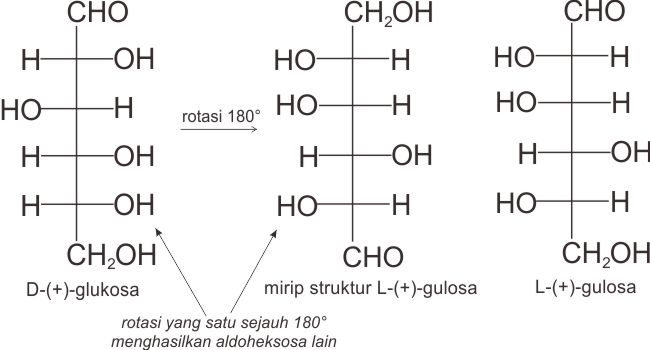
Fakta 4: Gula (+)-gulosa (aldoheksosa lain) dan (+)-glukosa keduanya menghasilkan dwiasam yang sama bila dioksidasi. Diantara dwiasam-dwiasam yang mungkin, yang dapat diperoleh dari kedua struktur yang merupakan (+)-glukosa dan (+)-manosa, hanya satu yang dapat berasal dari dua gula yang berlainan.

Pertama-tama akan diperiksa dwiasam II lebih dahulu. Kedua aldoheksosa yang potensial dapat menghasilkan dwiasam II adalah sebagai berikut:

Tetapi kedua aldoheksosa itu sama. Hal itu jelas terlihat dengan rotasi pada bidang kertas sejauh 180°. Hanya satu aldoheksosa ini yang dapat menghasilkan dwiasam II. Aldoheksosa ini pastilah (+)-manosa.
Sekarang periksa dwiasam I. Dwiasam ini dapat dihasilkan dari dua aldoheksosa yang mungkin, yang tidak sama: D-glukosa danL-gulosa.
Jika kedua gula ini menghasilkan dwiasam yang sama (dwiasam I), maka struktur kiri adalah (+)-glukosa, struktur kanan adalah (+)-gulosa, dan aldoheksosa yang menghasilkan dwiasam II adalah (+)-manosa. Perhatikan gambar di bawah ini.

Penentuan Ukuran Cincin Glukosa
Struktur-struktur siklik untuk glukosa dipostulatkan pada tahun 1895, tetapi tidak pernah dibuktikan sampai tahun 1926 bahwa glukosa membentuk hemaisetal siklik enam-anggota dan glikosida. Sekali lagi, reaksi yang digunakan untuk menetapkan ukuran cincin ini tidaklah kompleks.
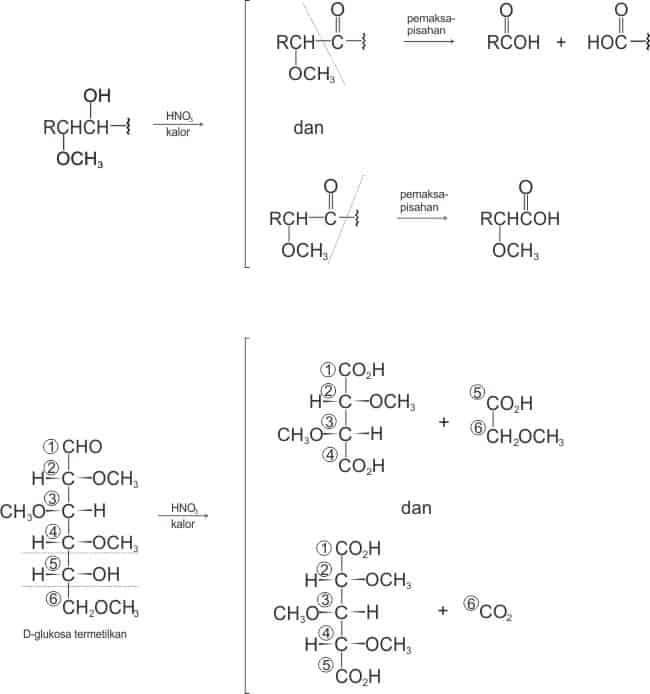
Suatu monosakarida bereaksi dengan dimetil sulfat untuk menghasilkan suatu struktur yang termetilkan secara lengkap. Dalam larutan asam, metil glikosida termetilkan dapat dihidrolisis dan cincinnya terbuka. Gugus-gugus metoksil, yang adalah eter, tidak dipengaruhi oleh reaksi ini. Oleh karena itu asetal yang terhidrolisis hanya mempunyai satu gugus hidroksil. Penentuan posisi gugus hidroksil ini merupakan informasi yang diperlukan untuk mengetahui ukuran cincin daria setal aslinya.
Posisi gugus OH ditentukan dengan oksidasi kuat dalam mana gugus —CHO diokasidasi menjadi —CO2H dan gugus OH tunggal dioksidasi menjadi suatu keton. Pada kondisi oksidasi ini, pemaksapisahan (cleavage) molekul terjadi di dekat gugus keton (pada kedua sisinya) untuk menghasilkan dua asam karboksilat.
Dari glukosa termetilkan, kedua dwiasam metoksi yang ditunjukan dalam persamaan di atas, dijumpai sebagai produk-produk utama (bersama-sama asam metoksiasetat dan CO2). Struktur kedua dwiasam itu ditentukan dengan membandingkan sifat fisisnya dengan sifat dwiasam metoksi yang strukturnya telah diketahui. Karena dwiasam produk ini merupakan derivat metoksi dari dwiasam empat dan lima karbon, maka disimpulkan bahwa karbon 5 mengikat gugus OH dalam glikosida terhidrolisis itu dan bahwa cincin glikosida asli adalah cincin enam-anggota.
Disakarida (Karbohidrat Gabungan Dua Monosakarida)
Suatu disakarida adalah suatu karbohidrat yang tersusun dari dua satuan monosakarida yang dipersatukan oleh suatu hubungan glikosida dari karbon 1 dari satu satuan ke suatu OH satuan lain. Suatu cara ikatan yang lazim ialah suatu hubungan glikosida α dan β dari satuan pertama ke gugus 4-hidroksil dari satuan kedua. Hubungan ini disebut suatu ikatan 1,4′-α atau 1,4′-β, bergantung pada stereokimia pada karbon glikosida.
Perhatikan struktur-struktur di atas ini dengan lebih cermat. Satuan 1 (satuan kiri dalam tiap struktur) mempunyai suatu ikatan β-glikosida ke satuan 2. Dalam larutan air, ikatan glikosida ini tetap tak berubah. Ikatan ini tidak berada dalam kesetimbangan dengan anomernya. Tetapi, satuan 2 (satuan kanan dalam tiap struktur) mengandung suatu gugus hemiasetal. Dalam larutan air, gugus khusus ini berada dalam kesetimbangan dengan bentuk aldehida rantai terbuka dan dengan anomer yang lain.
a. Maltosa
Disakarida maltosa digunakan dalam makanan bayi dan susu bubuk beragi (malted milk). Gula ini merupakan disakarida utama yang diperoleh dari hidrolisis pati. Pati diurai menjadi maltosa kelihatannya secara acak, oleh enzim yang terdapat dalam liur, yang disebut α-1,4-glukan 4-glukanohidrolase. Enzim α-1,4-glukan 4-maltohidrolase, yang terdapat dalam ekcambah jelai (malt), mengubah pati secara spesifik menjadi satuan maltosa. Dalam pembuatan bir, malt digunakan untuk mengubah pati dari gandum atau sumber lain menjadi maltosa. Enzim dalam ragi (α-glukosidase) mengkatalis hidrolisis maltosa menjadi D-glukosa, yang oleh enzim lain dalam ragi diubah menjadi etanol. Satu molekul maltosa menghasilkan dua molekul D-glukosa, tak peduli apakah hidrolisis berlangsung dalam sebuah labu laboratorium, dalam organisme, ataupun dalam tong peragian.
\scriptsize \text{pati} \xrightarrow[\text{H$^+$ atau enzim}]{\text{H$_2$O}} \text{maltosa} \xrightarrow[\text{H$^+$ atau enzim}]{\text{H$_2$O}} \text{D-glukosa} \xrightarrow[\text{enzim}]{} {\text{CH$_3$CH$_2$OH} \atop \text{etanol}}Suatu molekul maltosa mengandung dua satuan D-glikopiranosa. Satuan pertama (ditunjukan di kiri) adalah dalam bentuk α-glikosida. Satuan ini terikat ke oksigen pada karbon 4′ dalam satuan kedua oleh suatu hunungan 1,4′-α.
Karbon anomerik dari satuan kedua glukopiranosa dalam maltosa merupakan bagian dari suatu gugus hemiasetal. Akibatnya, terdapat dua bentuk maltosa (α- dan β-maltosa), yang berada dalam kesetimbangan satu sama lain dalam larutan. Maltosa mengalami mutarotasi, bersifat gula pereduksi, dan dapat dioksidasi menjadi asam maltobionat, suatu asam karboksilat, oleh suatu larutan air brom.
b. Selobiosa
Disakarida yang diperoleh dari hidrolisis parisal dari selulosa disebut selobiosa (cellobiose). Seperti maltosa, selobiosa tersusun dari dua satuan glukopiranosa yang digabung oleh suatu ikatan-1,4′. Selobiosa berbeda dari maltosa dalam hal ikatan-1,4 yang pada selobiosa lebih merupakan iaktan 1,4-β, bukan α.
Hidrolisis kimia dari selobiosa dalam asam berair menghasilkan suatu campuran α- dan β-D-glukosa, produk-produk yang sama seperti yang diperoleh dari maltosa. Selobiosa dapat juga dihidrolisis dengan enzim β-glukosidase (dikenal juga sebagai emulsin), tetapi tidak oleh α-glukosidase, yang bersifat spesifik untuk ikatan α (yakni maltosa).
c. Laktosa
Laktosa (gula susu) berbeda dari maltosa atau selobiosa dalam hal laktosa terdiri dari dua monosakarida atau karbohidrat sederhana yang berlainan, D-glukosa dan D-galaktosa.
Laktosa merupakan disakarida alamiah yang dijumpai hanya pada binatang mamalia. Air susu sapi dan manusia mengandung kira-kira sekitar 5% laktosa. Laktosa diperoleh secara komersial sebagai hasil samping produksi keju.
Pada metabolisme tubuh manusia yang normal, laktosa dihidrolisis secara enzimatis menjadi D-galaktosa dan D-glukosa kemudian galaktosa tersebut diubah menjadi glukosa untuk mengalami metabolisme selanjutnya. Suatu keadaan yang disebut galaktosemia terjadi pada bayi akibat kurangnya enzim untuk mengubah galaktosa menjadi glukosa.
Galaktosemia dicirikan oleh tingginya kadar galaktosa dalam darah dan urin. Gejalanya beraneka ragam mulai dari muntah-muntah sampai keterbelakangan mental dan jasmani serta dapat bersifat fatal. Pengobatannya dilakukan dengan menghilangkan susu dan produk susu dari diet. Sebagai penggantinya dapat diganti dengan susu kedelai.
d. Sukrosa
Sukrosa dalam sehari-hari adalah gula pasir atau gula tebu. Tebu sudah ditanam di pekarangan sejak tahun 6000 SM di India. Kata sugar dan sukrosa berasal dari bahasa Sansekerta sarkara. Pada tahun 325 SM Iskandar Agung menyerbu India dan menjumpai gula tebu ini. Setelah itu, penggunaan sukrosa tersebar baik melalui bangsa Aran maupun pejuang Perang Salib. Tebu kemudian dibawa oleh Columbus ke Amerika (Santo Dominggo) tahun 1493. Pada abad ke-18 ditemukan pula bahwa bit tertentu juga mengandung sukrosa dalam kadar tinggi. Penemuan ini menunjukan bahwa gula juga dapat diperoleh dari tumbuhan di daerah subtropis.
Baik gula yang berasal bit atau tebu, komposisi kimia dari gula adalah sama yakni berupa disakarida yang terdiri dari fruktosa dan glukosa. Ikatan glikosida menghubungkan karbon ketal dan asetal dan bersifat β dari fruktosa dan α dari glukosa. Perhatikan perbedaan antara sukrosa dan disakarida lain yang telah dibahas yaitu dalam sukrosa, kedua atom karbon anomerik (tidak sekedar satu) digunakan untuk ikatan glikosida. Dalam sukrosa, baik fruktosa maupun glukosa tidak memiliki gugus hemiasetal. Oleh sebab itu, sukrosa di air tidak berada dalam kesetimbangan dengan suatu bentuk aldehida atau keto. Sukrsa tidak menunjukan mutarotasi dan bukanlah gula pereduksi.
Gula inversi adalah campuran D-glukosa dan D-fruktosa yang diperoleh dengan hidrolisis asam atau enzimatik dari sukrosa. Enzim yang mengkatalis hidrolisis sukrosa disebut invertase, bersifat spesifik untuk ikatan β-D-fruktofuranosida dan terdapat dalam ragi dan lebah (madu terutama terdiri dari gula inversi). Karena adanya fruktosa bebas (gula termanis), gula inversi lebih manis dari pada sukrosa. Suatu gula inversi sintetik yang disebut isomerase dibuat dengan isomerasi enzimatik dari glukosa dalam sirup jagung (corn syrup). Penggunaan komersialnya adalah untuk pembuatan es krim, minuman ringan, dan permen.
Nama “gula inversi” diturunkan dari inversi (pembalikan) tanda rotasi jenis bila sukrosa dihidrolisis. Sukrosa mempunyai rotasi jenis +66,5°, suatu rotasi positif. Capuran produk (glukosa, [α] = +52,7°, dan fruktosa, [α] = -92,4°) mempunyai rotasi netto negatif.
Polisakarida: Karbohidrat Kompleks
Suatu polisakarida atau karbohdirat kompleks adalah senyawa dalam mana molekul-molekul mengandung banyak satuan monosakarida yang dipersatukan dengan ikatan glukosida. Hidrolisis lengkap akan mengubah suatu polisakarida menjadi monosakarida.
Polisakarida memenuhi tiga maksud dalam suatu kehidupan: sebagai bahan bangunan (arsitektural), bahan makanan (nutrisi), dan sebagai zat spesifik. Polisakarida arsitektural misalnya selulosa, yang memberikan kekuatan pada pokok kayu dan bahan bagi tumbuhan, dan kitin (chitin), komponen struktur dari kerangka luar serangga. Polisakarida nutrisi yang lazim ialah pati (starch) yang terdapat pada padi dan kentang, serta glikogen, karbohidrat siap pakai yang berada di dalam tubuh hewan terutama organ hati. Heparin, suatu contoh zat spesifik adalah suatu polisakarida yang mencegah koagulasi darah atau trombosis.
Polisakarida dapat juga terikat pada molekul tipe lainnya seperti dalam glikoprotein (kompleks polisakarida-protein) dan glikolipid (kompleks polisakarida-lipid).
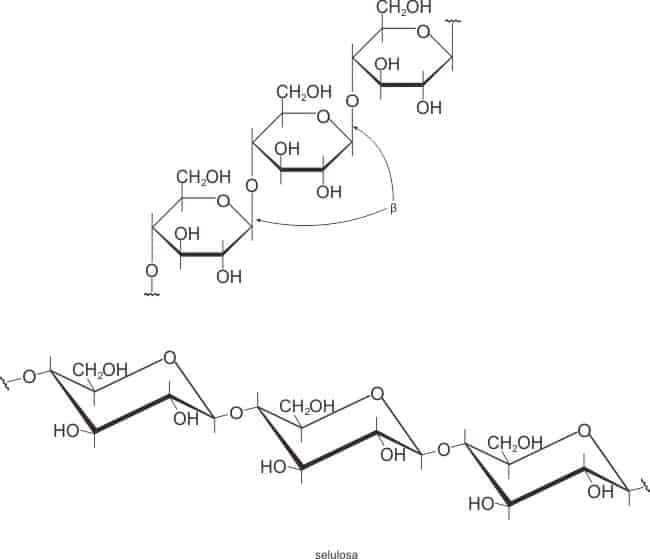
a. Selulosa
Selulosa merupakan senyawa organik yang paling melimpah di bumi. Diperkirakan sekitar 1011 ton selulosa disintesis setiap tahun. Selulosa mencakup sekitar 50% dari karbon tak bebas di bumi. Daun kering mengandung 10-20% selulosa; kayu 50%, dan kapas 90%. Sumber selulosa murni yang paling gampang di laboaratorium adalah kertas saring.
Selulosa membentuk komponen serat dari dinding sel tumbuhan. Ketegaran selulosa disebabkan oleh struktur keseluruhannya. Molekul selulosa merupakan rantai-rantai atau kirofibril dari D-glukosa sampai sebanyak 14.000 satuan yang terdapat sebagai berkas-berkas terpuntir mirip tali, yang terikat satu sama lain oleh ikatan hidrogen.
Suatu molekul tunggal selulosa merupakan polimer lurus dari 1,4′-β-D-glukosa. Hidrolisis lengkap dalam HCl 40% dalam air, hanya menghasilkan D-glukosa. Disakarida yang terisolasi dari selulosa yang terhidrolisis sebagian adalah selobiosa, yang dapat dihidrolisis lebih lanjut menjadi D-glukosa dengan suatu katalis asam atau dengan emulsin enzim. Selulosa sendiri tak mempunyai karbon hemiasetal-selulosa tak dapat mengalami mutarotasi atau dioksidasi oleh reagensia seperti reagensia Tollens. Mungkin terdapat suatu hemiasetal pada satu ujung dari tiap molekul selulosa, tetapi ujung ini hanya sebagian kecil dari keseluruhan dan tidak mengarah ke reaksi yang dapat diamati.
Meskipun binatang menyusui tidak mengeluarkan enzim yang sesuai untuk memecah selulosa menjadi glukosa, bakteri dan protozoa tertentu mengeluarkan enzim-enzim ini. Binatang pemakan rumput menggunakan selulosa sebagai makanan secara tidak langsung. Lambung dan ususnya dihuni oleh miroorganisme yang hidup dan berkembang biak pada selulosa; hewan itu memanfaatkan mikroorganisme ini dan hasil sampingannya sebagai makanan.
b. Pati
Pati merupakan polisakarida paling melimpah kedua setelah selulosa. Pati dapat dipisahkan menjadi dua fraksi utama berdasarkan kelarutan bila dibuburi (triturasi) dengan air panas: sekitar 20% pati adalah amilosa (larut) dan 80% sisanya adalah amilopektin (tidak larut).
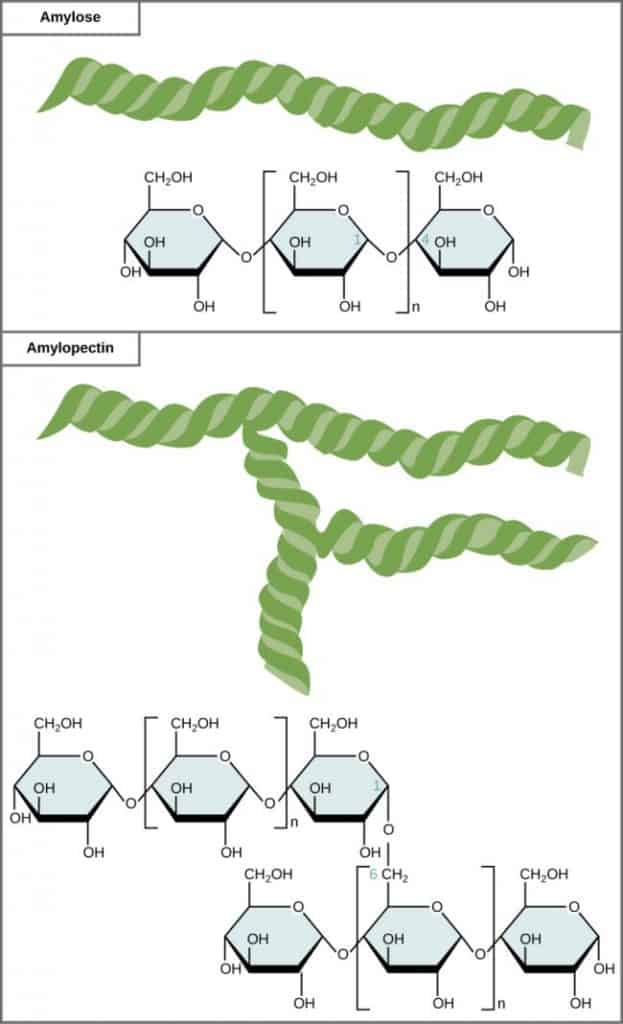
Amilosa
Hidrolisis lengkap amilosa menghasilkan hanya D-glukosa sedangkan hidrolisis parsial menghasilkan maltosa sebagai satu-satunya disakarida. Disimpulkan bahwa amilosa adalah polimer linear dari α-D-glukosa yang dihubungkan secara-1,4′. Beda antara amilosa dan selulosa ialah ikatan glikosidanya: β dalam selulosa dan α dalam amilosa. Perbedaan ini menjadi penyebab perbedaan sifat antara kedua polisakarida ini.
Terdapat 250 satuan glukosa glukosa atau lebih per molekul amilosa; banyaknya satuan bergantung spesies hewan atau tumbuhan tersebut. Pengukuran panjang rantai dikacaukan oleh fakta bahwa amilosa alamiah terdegradasi menjadi rantai yang lebih kecil selama pemisahan dan pemurnian.
Molekul amilosa membentuk spiral di sekitar molekul I2; timbul warna biru tua dari antaraksi antara keduanya. Warna ini merupakan dasar uji iod untuk pati, dalam mana suatu larutan iod ditambahkan ke suatu contoh yang tidak diketahui, untuk menguji hadirnya pati.
Amilopektin
Amilopektin merupakan suatu polisakarida yang jauh lebih besar ukurannya dari pada amilosa, mengandung 1000 satuan glukosa atau lebih sedikit per molekulnya. Seperti rantai dalam amilosa, rantai utama dari amilopektin mengandung 1,4′-α-D-glukosa. Tidak seperti amilosa, amilopektin bercabang sehingga terdapat satu glukosa ujung untuk kira-kira tiap 25 satuan glukosa. Ikatan pada titik percabangan ialah ikatan 1,6′-α-glikosida.
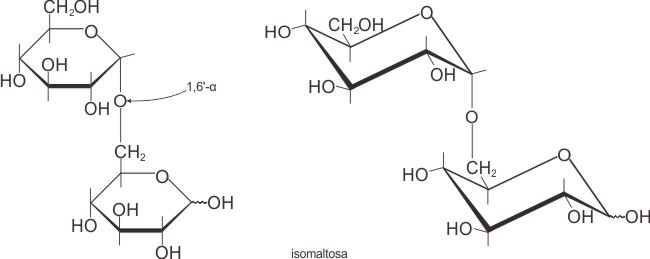
Hidrolisis lengkap amilopektin hanya menghasilkan D-glukosa. Namun hidrolisis tak lengkap menghasilkan suatu campuran disakarida maltosa dan isomaltosa, yang kedua ini berasal dari percabangan 1,6′. Campuran oligosakarida yang diperoleh dari hidrolisis parsial amilopektin, yang biasa dirujuk sebagai dekstrin, digunakan untuk membuat lem, pasta dan kanji tekstil.
\scriptsize \text{amilopektin} \xrightarrow[]{\text{H$_2$O}} \text{dekstrin} \xrightarrow[]{\text{H$_2$O}} \text{maltosa} +\text{isomaltosa} \xrightarrow[]{\text{H$_2$O}} \text{D-glukosa}Glikogen
Glikogen merupakan polisakarida yang digunakan untuk menyimpan glukosa pada hewan dan disimpan terutama di hati dan otot. Dari segi struktur, glikogen mirip amilopektin. Glikogen mengandung rantai glukosa yang terikat 1,4′-α dengan percabangan-percabangan (1,6′-α). Beda antara glikogen dan amilopektin ialah bahwa glikogen lebih bercabang dari pada amilopektin.
c. Kitin
Polisakarida yang merupakan bangunan utama dari hewan berkaki banyak (misalnya, ketam dan serangga) adalah kitin (chitin). Diperkirakan bahwa 109 ton kitin dibiosintesis di bumi tiap tahun. Kitin adalah polisakarida linear yang mengandung N-asetil-D-glukosamina terikat β. Pada hidrolisis, kitin menghasilkan 2-amino-2-deoksi-D-glukosa. Gugus asetat terkeoas dalam tahap hidrolisis. Dalam alam, kitin terikat pada bahan bukan polisakarida (protein dan lipid).

Kesimpulan
Karbohidrat merupakan senyawa aldehida dan keton polihidroksi atau derivatnya. Bentuk karbohidrat paling sederhana adalah monosakarida dan tidak dapat dihidrolisis menjadi satuan yang lebih kecil lagi. Pada makhluk hidup, karbohidrat memegang fungsi penting baik sebagai sumber energi (proses glikolisis, dekarboksikasi oksidatif), fungsi struktural, maupun fungsi khusus lainnya. Dengan mempelajari struktur molekul karbohidrat maupun reaksi penting yang berhubungan dapat membantu memahami kunci peran karbohidrat pada kehidupan kita sehari-hari.
Referensi
- Carbohydrates(Opens in a new window),” by OpenStax College, Biology (CC BY 3.0). Download the original article for free at http://cnx.org/contents/185cbf87-c72e-48f5-b51e-f14f21b5eabd@9.85:11/Biology.
- Fessenden RJ, Fessenden JS. Organic chemistry. 3rd ed. Belmont: Wadsworth; 1986.

Seorang dokter, saat ini sedang menjalani pendidikan dokter spesialis penyakit dalam FKUI. Peminat berbagai topik sejarah dan astronomi.